Hvad bestemmer den kemiske energi, der er lagret i et stof?
Hvad bestemmer den kemiske energi, der er lagret i et stof?
Mængden af kemisk energi et stof kan levere er kodet i de bindinger, der holder dets atomer sammen. Under en kemisk reaktion brydes disse bindinger og omdannes, og nettoenergiændringen afhænger af den relative styrke af de involverede bindinger.
Typer af kemiske bindinger
Atomer er forbundet med forskellige slags bindinger - kovalente, ioniske, metalliske og hydrogen - hver bærer en karakteristisk mængde energi. Kovalente bindinger, dannet ved elektrondeling, er typisk de stærkeste og lagrer dermed mest energi (f.eks. O-H-bindingerne i vand). Ionbindinger, såsom Na⁺–Cl⁻ i bordsalt, er svagere, mens hydrogenbindinger mellem vandmolekyler er blandt de svageste.
Måling af energi i reaktioner
I praksis registrerer en kemiker mængden af reaktanter, temperaturen og trykket før og efter en reaktion. Kun nettoændringen i bindingsenergi har betydning:Hvis bindingerne i produkterne indeholder mindre energi end i reaktanterne, frigives varme (en eksoterm proces). Omvendt, hvis produkterne besidder mere energi, absorberer reaktionen varme fra omgivelserne (endotermisk).
Eksoterme vs. endoterme reaktioner
Eksoterme reaktioner frigiver varme, fx forbrænding af træ, hvor kulstof og brint reagerer med ilt og danner CO₂ og H₂O. Endoterme reaktioner forbruger varme, såsom opløsning af NaCl i vand, hvilket sænker opløsningens temperatur lidt.
Spontane vs. ikke-spontane reaktioner
Hvorvidt en reaktion sker af sig selv, afhænger af systemets frie energi. Spontane reaktioner, som natriummetal, der reagerer voldsomt med vand, forløber uden ekstern input. Ikke-spontane reaktioner, såsom antændelse af benzin, kræver en energitilførsel (f.eks. en gnist) for at krydse en aktiveringsbarriere.
Forståelse af disse principper gør det muligt for kemikere at forudsige og kontrollere energistrømmen i kemiske processer.
 Varme artikler
Varme artikler
-
 Enhedsopdatering muliggør mobiltest for vira, bakterier og aktive toksinerSandia National Laboratories kemiker Chung-Yan Koh, venstre, og tidligere Sandia bioingeniør Chris Phaneuf, ret, behold den nyligt opdaterede SpinDx diagnostiske enhed. Kredit:Jules Bernstein Du s
Enhedsopdatering muliggør mobiltest for vira, bakterier og aktive toksinerSandia National Laboratories kemiker Chung-Yan Koh, venstre, og tidligere Sandia bioingeniør Chris Phaneuf, ret, behold den nyligt opdaterede SpinDx diagnostiske enhed. Kredit:Jules Bernstein Du s -
 Fuldt inkjet-printede vanadiumdioxid-baserede radiofrekvensomskiftere til fleksible rekonfigurerbare…To termisk og elektrisk responsive kontaktkonfigurationer på en safiroverflade. Kredit:KAUST Inkjet-printede switche gør flere frekvensbånd nemmere og billigere at administrere i trådløse enheder.
Fuldt inkjet-printede vanadiumdioxid-baserede radiofrekvensomskiftere til fleksible rekonfigurerbare…To termisk og elektrisk responsive kontaktkonfigurationer på en safiroverflade. Kredit:KAUST Inkjet-printede switche gør flere frekvensbånd nemmere og billigere at administrere i trådløse enheder. -
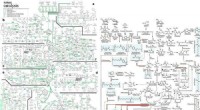 Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re
Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re -
 Video:Glaspusteriets kunst og videnskabKredit:The American Chemical Society Hvis du nogensinde har trykket på en skærm for at sende et tweet, valgt en sodavand på glasflaske på grund af smag, eller savlede over kunstglas i et galleri,
Video:Glaspusteriets kunst og videnskabKredit:The American Chemical Society Hvis du nogensinde har trykket på en skærm for at sende et tweet, valgt en sodavand på glasflaske på grund af smag, eller savlede over kunstglas i et galleri,
- Hvilken videnskabsmand studerer alle aspekter af samfundet og de interpersonelle forhold mennesker i…
- Magnetiske nanopartikler Fjerner ovariecancerceller fra bughulen
- Hvordan påvirker den ekstreme temperaturfølsomhed af CNO -cyklus strukturstjerner?
- Beskriv de 3 mulige mors og måneskør?
- Hvor loftsventilator konverterer elektrisk energi til mekanisk energi?
- Hvilken organisme har silicapægge?


