Beregning af enzymkatalytisk effektivitet:En praktisk vejledning
Af Kevin Beck
Opdateret 30. august 2022
Enzymer er biologiske katalysatorer, der accelererer reaktioner ved at sænke aktiveringsenergien uden at ændre termodynamikken af reaktanterne eller produkterne. Deres bemærkelsesværdige specificitet – ofte sammenlignet med en lås-og-nøgle-mekanisme – gør dem uundværlige i både fysiologi og bioteknologi. At forstå, hvor effektivt et enzym udfører sit job, er afgørende for lægemiddeludvikling, metabolisk konstruktion og diagnostiske analyser.
Enzyme Basics
Hvert enzym er et unikt protein sammensat af en sekvens af aminosyrer. Det aktive sted, dannet af specifikke rester, binder et enkelt substratmolekyle ("nøglen") og letter dets omdannelse til et produkt. Fordi enzymer ikke forbruges i reaktionen, kan de gentagne gange binde nye substratmolekyler, hvilket skaber et enzym-substratkompleks, der i sidste ende frigiver produktet.
Enzymkinetik
Den katalytiske cyklus kan repræsenteres som:
E + S ⇔ ES → E + P
Her, E er enzymet S substratet, ES enzym-substratkomplekset og P produktet. Den reversible dannelse af ES afspejler den dynamiske ligevægt mellem binding og dissociation, mens omdannelsen til produkt er effektivt irreversibel under fysiologiske forhold.
Kurskonstanter
Tre elementære trin styrer reaktionen:
- Bindende:E + S → ES med hastighedskonstant k1
- Dissociation:ES → E + S med hastighedskonstant k-1
- Katalyse:ES → E + P med hastighedskonstant k2 (kkat )
Michaelis konstant og enzymeffektivitet
Under steady-state forhold, hastigheden af produktdannelse (hastighed, v ) er:
v =k2 [ES]
Fordi dannelsen og nedbrydningen af ES er afbalancerede, har vi:
k1 [E][S] =k2 [ES] + k-1 [ES]
Omarrangering giver Michaelis-konstanten, KM =(k2 + k-1 )/k1 :
[E][S] =KM [ES]
Substituering i hastighedsligningen giver den velkendte Michaelis-Menten-form:
v =(k2 /KM )·[E][S]
Forholdet k2 /KM kaldes specificitet eller kinetisk effektivitet konstant. Det indkapsler både den katalytiske omsætningshastighed og affiniteten til substrat, hvilket giver en enkelt metrik til sammenligning af enzymer under identiske forhold.
For at beregne denne effektivitet ud fra eksperimentelle data skal du omarrangere ligningen:
k2 /KM =v / ([E][S])
Ved at måle reaktionshastigheden (v ), enzymkoncentration ([E] ), og substratkoncentration ([S] ), kan forskere kvantificere, hvor effektivt et enzym omdanner substrat til produkt, vejleder enzymvalg i industrielle processer og informerer om terapeutisk enzymdesign.
 Varme artikler
Varme artikler
-
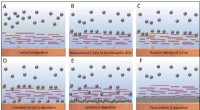 At overvinde et batteris fatale fejlSkema af litumaflejringsmekanisme i tilfælde af grafenoxid-modificerede prøver. A-F) Adsorption af Li-ioner til den lithiofile GOn-belægning og kontrolleret levering på stedet af Li-ioner til metalove
At overvinde et batteris fatale fejlSkema af litumaflejringsmekanisme i tilfælde af grafenoxid-modificerede prøver. A-F) Adsorption af Li-ioner til den lithiofile GOn-belægning og kontrolleret levering på stedet af Li-ioner til metalove -
 Ny filtreringsmetode lover sikrere drikkevand, forbedret industriproduktionKredit:Pixabay/CC0 Public Domain Et team af forskere ved Tufts University School of Engineering har udviklet en ny filtreringsteknologi. Inspireret af biologi, det kunne hjælpe med at dæmme op for
Ny filtreringsmetode lover sikrere drikkevand, forbedret industriproduktionKredit:Pixabay/CC0 Public Domain Et team af forskere ved Tufts University School of Engineering har udviklet en ny filtreringsteknologi. Inspireret af biologi, det kunne hjælpe med at dæmme op for -
 Ny sommerfugl-inspireret brintsensor drives af lysPh.d.-forsker Ebtsam Alenezy har en prototype af den lysaktiverede brintsensor, som kan levere ultrapræcise resultater ved stuetemperatur. Kredit:RMIT University Inspireret af overfladen af somm
Ny sommerfugl-inspireret brintsensor drives af lysPh.d.-forsker Ebtsam Alenezy har en prototype af den lysaktiverede brintsensor, som kan levere ultrapræcise resultater ved stuetemperatur. Kredit:RMIT University Inspireret af overfladen af somm -
 Løftet om dybe rillerDette viser siliciumskiver, i størrelse fra 4 ”til 12” diameter, som er blevet behandlet ved hjælp af Argonnes sekventielle infiltrationssyntesemetode. Kredit:Argonne National Laboratory En fremst
Løftet om dybe rillerDette viser siliciumskiver, i størrelse fra 4 ”til 12” diameter, som er blevet behandlet ved hjælp af Argonnes sekventielle infiltrationssyntesemetode. Kredit:Argonne National Laboratory En fremst
- Er peroxid på en øm kemisk forandring?
- Simple Hydraulic Projects for Science
- Hvad er tilstanden af stof zink ved 25 grader celsius?
- Ny tilgang viser løfte om at overvinde flaskehalsen med blå emission i skærme, der bruger OLED'er
- Billede:Kaotiske skyer af Jupiter
- Skinnende lys på det undvigende carbon nanorør


