En praktisk guide til de seks kernetyper af kemiske reaktioner
Af Lan Luo
Opdateret 30. august 2022
Jardul/iStock/GettyImages
Kemiske reaktioner er en integreret del af moderne teknologi og hverdagsliv – fra at drive motorer til at brygge drikkevarer. De driver også naturlige processer såsom fotosyntese og stenforvitring.
Tre brede kategorier af reaktioner
Fysiske reaktioner kun indebære en ændring i tilstand eller fysisk arrangement, uden ændring af stoffernes kemiske identitet. For eksempel frysevand:
H2O(l) → H2O(s)
Kemiske reaktioner omdanne reaktanter til nye produkter gennem omlejring af atomer. Et klassisk eksempel er at opløse CO₂ i vand for at danne kulsyre:
CO₂(g) + H₂O(l) → H₂CO₃(aq)
Atomreaktioner involverer ændringer i atomkerner, såsom Rutherfords transmutation af nitrogen:
¹⁴N + α → ¹⁷O + p
De seks centrale kemiske reaktionstyper
Syntese (kombinations) reaktion
To eller flere reaktanter kombineres for at producere et enkelt, mere komplekst produkt. Generel form:
A + B → AB
Eksempler:
Fe(s) + S(s) → FeS(s)
2Na(s) + Cl2(g) → 2NaCl(s)
Dekomponeringsreaktion
En enkelt kompleks reaktant bryder i to eller flere enklere produkter. Generel form:
AB → A + B
Eksempler:
H2O(l) → H₂(g) + O₂(g) (elektrolyse)
H₂CO₃(aq) → H2O(l) + CO₂(g) (termisk nedbrydning)
Enkeltforskydningsreaktion (erstatning)
Et grundstof fortrænger et andet fra en forbindelse. Generel form:
A + BC → AC + B
Eksempler:
Mg(s) + 2HCl(aq) → H2(g) + MgCl2(aq)
Mg(s) + 2H2O(l) → H2(g) + Mg(OH)2(aq)
Dobbeltforskydningsreaktion (metatese)
Kationer og anioner bytter partnere og danner to nye forbindelser. Generel form:
AB + CD → AD + CB
Eksempler:
BaCl2 + MgS04 -> BaS04 + MgCl2
Pb(NO3)2 + 2KI → PbI2 + 2KNO3
Forbrændingsreaktion
En eksoterm redoxproces, hvor et brændstof reagerer med oxygen og producerer hovedsageligt CO₂ og H₂O. Fuldstændig forbrænding:
4CxHy + (4x+y)O₂ → 4xCO₂ + 2yH₂O + varme
Specifikke eksempler:
CH4 + 2O₂ → CO₂ + 2H₂O + varme (≈891kJmol⁻¹)
C₁₀H₈ + 12O₂ → 10CO₂ + 4H2O + varme
CH3OH + O₂ → CO₂ + 2H2O + varme
Ufuldstændig forbrænding opstår, når O₂ er begrænset, hvilket producerer CO, sod eller andre biprodukter.
Syre-basereaktion
En neutraliseringsproces, hvor en syre reagerer med en base og danner et salt og vand. Det er et særligt tilfælde af dobbelt forskydning:
HA + BOH → BA + H2O
Eksempler:
Ca(OH)2 + 2HCl → CaCl2 + 2H20
CH3COOH + NaHCO3 → CH3COONa + H2O + CO2
Hvorfor er det vigtigt at forstå disse typer
Genkendelse af reaktionsmønstret hjælper kemikere og ingeniører med at forudsige produkter, optimere forhold og sikre sikkerhed - især i industriel forbrænding eller farmaceutisk syntese.
 Varme artikler
Varme artikler
-
 DIY saltvandsopløsning:Simpelt hjemmemiddel til klare næsepassagerZinkevych/iStock/GettyImages Når en forkølelse eller bihulebetændelse opstår, kan saltvand hjælpe dig med at trække vejret. Vanding kan åbne næsepassagerne og give lindring fra elendigheden med tilst
DIY saltvandsopløsning:Simpelt hjemmemiddel til klare næsepassagerZinkevych/iStock/GettyImages Når en forkølelse eller bihulebetændelse opstår, kan saltvand hjælpe dig med at trække vejret. Vanding kan åbne næsepassagerne og give lindring fra elendigheden med tilst -
 Retsmedicinsk kemiker opdager brug af marihuana baseret på svedtestUAlbany retsmedicinsk kemiker Jan Halámek med kandidatstuderende forsker Mindy Hair. Kredit:Scott Freedman Retsmedicinsk kemiker Jan Halámek beviser, at vores egen sved ikke kun fortæller, hvor fu
Retsmedicinsk kemiker opdager brug af marihuana baseret på svedtestUAlbany retsmedicinsk kemiker Jan Halámek med kandidatstuderende forsker Mindy Hair. Kredit:Scott Freedman Retsmedicinsk kemiker Jan Halámek beviser, at vores egen sved ikke kun fortæller, hvor fu -
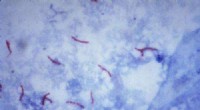 Lille robot kunne være game-changer i kampen mod tuberkuloseDette mikrofotografi afslører Mycobacterium tuberculosis-bakterier ved hjælp af syrefast Ziehl-Neelsen-farve; Forstørret 1000 X. De syrefaste pletter afhænger af mykobakteriers evne til at tilbagehold
Lille robot kunne være game-changer i kampen mod tuberkuloseDette mikrofotografi afslører Mycobacterium tuberculosis-bakterier ved hjælp af syrefast Ziehl-Neelsen-farve; Forstørret 1000 X. De syrefaste pletter afhænger af mykobakteriers evne til at tilbagehold -
 Touchscreen-alternativ dæmper frygten for verdensmangel på indiumDet nye materiale er skabt ved hjælp af en proces kaldet plasmasputtering. Kredit:Behnam Akhavan Har du nogensinde forestillet dig din smartphone eller tablet uden en berøringsskærm? Dette kan sna
Touchscreen-alternativ dæmper frygten for verdensmangel på indiumDet nye materiale er skabt ved hjælp af en proces kaldet plasmasputtering. Kredit:Behnam Akhavan Har du nogensinde forestillet dig din smartphone eller tablet uden en berøringsskærm? Dette kan sna
- Byplanlægning bør overveje bygningshøjde, form og arrangement for at beskytte fodgængere under r…
- Hvad er det atomnummer, der bruges til?
- Hvilken stjerne er lysere end Sirius?
- 'Råbeafstand':Så tæt ville Inflations Reduction Act bringe USA på deres klimamål
- Hvad er formlen for at finde kraft, når masse og acceleration er kendt?
- Målet for den mængde elektriske energi, der overføres med en elektrisk ladning, er?


