Bestemmelse af, om atomer er polære eller ikke-polære:En praktisk vejledning
Af Jess Kroll, Opdateret 24. marts 2022
Når atomer danner kovalente bindinger, deler de elektroner for at skabe et stabilt molekyle. Hvis et atom har et stærkere træk på de delte elektroner, får det en delvis negativ ladning, mens det andet atom bærer en delvis positiv ladning. Denne ulige ladningsfordeling definerer et polært molekyle, hvorimod en jævn fordeling resulterer i et ikke-polært molekyle. Følg disse trin for at vurdere, om et specifikt atom er polært eller ikke-polært.
Trin 1:Identificer obligationstypen
Først skal du bestemme, om bindingen er kovalent eller ionisk. Ionbindinger dannes mellem ioner - atomer, der har fået eller mistet elektroner og bærer en nettoladning. Da ionbindinger involverer ladede arter, beskrives atomerne i sig selv ikke som polære eller ikke-polære i sammenhæng med molekylær polaritet. I modsætning hertil involverer kovalente bindinger neutrale atomer, der deler elektroner, og kun atomer i sådanne bindinger kan udvise polaritet.
Trin 2:Undersøg atomsammensætningen
Dernæst skal du se på de grundstoffer, der udgør molekylet. Homonukleære bindinger (f.eks. N₂, O₂, O₃) deler elektroner ligeligt, hvilket gør atomerne upolære. Heteronukleære bindinger - dem mellem forskellige elementer - har tendens til at være polære, fordi atomerne har forskellige elektronegativiteter. Eksempler omfatter CO₂, hvor carbon-oxygen-bindingerne er polære, og H₂O, hvor hydrogen-oxygen-bindingerne er stærkt polære. Hvis et molekyle indeholder mere end ét grundstof, er atomerne involveret i heteronukleære bindinger typisk polære.
Trin 3:Vurder molekylær geometri
Til sidst skal du vurdere molekylets overordnede form. Symmetriske arrangementer kan udligne individuelle dipolmomenter, hvilket gør hele molekylet upolært, selvom dets atomer er polære. For eksempel er CO₂ lineær og ikke-polær, fordi dens to polære bindinger er spejlbilleder. Asymmetriske molekyler, såsom vand (H2O), har et netto dipolmoment og klassificeres som polære. Dette trin er afgørende for at forudsige stoffets fysiske egenskaber.
Disse principper er grundlæggende i kemiundervisning og bruges af videnskabsmænd til at forudsige reaktivitet, opløselighed og andre nøgleegenskaber ved forbindelser.
 Varme artikler
Varme artikler
-
 Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at
Forskere bringer polymerer i fokus på atomskalaEn gengivelse (grå og pink) af den molekylære struktur af en peptoid polymer, der blev undersøgt af et team ledet af Berkeley Lab og UC Berkeley. Holdets succes med at afbilde polymerers struktur i at -
 Forskere skaber en mere effektiv hydrogel til at hele sårElektronmikroskopbillede af den porøse hydrogel. Kredit:UNH Forskere ved University of New Hampshire har skabt en nem at lave, lavpris injicerbar hydrogel, der kan hjælpe sår med at hele hurtigere
Forskere skaber en mere effektiv hydrogel til at hele sårElektronmikroskopbillede af den porøse hydrogel. Kredit:UNH Forskere ved University of New Hampshire har skabt en nem at lave, lavpris injicerbar hydrogel, der kan hjælpe sår med at hele hurtigere -
 Sundhedsbehandling gennem kemisk synteseArbejder i farmaceutisk kemi, vores primære mål er at forberede molekyler til at tackle sundhedsproblemer – Vittorio Pace er gruppeleder i syntetisk kemi ved universitetet i Wien. Kredit:rizenagard/pi
Sundhedsbehandling gennem kemisk synteseArbejder i farmaceutisk kemi, vores primære mål er at forberede molekyler til at tackle sundhedsproblemer – Vittorio Pace er gruppeleder i syntetisk kemi ved universitetet i Wien. Kredit:rizenagard/pi -
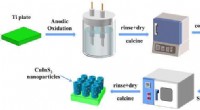 CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto
CuInS2/TiO2-fotoanodekompositter klarer sig godt i foto-induceret katodisk beskyttelseGrafisk abstrakt. Kredit:Journal of Materials Science &Technology (2022). DOI:10.1016/j.jmst.2022.02.011 Fotogenereret katodisk beskyttelsesteknologi som en værdifuld gren af fotokatalyse og foto


