Videnskaben bag vaskemidler:hvordan de reducerer vandoverfladespændingen
Af Athena Hessong Opdateret 24. marts 2022
Kwangmoozaa/iStock/GettyImages
Detergentmolekyler har en meget smart egenskab, hvor den ene ende er hydrofil eller vandelskende, og den anden er hydrofob eller frastødes af vand. Denne dobbelte natur gør det muligt for vaskemidlet at tiltrække både vand og olie, hvilket giver det dens evne til at rense dit vasketøj. Det er også meget effektivt til at reducere overfladespændingen af vand ved at skubbe vandmolekyler fra hinanden med den hydrofobe ende af vaskemiddelmolekylet.
Vandmolekyler og overfladespænding
Vandmolekyler og overfladespænding
Vand har unikke egenskaber, som gør det "klæbrigt" ved overfladen. Hvert individuelt vandmolekyle har et stort oxygenatom og to mindre brintatomer. Brintatomerne holder en let positiv ladning, hvilket gør hele vandmolekylet polært. Ligesom små magneter tiltrækker brintatomerne oxygenatomerne fra andre vandmolekyler og skaber midlertidige brintbindinger i vandet.
Hvert vandmolekyle oplever et træk fra andre vandmolekyler fra alle retninger, men vandmolekyler ved overfladen har ikke molekyler over overfladen til at trække i dem. Disse vandmolekyler har mere træk fra vandet nedenunder end overfladen over. Denne forskel i kraft pakker vandmolekylerne ved overfladen tættere sammen, end de er inde i væsken. Det tynde, tætte lag af molekyler frembringer det fænomen, der kaldes overfladespænding.
Vaskemiddel og sæbe
Vaskemiddel og sæbe
Vaskemiddel og sæbe ligner hinanden kemisk, bortset fra olien i dem. Mange sæber bruger naturlige fedtstoffer, mens rengøringsmidler bruger raffineret petroleum. Sæbe- og vaskemiddelmolekyler har to ender, der fungerer som en bro mellem vandmolekyler og fedt (fedt)molekyler. Dette gør det muligt for sæben eller opvaskemidlet at gribe fat i fedtet fra et snavset fad og bruge den anden ende af vaskemiddelmolekylet til at låse sig fast på vand, der skal vaskes væk.
Vaskemiddel- og sæbebrudsoverfladespænding
Vaskemiddel- og sæbebrudsoverfladespænding
Vaskemiddelmolekylers to ender gør det i stand til at bryde gennem vands overfladespænding. Den ende af vaskemiddelmolekylet, som binder til fedt (fedt), afviser vandmolekyler. Det er kendt som hydrofobisk, hvilket betyder "vandfrygt". Ved at forsøge at bevæge sig væk fra vandmolekylerne skubber de hydrofobe ender af vaskemiddelmolekylerne op til overfladen. Dette svækker hydrogenbindingerne, der holder vandmolekylerne sammen ved overfladen. Resultatet er et brud i vandets overfladespænding.
 Varme artikler
Varme artikler
-
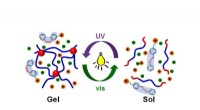 Fotoreversibel molekylær switch ændrer den fysiske egenskab af termoresponsiv polymerSkematisk illustration af sol-gelovergang udløst af fotoisomerisering af azobenezen-holdig ionisk flydende molekylær switch. Kredit:Yokohama National University Forskere har udviklet en ny strateg
Fotoreversibel molekylær switch ændrer den fysiske egenskab af termoresponsiv polymerSkematisk illustration af sol-gelovergang udløst af fotoisomerisering af azobenezen-holdig ionisk flydende molekylær switch. Kredit:Yokohama National University Forskere har udviklet en ny strateg -
 Enkel og omkostningseffektiv udvinding af sjældne metaller fra industriaffaldKredit:CC0 Public Domain Mange sjældne metaller er mangelfulde, alligevel efterspørgsel efter brug i elektronik, medicinsk instrumentering, og andre formål fortsætter med at stige. Som affald, dis
Enkel og omkostningseffektiv udvinding af sjældne metaller fra industriaffaldKredit:CC0 Public Domain Mange sjældne metaller er mangelfulde, alligevel efterspørgsel efter brug i elektronik, medicinsk instrumentering, og andre formål fortsætter med at stige. Som affald, dis -
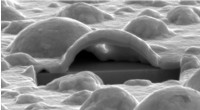 Platin danner nano-boblerElektronmikroskopudsigt ind i det indre af en platinboble. Tværsnittet blev eksponeret med en fokuseret ionstråle. Under den hule Pt-boble kan den kantede YSZ-krystal ses. Kredit:DESY, Satishkumar Kul
Platin danner nano-boblerElektronmikroskopudsigt ind i det indre af en platinboble. Tværsnittet blev eksponeret med en fokuseret ionstråle. Under den hule Pt-boble kan den kantede YSZ-krystal ses. Kredit:DESY, Satishkumar Kul -
 Farveændrende kontaktlinse kan forbedre overvågningen af behandlinger med øjensygdommeKontaktlinser, der skifter farve efter at have frigivet lægemidler i øjet, kan hjælpe læger med at afgøre, om en medicin bliver leveret til det tilsigtede behandlingssted. Kredit:American Chemical Soc
Farveændrende kontaktlinse kan forbedre overvågningen af behandlinger med øjensygdommeKontaktlinser, der skifter farve efter at have frigivet lægemidler i øjet, kan hjælpe læger med at afgøre, om en medicin bliver leveret til det tilsigtede behandlingssted. Kredit:American Chemical Soc
- Hvor mange elektroner er den ydre skal af klor?
- Enhed i den celle, hvor DNA er delt og pakket?
- Hvem er far til menneskelig geologi?
- Ingeniører udvikler tynde, letvægts linse, der kunne producere slankere kameratelefoner, længere …
- En universel indsættelse af forskellige molekyler i ioniske krystaller under højt tryk
- Rapport:Klimaændringer skader flere verdensarvssteder


