Beregn kemiske koncentrationer ud fra absorption med Beer-Lambert Law
Af Riti Gupta — Opdateret 24. marts 2022
Nøjagtig bestemmelse af koncentrationen af reagenser og produkter er afgørende i ethvert laboratorieeksperiment. Ved at måle, hvor meget lys en opløsning absorberer, kan videnskabsmænd udlede koncentrationen af den absorberende art ved hjælp af den veletablerede Beer-Lambert-lov.
Hvad er Beer-Lambert-loven?
Beer-Lambert-loven beskriver, hvordan lysets intensitet aftager, når det passerer gennem et materiale. Ved ultraviolet-synlig (UV-Vis) spektroskopi skinner en lysstråle gennem en prøve; den del, der ikke transmitteres, absorberes af molekylerne i opløsningen.
Det absorberede lys er proportional med to faktorer:lysets vejlængde gennem prøven (l) og koncentrationen af den absorberende art (c). Loven er udtrykt som:
A =log (I0 / I) =εlc
Her A er absorbansen (en enhedsløs mængde), I0 er den indfaldende lysintensitet, I er den transmitterede lysintensitet, ε er den molære absorptionsevne (eller molær ekstinktionskoefficient), og l er stiens længde.
Enheder og øllov
For at anvende ligningen korrekt skal hver variabel udtrykkes i dens standardenheder:
- Koncentration (c):mol pr. liter (molL –1 eller M)
- Stierængde (l):centimeter (cm)
- Molar absorptionsevne (ε):liter pr. mol-centimeter (Lmol –1 cm –1 )
Når disse enheder kombineres, er resultatet en dimensionsløs absorbans, som forventet.
Brug af Beers lov til at beregne koncentration
Antag, at du ønsker at bestemme koncentrationen af fødevarefarvestoffet Red#40 i en opløsning. Farvestoffet har en molær absorptionsevne på 25.900 Lmol –1 cm –1 ved 501nm. Du placerer 1mL af opløsningen i en kuvette med en banelængde på 1 cm og måler en absorbans på 0,17.
Tilføjelse af de kendte værdier i Beer-Lambert-ligningen giver:
0,17 =(25.900 Lmol –1 cm –1 )×(1cm)×c
Løsning for koncentration:
c =6,56×10 –6 M
For lettere fortolkning er dette ofte udtrykt i mikromolar:
c =6,56 µM
Red#40-opløsningen har således en koncentration på 6,56 µM.
Ved at mestre Beer-Lambert-loven kan forskere pålideligt kvantificere analytter i opløsning, spore reaktionsforløb og sikre nøjagtige eksperimentelle forhold.
 Varme artikler
Varme artikler
-
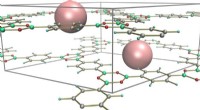 Porøse polymerer viser bemærkelsesværdig stabilitet ved højt trykPorøst nanomateriale kaldet COFer (kovalente organiske rammer). Kredit:Alexandr Talyzin Umeå-fysikere i samarbejde med Dresdens Tekniske Universitet og Chalmers Universitet er de første til at vis
Porøse polymerer viser bemærkelsesværdig stabilitet ved højt trykPorøst nanomateriale kaldet COFer (kovalente organiske rammer). Kredit:Alexandr Talyzin Umeå-fysikere i samarbejde med Dresdens Tekniske Universitet og Chalmers Universitet er de første til at vis -
 Nyt værktøj til at forudsige polymeregenskaberKredit:Gent Universitet Et tværfagligt team af forskere har udviklet et kraftfuldt matematisk modelleringsværktøj, der vil give forskere mulighed for at forudsige egenskaberne af polymernetværk, f
Nyt værktøj til at forudsige polymeregenskaberKredit:Gent Universitet Et tværfagligt team af forskere har udviklet et kraftfuldt matematisk modelleringsværktøj, der vil give forskere mulighed for at forudsige egenskaberne af polymernetværk, f -
 Forskere udvikler smartphone-læser til hurtigere infektionstestWSU-professor Lei Li og kandidatstuderende Yu-Chung Chang (l-r) tester den nye smartphone, der opdager 12 almindelige virale og bakterielle infektionssygdomme. Kredit:Washington State University W
Forskere udvikler smartphone-læser til hurtigere infektionstestWSU-professor Lei Li og kandidatstuderende Yu-Chung Chang (l-r) tester den nye smartphone, der opdager 12 almindelige virale og bakterielle infektionssygdomme. Kredit:Washington State University W -
 Neutronstråle fra atomreaktor bruges til at producere sikrere bilerPrøveklemningstrin på hexapod -bevægelig platform for at muliggøre præcis prøveoversættelse gennem neutronstråle. Kredit:University of Warwick Et partnerskab ledet af WMG ved University of Warwick
Neutronstråle fra atomreaktor bruges til at producere sikrere bilerPrøveklemningstrin på hexapod -bevægelig platform for at muliggøre præcis prøveoversættelse gennem neutronstråle. Kredit:University of Warwick Et partnerskab ledet af WMG ved University of Warwick
- Hvad er det materiale, gennem hvilket lys rejser (som luft eller vand) kaldes?
- Beskriv tilstanden af Matter Mercury og bevægelse dens partikler, når den opvarmes fra -45 grade…
- Hvad består levende organismer af?
- Hvilke skridt skal du tage, når du udfører et eksperiment, der involverer uønskede eller ubehagel…
- Hvorfor opsøger investorer aktiesvindel?
- Hvordan fungerer gastermometeret?


