Måling af størrelsen af et atom:Forståelse af atomradius og kernedimensioner
Af Kevin Beck | Opdateret 24. marts 2022
Atomer er de mindste enheder af stof, der bevarer identiteten af et grundstof. Mens en mursten på et pund guld kan opdeles i stadig mindre fragmenter, er den ultimative bestanddel selve guldatomet – en enhed, der både er umådelig lille og bemærkelsesværdigt velforstået.
Hvad udgør et atom
Hvert atom indeholder mindst én proton i sin kerne; protontallet, eller atomnummeret, identificerer entydigt grundstoffet. I et neutralt atom er antallet af elektroner er lig med antallet af protoner, og de fleste grundstoffer indeholder også neutroner - neutrale partikler, der tilføjer masse uden at ændre ladningen. Varianter med forskellige neutrontal er kendt som isotoper .
Protoner og neutroner danner en kompakt kerne, mens elektroner optager omgivende orbitaler, der er mange gange længere fra kernen end selve kernen.
Krafter, der former atomstørrelse
atomradius er defineret som afstanden fra kernens centrum til den yderste elektronorbital. Denne radius bestemmes i høj grad af balancen mellem kerneladningen (som trækker elektroner indad) og elektron-elektron frastødningen, der skubber dem udad.
I løbet af en periode, når atomnummeret stiger, øger de tilføjede protoner den nukleare attraktion. Fordi elektroner tilføjes til den samme skal, krymper radius typisk, indtil en ædelgas nås. Når den næste periode begynder, introduceres en ny elektronskal, hvilket forårsager en pludselig stigning i radius, efterfulgt af et gradvist fald igen, efterhånden som perioden skrider frem.
Størrelse af atomkernen
I modsætning til den ydre radius er kernen ensartet lille – omkring 1×10⁻¹⁵m i diameter for alle elementer. I modsætning hertil ville den yderste elektron i et typisk atom ligge omkring 100 m fra kernen, hvis atomet blev forstørret til størrelsen af et fodboldstadion.
Estimering af atomradius
Selvom der ikke er nogen enkelt formel, der gælder for hvert atom, estimerer kemikere ofte kovalente radier ved at måle afstanden mellem kerner i et bundet molekyle og halvere denne værdi. For eksempel, hvis calcium har en kendt radius på 178 pm, og Ca-Se-bindingslængden i calciumselenid er 278 pm, kan selenradius tilnærmes til 100 pm.
Atomradius på tværs af det periodiske system
Følgende diagram (se IUPAC ) angiver omtrentlige radier for de første 86 grundstoffer, der spænder fra omkring 40 pm for brint til 240 pm for cæsium.
At forstå disse dimensioner hjælper videnskabsmænd med at forudsige kemisk adfærd, designe nye materialer og forklare stoffets fysiske egenskaber.
 Varme artikler
Varme artikler
-
 Forskere gør et betydeligt gennembrud på vej mod det nye superbug-dræbende antibiotikum teixobact…Methicillin-resistent Staphylococcus aureus . Kredit:NIH/NIAID Forskere, der arbejder på at udvikle et game-changing nyt antibiotikum, har gjort et betydeligt fremskridt i retning af at skabe ko
Forskere gør et betydeligt gennembrud på vej mod det nye superbug-dræbende antibiotikum teixobact…Methicillin-resistent Staphylococcus aureus . Kredit:NIH/NIAID Forskere, der arbejder på at udvikle et game-changing nyt antibiotikum, har gjort et betydeligt fremskridt i retning af at skabe ko -
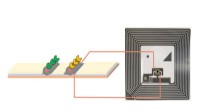 Kemikere udvikler en trådløs elektronisk lateral flow-analysetest til biosensingI denne laterale flowanalyse har papiret, der transporterer opløsningen (til venstre), kontrol- og testlinjer, der kan tilsluttes parallelt med det integrerede kredsløb af en RFID-enhed til trådløs de
Kemikere udvikler en trådløs elektronisk lateral flow-analysetest til biosensingI denne laterale flowanalyse har papiret, der transporterer opløsningen (til venstre), kontrol- og testlinjer, der kan tilsluttes parallelt med det integrerede kredsløb af en RFID-enhed til trådløs de -
 Team udvikler robust molekylær propel til ensrettede rotationerEt kig på hvordan propellen er sammensat og de ensrettede rotationer. Kredit:Saw-Wai Hla Et team af forskere fra Ohio University, Argonne National Laboratory, Universitié de Toulouse i Frankrig og
Team udvikler robust molekylær propel til ensrettede rotationerEt kig på hvordan propellen er sammensat og de ensrettede rotationer. Kredit:Saw-Wai Hla Et team af forskere fra Ohio University, Argonne National Laboratory, Universitié de Toulouse i Frankrig og -
 Polymerer går sammen om at levereEt TEM-billede af de opnåede nanokapsler. Kredit:The Royal Society of Chemistry En overkommelig, tungmetal- og lugtfri metode til fremstilling af hule polymer nanostrukturer er designet af A*STAR
Polymerer går sammen om at levereEt TEM-billede af de opnåede nanokapsler. Kredit:The Royal Society of Chemistry En overkommelig, tungmetal- og lugtfri metode til fremstilling af hule polymer nanostrukturer er designet af A*STAR
- NASA finder den tropiske storm Sergio på randen af orkanstatus
- Hvad skal skyttegrave og bjergkæder med ringen af brandpladetektonik?
- Bliver Windows Home Server det næste 'Me Too'-marked?
- Hvad er den øjeblikkelige hastighed på et objekt, der på det højeste punkt, da det kastede sig o…
- Nanokrystaller ikke små nok til at undgå defekter
- SLACs højhastighedselektronkamera filmer molekylær film i HD


