Mestring af molaritet:En trin-for-trin guide til beregning af mol pr. liter
Af bidragyder Opdateret 24. marts 2022
Forskere bruger molaritet til at angive mængden af et kemikalie (opløst stof) i et volumen opløsning. Typisk er de enheder, hvori molariteten rapporteres, mol pr. liter, og et "M" med stort bogstav bruges som symbol for ordene "mol pr. liter". En én molær opløsning af natriumchlorid (salt eller NaCl) omtales ofte som en 1,0 molær eller 1,0 M NaCl opløsning. Beregning af molariteten af en opløsning involverer således at bestemme, hvor mange mol af det opløste stof (f.eks. NaCl) der er til stede i en liter af opløsningen.
Beregning af mol
Beregning af mol
En muldvarp er Avagadros tal:6.022 * 10^23 enheder af hvad som helst. I tilfælde af molaritet af en opløsning, refererer 1 mol til 6,022 * 10^23 molekyler af en forbindelse såsom NaCl.
Det er en simpel sag at beregne antallet af mol af en forbindelse ud fra dens vægt. Dette gøres ved at veje forbindelsen og dividere vægten med grammolekylvægten (GMW) af forbindelsen. Du skal slå atomvægtene op for hvert grundstof i forbindelsen. Du kan finde grundstoffernes atomvægte på periodiske diagrammer over grundstofferne og i lærebøger og kemihåndbøger. For NaCl vil du tilføje atomvægten af natrium til den af chlor for at få GMW af NaCl. Da atomvægten af natrium er 22,99 g pr. mol, og den af chlor er 35,45 g pr. mol, er GMW af NaCl 58,44 g pr. mol.
For en forbindelse som natriumsulfat (Na2SO4, skal du fordoble atomvægten af natrium (Na) og firdoble atomvægten af oxygen (O) og tilføje dem til atomvægten af svovl (S), da der er to natriumatomer og fire oxygenatomer i hvert natriumsulfatmolekyle.
Du kan beregne antallet af mol af din forbindelse ved at dividere antallet af gram af forbindelsen med GMW af forbindelsen. Hvis du har 100 g NaCl, vil du beregne antallet af mol ved at dividere de 100 g med den beregnede GMW på 58,44 g pr. mol for at få 1,71 mol NaCl.
Beregning af molaritet
Beregning af molaritet
Nu hvor du ved, hvor mange mol opløst stof du har, kan du tilføje forbindelsen til dit opløsningsmiddel for at lave en opløsning. Mål derefter opløsningens volumen. Divider nu antallet af mol af det opløste stof med volumenet af den resulterende opløsning (i liter) for at finde molariteten.
I ovenstående eksempel, hvis du opløste de 100 g (1,71 mol) NaCl i vand nok til at lave 1 liter opløsning, ville du have en 1,71 M NaCl-opløsning. Hvis du opløste de 1,71 mol NaCl i vand nok til at lave en 1,71 liter opløsning, ville du have en 1,0 M opløsning.
 Varme artikler
Varme artikler
-
 Accelerering af kobberkorrosion på en øre:En videnskabelig trin-for-trin-vejledningAf Irene A. Blake, Opdateret Aug302022 En øre ruster ikke rigtigt. Den tynde kobberbelægning på mønten oxiderer gradvist og danner en grønlig patina. Denne oxidation opstår, når kobber reagerer med i
Accelerering af kobberkorrosion på en øre:En videnskabelig trin-for-trin-vejledningAf Irene A. Blake, Opdateret Aug302022 En øre ruster ikke rigtigt. Den tynde kobberbelægning på mønten oxiderer gradvist og danner en grønlig patina. Denne oxidation opstår, når kobber reagerer med i -
 Nyt kunstigt enzym nedbryder sejt, træagtigt lignin:Undersøgelse viser løfte om at udvikle en ny …Woody lignin, set her i renset form, har et betydeligt løfte som et vedvarende biobrændstof, hvis det effektivt kan nedbrydes til nyttig form. Kredit:Andrea Starr | Pacific Northwest National Laborato
Nyt kunstigt enzym nedbryder sejt, træagtigt lignin:Undersøgelse viser løfte om at udvikle en ny …Woody lignin, set her i renset form, har et betydeligt løfte som et vedvarende biobrændstof, hvis det effektivt kan nedbrydes til nyttig form. Kredit:Andrea Starr | Pacific Northwest National Laborato -
 Hvordan nye materialer øger effektiviteten af direkte ethanolbrændselscellerMaterialet består af Nafion med indlejrede nanopartikler. Kredit:B.Matos/IPEN Ethanol har fem gange højere volumetrisk energitæthed (6,7 kWh/L) end brint (1,3 kWh/L) og kan sikkert bruges i brænds
Hvordan nye materialer øger effektiviteten af direkte ethanolbrændselscellerMaterialet består af Nafion med indlejrede nanopartikler. Kredit:B.Matos/IPEN Ethanol har fem gange højere volumetrisk energitæthed (6,7 kWh/L) end brint (1,3 kWh/L) og kan sikkert bruges i brænds -
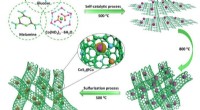 S, N co-doteret carbon nanorør-indkapslet CoS2@CoSkematisk illustration og fysisk karakterisering af S, N co-dopede kulstof nanorør indkapslede kerne-skal (CoS2@Co) nanopartikler. Kredit:©Science China Press Elektrokemisk vandopdeling er en guns
S, N co-doteret carbon nanorør-indkapslet CoS2@CoSkematisk illustration og fysisk karakterisering af S, N co-dopede kulstof nanorør indkapslede kerne-skal (CoS2@Co) nanopartikler. Kredit:©Science China Press Elektrokemisk vandopdeling er en guns


