Nøglefaktorer, der påvirker osmolariteten af en opløsning
Af John Brennan Opdateret 24. marts 2022
Når en ionforbindelse opløses, adskilles den i sine bestanddele. Hver af disse ioner bliver omgivet af opløsningsmiddelmolekyler, en proces kaldet solvatisering. En ionforbindelse bidrager derfor med flere partikler til en opløsning end en molekylær forbindelse, som ikke dissocierer på denne måde. Osmolaritet er nyttig til at bestemme osmotisk tryk.
Molaritet vs. osmolaritet
Molaritet vs. osmolaritet
Kemikere beskriver normalt koncentration i form af molaritet, hvor et mol er 6,022 x 10^23 partikler, ioner eller molekyler, og en én molær opløsning har et mol opløst stof pr. liter opløsning. En en molær opløsning af NaCl ville indeholde et mol NaCl formelenheder. Da NaCl'et opløses i Na+ og Cl-ioner i vandet, indeholder opløsningen reelt to mol ioner:et mol Na+ ioner og et mol Cl-ioner. For at skelne denne måling fra molaritet, refererer kemikere til det som osmolaritet; en én molær opløsning af salt er to osmolær i form af ionkoncentration.
Faktorer
Faktorer
Den vigtigste faktor til bestemmelse af osmolaritet er opløsningens molaritet - jo flere mol opløst stof, jo flere osmoler af ioner er til stede. En anden vigtig faktor er imidlertid antallet af ioner, som forbindelsen dissocierer i. NaCl dissocierer i to ioner, men calciumchlorid (CaCl2) dissocierer i tre:en calciumion og to chloridioner. Følgelig vil en opløsning af calciumchlorid, alt andet lige, have en højere osmolaritet end en opløsning af natriumchlorid.
Afvigelse fra idealitet
Afvigelse fra idealitet
Den tredje og sidste faktor, der påvirker osmolariteten, er afvigelsen fra idealitet. I teorien burde alle ioniske forbindelser dissociere fuldstændigt. I virkeligheden forbliver lidt af forbindelsen dog udissocieret. Det meste natriumchlorid spaltes til natrium- og chloridioner i vand, men en lille del forbliver bundet sammen som NaCl. Mængden af udissocieret forbindelse stiger, når koncentrationen af forbindelsen stiger, så denne faktor kan blive et mere signifikant problem ved højere koncentrationer. For lave koncentrationer af opløst stof er afvigelsen fra idealitet ubetydelig.
Betydning
Betydning
Osmolaritet er vigtig, fordi den bestemmer osmotisk tryk. Hvis en opløsning er adskilt fra en anden opløsning af forskellig koncentration af en semipermeabel membran, og hvis den semipermeable membran vil tillade vandmolekyler, men ikke ioner at passere gennem den, vil vandet diffundere gennem membranen i retning af stigende koncentration. Denne proces kaldes osmose. Membranerne af celler i din krop fungerer som semipermeable membraner, fordi vand kan krydse dem, men ioner kan ikke. Det er derfor, læger bruger saltvandsopløsning til IV-infusion og ikke rent vand; hvis de brugte rent vand, ville osmolariteten af dit blod falde, hvilket får celler som røde blodlegemer til at optage vand og briste.
Referencer
- "Kemiske principper:Søgen efter indsigt"; Peter Atkins, et al.; 2008
- Osmoseenheden:Osmolalitet
- "Biologi"; Neil A. Campbell, et al.; 2008
 Varme artikler
Varme artikler
-
 Ny undersøgelse præsenterer højaktive ozygenerede grupper i kulstofmaterialer til oxygenreduktion…Figur 1. Ydeevnekarakteriseringerne af ORHP. Kredit:Professor Jong-Beom Baek, UNIST Hydrogenperoxid (H 2 O 2 ) har fundet mange anvendelser i den moderne industri, herunder at fungere som en g
Ny undersøgelse præsenterer højaktive ozygenerede grupper i kulstofmaterialer til oxygenreduktion…Figur 1. Ydeevnekarakteriseringerne af ORHP. Kredit:Professor Jong-Beom Baek, UNIST Hydrogenperoxid (H 2 O 2 ) har fundet mange anvendelser i den moderne industri, herunder at fungere som en g -
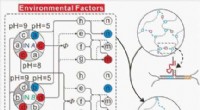 Ændring af blødt stofs form ved hjælp af logiske kredsløb lavet af DNAKredit: Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202102169 De utallige processer, der foregår i biologiske celler, kan ved første øjekast virke utroligt komplekse. Og stad
Ændring af blødt stofs form ved hjælp af logiske kredsløb lavet af DNAKredit: Angewandte Chemie International Edition (2021). DOI:10.1002/anie.202102169 De utallige processer, der foregår i biologiske celler, kan ved første øjekast virke utroligt komplekse. Og stad -
 Forskere udvikler metode, der kan producere stærkere, mere bøjelige metallerKredit:Brigham Young University Det er måske ikke så iørefaldende som kæder og svage led, men fysikere og ingeniører ved et materiale er kun så stærkt som dets svageste korngrænse. OKAY, det er s
Forskere udvikler metode, der kan producere stærkere, mere bøjelige metallerKredit:Brigham Young University Det er måske ikke så iørefaldende som kæder og svage led, men fysikere og ingeniører ved et materiale er kun så stærkt som dets svageste korngrænse. OKAY, det er s -
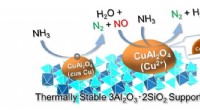 Ny katalysator gør ammoniak til et innovativt rent brændstofCuOx/3A2S producerer selektivt N 2 og H 2 O fra NH 3 gennem en to-trins reaktion. Kredit:Dr. Satoshi Hinokuma At træffe foranstaltninger mod klimaændringer og konvertere til samfund, der bru
Ny katalysator gør ammoniak til et innovativt rent brændstofCuOx/3A2S producerer selektivt N 2 og H 2 O fra NH 3 gennem en to-trins reaktion. Kredit:Dr. Satoshi Hinokuma At træffe foranstaltninger mod klimaændringer og konvertere til samfund, der bru
- Kolde støvkerner i den centrale zone af Mælkevejen
- Hvad er varmetab for en motor, der har input Energy 10750 Joules og fungerer 2420?
- Forskere kortlægger symbiotiske forhold mellem træer og mikrober verden over
- Hvad er syrefældningen et middel for?
- Hvorfor kan et elevatorkabel bryde under acceleration, når man løfter en lettere belastning, end d…
- Hvor eller under hvilke indstillinger ville en metamorfe klippe sandsynligvis danne?


