Hvorfor simpel destillation ikke altid er nok:Nøglebegrænsninger og alternativer
Af John Brennan
Opdateret 24. marts 2022
Ved simpel destillation opvarmes en blanding af væsker til den temperatur, hvor en komponent koger. Den resulterende damp opsamles og genkondenseres til væske. Selvom de er hurtige og ligetil, kan mange blandinger ikke adskilles på denne måde og kræver mere avancerede teknikker.
Renheder
Fordi blandingen kun koges og genkondenseres én gang, afspejler slutproduktet dampens sammensætning. Når komponentens kogepunkter er tæt på, kan destillatet indeholde betydelige urenheder. I praksis er simpel destillation kun effektiv, når kogepunktsforskellen er mindst 25°C. Blandinger med tættere kogepunkter håndteres bedre ved fraktioneret destillation.
Azeotropiske blandinger
Nogle flydende blandinger danner azeotroper - sammensætninger, der koger ved en konstant temperatur og bevarer den samme dampsammensætning som væsken. Et klassisk eksempel er 95,6 % ethanol med 4,4 % vand, som koger ved en lavere temperatur end de rene komponenter. Simpel destillation kan ikke bryde en azeotrop; heller ikke fraktioneret destillation. Andre metoder, såsom azeotrop eller ekstraktiv destillation, er typisk påkrævet.
Energiforbrug
Opvarmning af en væske eller blanding til dets kogepunkt kræver betydelig energi. Når det drives af fossile brændstoffer, øger dette kulstofemissioner og driftsomkostninger. For eksempel kræver destillering af ethanol i industriel skala store mængder brændstof. Laboratorieopsætninger bruger ofte en rotationsfordamper (rotovap), der anvender vakuum for at sænke kogepunktet, men denne fremgangsmåde er mindre praktisk til bulkproduktion.
Kemiske reaktioner
Forhøjede temperaturer kan udløse uønskede reaktioner og ændre det ønskede produkt. For eksempel kan opvarmning af en blanding af hydrogenbromid og butadien flytte forholdet mellem 3-brom-1-buten og 1-brom-2-buten. Varmefølsomme forbindelser, såsom nitroglycerin, udgør sikkerhedsrisici, hvis de udsættes for kogende temperaturer. Derfor skal blandingens termiske stabilitet overvejes, før du vælger simpel destillation.
 Varme artikler
Varme artikler
-
 Nuklear engineering forskere udvikler ny elastisk oxiddispersion styrket legeringKredit:Pixabay/CC0 Public Domain Forskere fra Texas A&M University har for nylig vist overlegen ydeevne af en ny oxiddispersion-forstærket (ODS) legering, de udviklede til brug i både fissions- og
Nuklear engineering forskere udvikler ny elastisk oxiddispersion styrket legeringKredit:Pixabay/CC0 Public Domain Forskere fra Texas A&M University har for nylig vist overlegen ydeevne af en ny oxiddispersion-forstærket (ODS) legering, de udviklede til brug i både fissions- og -
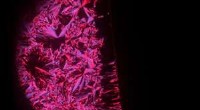 At bryde symmetri fører til responsive organiske fotodetektorerEt polariseret optisk mikroskopibillede af de søjleformede flydende krystaller klemt mellem to krydsede polarisatorer med (højre) og uden (venstre) et elektrisk felt. Dette tyder på, at anvendelse af
At bryde symmetri fører til responsive organiske fotodetektorerEt polariseret optisk mikroskopibillede af de søjleformede flydende krystaller klemt mellem to krydsede polarisatorer med (højre) og uden (venstre) et elektrisk felt. Dette tyder på, at anvendelse af -
 Frosset kobber opfører sig som ædelmetal i katalyse:undersøgelseUnik elektronkonfiguration af det 29. element Cu blev exciteret af højenergiplasma, resulterer i variation af dens kemiske egenskaber. Kredit:SUN Jian og YU Jiafeng Som et ikke-ædelt metal, kobber
Frosset kobber opfører sig som ædelmetal i katalyse:undersøgelseUnik elektronkonfiguration af det 29. element Cu blev exciteret af højenergiplasma, resulterer i variation af dens kemiske egenskaber. Kredit:SUN Jian og YU Jiafeng Som et ikke-ædelt metal, kobber -
 Ny krystalteknisk strategi til at designe ultralyse fluorescerende faste farvestofferNår det kommer til at designe ultralyse solid-state fluorescerende materialer, kan brobyggede krystaldesign være nøglen til at muliggøre monomer emission og få adgang til nye krystallinske systemer, a
Ny krystalteknisk strategi til at designe ultralyse fluorescerende faste farvestofferNår det kommer til at designe ultralyse solid-state fluorescerende materialer, kan brobyggede krystaldesign være nøglen til at muliggøre monomer emission og få adgang til nye krystallinske systemer, a
- Hvordan kunne du øge lufttrykket inde i en taske indeholdende gruppe af molekyler?
- Hvad er der galt, hvis der overhovedet ingen elektricitet i hele Geo Tracker?
- Eksperimentelt hjernestyret høreapparat afkoder, identificerer, hvem du vil høre
- Hvad er den kraft, der skubber?
- Sådan beregnes en T-Statistic
- Hvordan kan tyngdekraften bevæge store mængder sten og jord?


