Nanopartikler leverer et-to terapeutiske slag for at dræbe tumorceller
Standardtilgangen til kræftbehandling i dag er at blande og matche kemoterapimedicin for at angribe tumorer på flere måder. Nu, to separate teams af efterforskere har vist, at brug af nanopartikler til at levere flere lægemidler samtidigt kan producere en synergistisk effekt, der øger celledræbende evne af begge lægemidler.
I en undersøgelse, et hold af efterforskere ved Northwestern University har vist, at de kan kombinere to kraftige, men ekstremt giftige anticancermidler - cisplatin og doxorubicin - i en polymer nanopartikel, producerer et væsentligt løft i kombinationens evne til at ødelægge tumorer. Ud over, to-i-en nanopartikel reducerer mængden af begge lægemidler, der er nødvendige for at dræbe kræftceller, hvilket formentlig ville reducere de toksiske bivirkninger forbundet med disse lægemidler.
SonBinh Nguyen og Thomas O'Halloran ledede denne undersøgelse, som blev offentliggjort i Journal of the American Chemical Society . Dr. O'Halloran er co-principal investigator i et af 12 Cancer Nanotechnology Platform Partnerships finansieret af National Cancer Institute Alliance for Nanotechnology in Cancer. Han er også medlem af Northwestern University Center for Cancer Nanotechnology Excellence (CCNE), som også er en del af Alliance for Nanotechnology in Cancer.
Selvom det oprindeligt er designet til at transportere arsentrioxid til solide tumorer, de nanopartikler, der bruges i denne undersøgelse, viser sig at være ret alsidige i deres evne til at transportere en bred vifte af laster til maligniteter. I dette studie, efterforskerne ønskede at se, om levering af to lægemidler i en nanopartikel gav nogen fordele ved at levere dem uden nanopartikler eller i separate nanopartikler. Nanopartiklerne, som forskerne kalder nanobiner, fremstilles ved at indkapsle et liposom inde i et pH-responsivt polymerbur. I dette tilfælde, doxorubicin er fanget i liposomets kerne, mens cisplatin var fanget i polymerburet.
I et indledende sæt af eksperimenter, efterforskerne fastslog, at et forhold på 5 til 1 mellem cisplatin og doxorubicin var det mest effektive til behandling af ovarietumorer, når de to lægemidler blev kombineret i den samme nanopartikel. Når de to lægemidler blev administreret i dette forhold, men med hver sin nanopartikel, kombinationen var ikke kun mindre effektiv til at dræbe maligne celler, men de to stoffer så ud til at forstyrre hinanden, et fænomen, der ofte observeres i klinisk praksis. Administration af de to lægemidler i den samme nanopartikel sikrer, at lægemidlerne rammer deres intracellulære mål på samme tid, hvilket er det, der sandsynligvis fører til den synergisme, der er observeret i denne undersøgelse.
I mellemtiden Mansoor Amiji og Zhenfeng Duan, co-principal researchers of the Cancer Nanotechnology Platform Partnership ved Northeastern University, har vist, at en anden type polymer nanopartikel også kan levere to anticancermidler samtidigt og som et resultat kan dræbe kræftceller, der er blevet resistente over for lægemiddelbehandling. I dette tilfælde, forskerne syntetiserede biokompatible polymer-nanopartikler, der fangede paclitaxel og lonidamin, og som var rettet mod epidermal vækstfaktor-receptor (EGFR), der er overudtrykt på meget aggressive tumorer. Når det tilsættes til tumorceller, der vokser i kultur, nanopartiklerne, der indeholdt begge lægemidler, var langt mere effektiv til at dræbe de lægemiddelresistente celler, end når de to lægemidler blev administreret sammen i separate nanopartikler. Efterforskerne rapporterede deres resultater i journalen Molekylær Farmaceutik .
I et separat sæt eksperimenter, hvis resultater blev offentliggjort i tidsskriftet Angewandte Chemie International Edition , Drs. Nguyen og O'Halloran, sammen med Thomas Meade, et andet medlem af det nordvestlige CCNE, demonstreret, at nanobiner også kan co-levere et terapeutisk og magnetisk resonansbilleddannende middel til tumorer. I dette studie, forskerne fyldte anticancermidlet gemcitabin i nanobinets kerne og tilføjede et gadolinium magnetisk resonanskontrastmiddel til nanobinets overflade. Når det tilføjes til musetumorceller, nanobinerne blev optaget hurtigt, og nanobinerne var tydeligt synlige i magnetiske resonansbilleder. Ud over, nanopartiklerne frigav deres gemcitabin-nyttelast, når nanobinerne blev optaget af de dyrkede celler.
 Varme artikler
Varme artikler
-
 Grafen afslører sin magnetiske personlighed(PhysOrg.com) -- Kan organisk materiale opføre sig som en køleskabsmagnet? Forskere fra University of Manchester har nu vist, at det kan det. I en rapport offentliggjort i Naturfysik , de brugte gr
Grafen afslører sin magnetiske personlighed(PhysOrg.com) -- Kan organisk materiale opføre sig som en køleskabsmagnet? Forskere fra University of Manchester har nu vist, at det kan det. I en rapport offentliggjort i Naturfysik , de brugte gr -
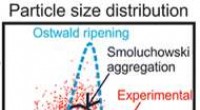 At se nanopartikler vokseSom vist her, Smoluchowski-modellen fanger kvantitativt den gennemsnitlige væksthastighed og partikelstørrelsesfordeling af en sølvnanopartikel, mens Ostwald-modning ikke gør det. Ved at overveje kine
At se nanopartikler vokseSom vist her, Smoluchowski-modellen fanger kvantitativt den gennemsnitlige væksthastighed og partikelstørrelsesfordeling af en sølvnanopartikel, mens Ostwald-modning ikke gør det. Ved at overveje kine -
 Ny teknik tillader nanobiopsier af levende celler(Phys.org) – Forskere ved UC Santa Cruz har udviklet et robot-nanobiopsi-system, der kan udtrække bittesmå prøver inde fra en levende celle uden at dræbe den. Enkeltcellet nanobiopsi-teknikken er et k
Ny teknik tillader nanobiopsier af levende celler(Phys.org) – Forskere ved UC Santa Cruz har udviklet et robot-nanobiopsi-system, der kan udtrække bittesmå prøver inde fra en levende celle uden at dræbe den. Enkeltcellet nanobiopsi-teknikken er et k -
 Teoretikere finder mekanisme bag næsten rene nanorør fra den usædvanlige katalysatorForskere fra Rice University har afkodet den usædvanlige vækst, der er karakteristisk for carbon nanorør, der starter som en kiralitet, men skifter til en anden, hvilket resulterer i næsten homogene p
Teoretikere finder mekanisme bag næsten rene nanorør fra den usædvanlige katalysatorForskere fra Rice University har afkodet den usædvanlige vækst, der er karakteristisk for carbon nanorør, der starter som en kiralitet, men skifter til en anden, hvilket resulterer i næsten homogene p
- 2019 teknologiske gaver:Lidt for enhver smag
- Forskere producerer radioaktivitetsfri Tjernobyl-vodka
- Forskeren foreslår en ny mekanisme til at stoppe tsunamier i deres spor
- Tidtagningsteori kombinerer kvanteure og Einsteins relativitetsteori
- Hvad er et carbonhydridkæde forhold til fedtstoffer i biologi?
- Manglende vindvariation betyder, at fremtidige virkninger af klimaændringer kan blive undervurderet…


