FDA skitserer politik for overvågning af nanoteknologi
Føderale tilsynsmyndigheder vil høre fra virksomheder, der bruger små, konstruerede mikropartikler i deres produkter, del af bestræbelserne på at holde sig ajour med det voksende område inden for nanoteknologi.
Food and Drug Administration udsendte tirsdag de sidste anbefalinger til virksomheder, der bruger nanoteknologi i produkter reguleret af regeringen, som kan omfatte medicinsk behandling, mad og kosmetik. FDA -tilsynsmyndigheder vil have virksomheder til at rådføre sig med dem, inden de lancerer nanoteknologiske produkter, selvom beslutningen om at gå på markedet i det væsentlige vil ligge hos producenterne.
FDA foretager ikke en vurdering af den overordnede sikkerhed ved nanoteknologi eller definerer endda udtrykket.
"Vi tager en forsigtig videnskabelig tilgang til at vurdere hvert produkt på sine egne meritter og gør ikke bredt, generelle antagelser om sikkerheden ved nanoteknologiske produkter, "sagde FDA -kommissær Margaret Hamburg, i en erklæring.
Branchegrupper definerer generelt nanopartikler som dem, der er mindre end 100 nanometer brede. Et nanometer er en milliarddel af en meter. Et menneskehår, for eksempel, er 80, 000 nanometer tyk, mens et ark papir er 100, 000 nanometer.
Disse submikroskopiske partikler har i stigende grad vist sig i FDA-regulerede produkter, herunder emballage til fødevarer, solcreme, hudcreme og blændreducerende brillebelægninger. Teknologien har også potentielle anvendelser inden for medicin, selvom de nye FDA -dokumenter fokuserer specifikt på mad og kosmetik.
Retningslinjerne for fødevareproducenter foreslår, at ændringer i fremstillingen, der involverer nanopartikler, kan kræve indsendelse af yderligere data for at vise, at ændringerne ikke påvirker fødevarens sikkerhed eller identitet. Under mangeårige regler, fødevarevirksomheder er ikke forpligtet til at søge myndighedsgodkendelse for produkter, der indeholder etablerede ingredienser og materialer, såsom koffein, krydderier og forskellige konserveringsmidler.
Men FDA siger, at "på dette tidspunkt, vi er ikke bekendt med fødevarestoffer, der bevidst er konstrueret på nanometerskalaen ", der ville kvalificere sig til den kategori af" generelt anerkendte som sikre "tilsætningsstoffer.
Fødevarevirksomheder undersøger belægninger af nanopartikler som en form for konservering og som en måde at potentielt reducere bakteriekontaminering i visse fødevarer.
I et separat vejledningsdokument, FDA lagde forslag til brug af nanoteknologi i kosmetik, en almindelig praksis i kosmetikindustrien siden 1990'erne. Nanopartikler bruges i hudfugtighedscreme, mineralsk makeup og anden kosmetik.
Vejledningen opfordrer producenterne til at rådføre sig med FDA, før de tester sikkerheden for nanopartikler, der bruges i kosmetik, bemærker, at traditionelle testmetoder ikke må opfange ændringer, der er produceret ved at tilføje nanoteknologi.
FDA har generelt mindre autoritet over kosmetik end fødevareingredienser. FDA gennemgår typisk ikke kosmetik, før de lanceres, og virksomheder er ansvarlige for at sikre deres produkters sikkerhed.
© 2014 Associated Press. Alle rettigheder forbeholdes.
 Varme artikler
Varme artikler
-
 Nanorørteknologi, der fører til hurtige, billigere medicinsk diagnostikNanorør sensor (PhysOrg.com) - Forskere ved Oregon State University har udnyttet den ekstraordinære kraft af kulstof nanorør for at øge hastigheden af biologiske sensorer, en teknologi, der muli
Nanorørteknologi, der fører til hurtige, billigere medicinsk diagnostikNanorør sensor (PhysOrg.com) - Forskere ved Oregon State University har udnyttet den ekstraordinære kraft af kulstof nanorør for at øge hastigheden af biologiske sensorer, en teknologi, der muli -
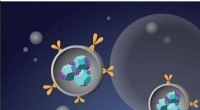 Forskningstrio skitserer måder, hvorpå nanodiamanter bliver brugt til at behandle kræftEt skema over målrettet lægemiddellevering mod brystkræft er vist. Nanodiamanter er indkapslet i liposomer, der er funktionaliserede med målrettede antistoffer. Kredit:Dr. Laura Moore (Prof. Dean Ho G
Forskningstrio skitserer måder, hvorpå nanodiamanter bliver brugt til at behandle kræftEt skema over målrettet lægemiddellevering mod brystkræft er vist. Nanodiamanter er indkapslet i liposomer, der er funktionaliserede med målrettede antistoffer. Kredit:Dr. Laura Moore (Prof. Dean Ho G -
 Forskere udvikler innovative hybridmaterialer ud fra plast og grafenGrafit (nederst til venstre) består af talrige lag af kulstofstoffet grafen (øverst til venstre). Grafenmakromolekylerne udviklet i Freiburg er mindre end en milliontedel millimeter tykke, men dækker
Forskere udvikler innovative hybridmaterialer ud fra plast og grafenGrafit (nederst til venstre) består af talrige lag af kulstofstoffet grafen (øverst til venstre). Grafenmakromolekylerne udviklet i Freiburg er mindre end en milliontedel millimeter tykke, men dækker -
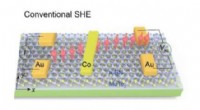 Udtynding af Weyl-halvmetaller giver et nyt twist til spintronicsSkematisk, der viser (venstre) konventionel spin Hall-effekt (SHE), hvor ladestrømmen langs y-aksen genererer en spin-strøm langs x-aksen (med spin-polarisering angivet af den røde kugle med pil). (Hø
Udtynding af Weyl-halvmetaller giver et nyt twist til spintronicsSkematisk, der viser (venstre) konventionel spin Hall-effekt (SHE), hvor ladestrømmen langs y-aksen genererer en spin-strøm langs x-aksen (med spin-polarisering angivet af den røde kugle med pil). (Hø
- Grafen og relaterede materialers sikkerhed:Menneskets sundhed og miljøet
- Fysikere løser et beta-forfalds-puslespil med avancerede nukleare modeller
- Ujævne havniveaustigninger bundet til klimaændringer
- Forskere opretter enkeltkrystal perovskit solceller
- Registrering af giftig PFAS med en sensor i chipstørrelse
- Undervandsrobotter hjælper med at forudsige, hvordan og hvornår ishylderne falder sammen


