Kemikere lukker hullet i at gøre nanomedicin sikrere, mere effektivt

Fra venstre:Drs. Xingya Jiang, Jie Zheng og Bujie Du forsker i nanopartiklers adfærd i kroppen på Natural Science and Engineering Research Laboratory på UT Dallas campus. Forskerne offentliggjorde en ny undersøgelse, der beskriver, hvordan en af leverens naturlige toksinfjernelsesprocesser kan forbedre leveringen af nanomedicin. Kredit:University of Texas i Dallas
Dr. Jie Zheng mener, at han har forvandlet en barriere til en bro, når det kommer til implementering af nanomedicin.
Professoren i kemi og hans forskerhold ved University of Texas i Dallas har påvist, at nanomedicin kan designes til at interagere med en naturlig afgiftningsproces i leveren for at forbedre deres sygdomsmålretning og samtidig minimere potentielle bivirkninger.
Deres studie, udgivet 15. juli i Natur nanoteknologi , angiver en vej til at gøre nanomedicin sikrere og mere effektiv.
"Folk har arbejdet på nanomedicin i årtier. Det har et stort potentiale til at fremme kræftbehandling og detektion, " sagde Zheng, Cecil H. og Ida Green professor i systembiologi ved Institut for Kemi og Biokemi ved UT Dallas. "Men der er også potentielle farer."
Nanomedicin refererer bredt til brugen af konstruerede nanopartikler, defineret ved deres mikroskopiske dimensioner, til forskellige sundhedsmæssige formål. Primær blandt disse roller er den præcise levering af lægemidler og påvisning af forskellige sygdomme.
leveren, det største afgiftningsorgan i kroppen, opfanger og fjerner mange stoffer, der stammer både i og uden for kroppen.
"Leveren beskytter os hver dag mod skader fra fremmede materialer, " sagde Zheng. "Men det er også en langvarig barriere for at lave sikker og effektiv nanomedicin, som patienter kan bruge."
Selvom mange nanomedicin målrette sygdom effektivt i prækliniske undersøgelser, Zheng sagde, at få af dem når klinisk brug. Dette er fordi, i leveren, makrofager - en type hvide blodlegemer - fanger og opbevarer dem i kroppen på lang sigt, reducere deres effektivitet og øge deres toksicitet.
"Udfordringen er at maksimere deres behandlingspotentiale og samtidig minimere bivirkninger, " sagde han. "Kun når du løser begge problemer, kan du virkelig bringe dette til klinikken."
Forskernes vigtigste opdagelse, udført i en musemodel, er, at en af leverens naturlige toksinfjernelsesprocesser kan bruges til at forbedre leveringen af nanomedicin og samtidig gøre dem sikre. Denne proces - glutathion-medieret biotransformation - eliminerer de off-target nanomedicin, så de ikke fortsætter med at skade kroppen.
"Vi bruger denne leverbiotransformation som en måde at modificere de cirkulerende nanomedicin, så makrofagoptagelsen vil blive reduceret, " sagde Dr. Xingya Jiang, hovedforfatteren af undersøgelsen. "Med denne leverbiotransformation, de nanomedicin, der savner målet, kan effektivt rydde ud uden langvarig ophobning i kroppen."
Denne biotransformation var tidligere kendt for at eliminere fedtmolekyler og små toksiner, såsom tungmetaller. Men dets interaktion med nanomedicin var uklart før denne undersøgelse.
"Leverceller udskiller konstant glutathion til sinusoiden, som er kapillæren i leveren. Denne glutathionudskillelse, kaldet efflux, kan omdanne nanopartiklers overfladekemi, så kroppen lettere kan fjerne dem, " sagde Zheng.
"Sammen med andre fysiologiske processer, denne efflux kan præcist kontrollere transporten af nanomedicin i kroppen, forbedre deres målretning mod tumoren og reducere deres uspecifikke ophobning i sundt væv i mellemtiden, " han sagde.
Sammen med Dr. Bujie Du, Zheng og Jiang designede en nanosonde, der bruger organisk farvestof til at rapportere, hvordan biotransformationen ændrer nanopartiklerne og for bedre at forstå både dens målretning og clearance.
Når nanosonden blev leveret ind i leveren, fluorescensen af farvestoffet blev hurtigt aktiveret, hvilket indikerer, at farvestoffet var adskilt fra nanopartiklerne i leveren.
"Det var ikke sikkert, før hvad der skete, da nanosonden kom ind i leveren, " sagde Jiang. "Vi antog, at der var en eller anden interaktion i leveren, der forårsagede dissociationen, men vi vidste det ikke rigtigt. Nu har vi set, hvordan det fungerer."
Holdet validerede, hvad der sker i leveren ved at bruge nanopartikler af en præcis størrelse og veldefineret struktur; I dette tilfælde, partiklerne indeholdt hver 25 guldatomer og fire farvestofmolekyler. At vide præcis, hvordan disse nanopartikler var struktureret, da de kom ind i kroppen, tillod nøjagtig fortolkning af, hvordan de adskilte sig, når de ryddede ud af kroppen.
"Som vi overvågede det, vi så, at tumormålretning af nanomedicin steg markant sammenlignet med kontroller, mens de resterende nanomedicin i normalt væv blev minimeret, " sagde Zheng. "På grund af dette atomisk præcise design, vi var også i stand til at opdage, at aminosyren cystein også er involveret i denne biotransformationsproces, hjælper med at modificere disse nanopartikler in vivo."
Zheng understregede, at denne forskning viser en ny vej til at designe nanomedicin ved at drage fordel af kroppens naturlige reaktioner.
"De fleste mennesker tænker på leveroptagelse som en barriere for levering af nanomedicin - at leveren vil tage dem op og holde dem i kroppen i lang tid. Dette er en ny strategi, " sagde han. "Vi har gjort den leveradfærd, som vi engang betragtede som en ulempe ved klinisk oversættelse af nanomedicin, til en fordel.
"Mere end blot at levere en ny strategi, Vi håber, at dette inspirerer os til at være kreative tænkere, så mange barrierer i vores forskning kan blive broer til større videnskabelige opdagelser."
Sidste artikelMolekylær kaos ved rod til batterinedbrud
Næste artikelMikrorobotter viser løfte om behandling af tumorer
 Varme artikler
Varme artikler
-
 Professor arbejder på at udvikle strømkilder til fleksible, strækbar elektronikDette billede viser en fuldt strækbar superkapacitor sammensat af carbon nanorør makrofilm, en polyurethan -membranseparator og organiske elektrolytter. (Phys.org) - Elektroniske enheder bliver mi
Professor arbejder på at udvikle strømkilder til fleksible, strækbar elektronikDette billede viser en fuldt strækbar superkapacitor sammensat af carbon nanorør makrofilm, en polyurethan -membranseparator og organiske elektrolytter. (Phys.org) - Elektroniske enheder bliver mi -
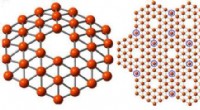 Grafenlignende materiale lavet af bor en mulighed, forsøg tyder påDette viser en 36-atom klynge af bor, venstre, arrangeret som en flad skive med et sekskantet hul i midten, passer til de teoretiske krav til fremstilling af et atom-tykt borark, ret, et teoretisk nan
Grafenlignende materiale lavet af bor en mulighed, forsøg tyder påDette viser en 36-atom klynge af bor, venstre, arrangeret som en flad skive med et sekskantet hul i midten, passer til de teoretiske krav til fremstilling af et atom-tykt borark, ret, et teoretisk nan -
 Fremtidens gnistre for diamantbaseret kvanteteknologiEn kunstners indtryk af en diamantbyggesten i et fremtidigt fotonisk kredsløb. Den røde farve understreger de ledige germaniumcentre, der udsender i det røde spektralområde, og ringen illustrerer hulr
Fremtidens gnistre for diamantbaseret kvanteteknologiEn kunstners indtryk af en diamantbyggesten i et fremtidigt fotonisk kredsløb. Den røde farve understreger de ledige germaniumcentre, der udsender i det røde spektralområde, og ringen illustrerer hulr -
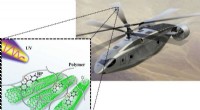 Ingeniører udvikler teknik til at lave adaptive materialerHærens forskere forestiller sig et rotorfartøjskoncept, som repræsenterer reaktive forstærkninger, der ved eksponering for ultraviolet lys vil øge den mekaniske adfærd efter behov. Ingeniørerne sagde,
Ingeniører udvikler teknik til at lave adaptive materialerHærens forskere forestiller sig et rotorfartøjskoncept, som repræsenterer reaktive forstærkninger, der ved eksponering for ultraviolet lys vil øge den mekaniske adfærd efter behov. Ingeniørerne sagde,
- Sådan bukker du fladt glas perfekt rundt om hjørner
- Illinois sportsfisk genopretning et resultat af 1972 Clean Water Act, videnskabsmænd rapporterer
- Forskere udvikler en ny metode til at reducere kvantestøj
- Forskelle mellem roterende og reciprocerende kompressorer
- Los Angeles og Google samarbejder om Tree Canopy-projektet
- Organisk ternær datalagringsenhed udviklet


