Yderligere detaljer afsløret om et meget effektivt anticancer-lægemiddelleveringssystem
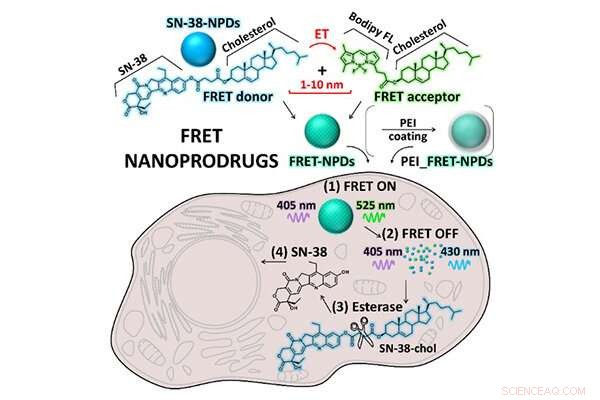
Intracellulær undersøgelse af FRET NPD'er. Kredit:Tohoku University
De fleste lægemiddelleveringssystemer bruger nanobærere til at transportere lægemidler på grund af deres lille størrelse og evne til at distribuere lægemidler til ellers utilgængelige steder i kroppen. Ulempen ved denne lille størrelse, imidlertid, er, at store mængder er nødvendige for at matche den nødvendige dosis.
Alternative transportørfrie systemer, kendt som nanopræparater (NPD), vise enorme løfter for kræftbehandling. For eksempel, en SN-38 NPD har omkring 10 gange højere anticancereffektivitet end kommercielt tilgængelige lægemidler. Nu, forskere har, for første gang, udviklet en omfattende undersøgelse af dynamikken af SN-38 NPD'er inde i kræftceller, inklusive deres internaliseringshastighed, intracellulær lokalisering, og nedbrydning, samt deres terapeutiske effektivitet.
"Disse innovative systemer viser høj anticanceraktivitet, men den grundlæggende viden for klinisk oversættelse, såsom deres interaktion med kræftceller, manglede stadig, " sagde professor Hitoshi Kasai, medforfatter af undersøgelsen.
Forskerholdet evaluerede tilstanden af NPD'er inde i kræftceller ved hjælp af den Förster Resonance Energy Transfer (FRET) baserede mikroskopiteknik. FRET er afhængig af energioverførslen mellem to lysfølsomme molekyler. Ved at drage fordel af den fluorescerende egenskab af SN-38 sammen med Bodipy FL fluorescensproben i de NPD'er, der er specielt designet til denne undersøgelse, FRET tillod forskerne at observere tilstanden af NPD'er fra intakt partikel til det opløste prodrug.
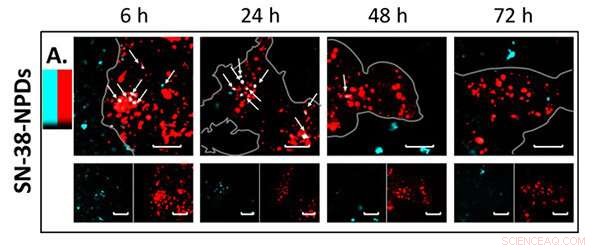
Fluorescensbilleder af NPD'er (i blåt), der co-lokaliserer og nedbryder inde i lysosomer (i rødt) over tid. Kredit:Tohoku University
Konfokal lasermikroskopi-observation bekræftede signifikant NPD-nedbrydning fra intakt tilstand til et opløst prodrug inde i cellerne over tid. Dette betyder, at NPD'er konsekvent blev absorberet af celler som intakte partikler, før de blev transporteret ind i lysosomerne - en membranbundet organel indeholdende fordøjelsesenzymer. En gang inde i lysosomerne, SN-38 prodrug opløst fra en intakt partikel (figur 2) og udførte dets terapeutiske virkninger på cancercellerne.
Kasai tilføjer, at "Vores værker giver et omfattende overblik over dynamikken af prodrug nanopartikler inde i kræftceller, giver mulighed for yderligere fremskridt hen imod deres anvendelse som næste generations anticancer-lægemiddelleveringsanordninger."
 Varme artikler
Varme artikler
-
 Optisk støvsuger kan manipulere nanopartiklerKoncept af den optiske støvsuger. Kredit:Tomsk Polytekniske Universitet Forskere ved Tomsk Polytechnic University udviklede sammen med russiske og internationale kolleger konceptet til at konstrue
Optisk støvsuger kan manipulere nanopartiklerKoncept af den optiske støvsuger. Kredit:Tomsk Polytekniske Universitet Forskere ved Tomsk Polytechnic University udviklede sammen med russiske og internationale kolleger konceptet til at konstrue -
 Ny molekylær egenskab kan betyde mere effektive sol- og optoelektroniske enhederEt nyt papir fra UMass Amherst beskriver en struktur, der vil gøre det lettere at bruge et bestemt molekyle til nye applikationer, for eksempel i enheder, der bruger polariseret lysindgang til optisk
Ny molekylær egenskab kan betyde mere effektive sol- og optoelektroniske enhederEt nyt papir fra UMass Amherst beskriver en struktur, der vil gøre det lettere at bruge et bestemt molekyle til nye applikationer, for eksempel i enheder, der bruger polariseret lysindgang til optisk -
 Fysikere opdager en ny form for friktion i nanoverdenenUndersøgelse af nanosystemers friktionsadfærd, forskere fra Technische Universitaet Muenchen (TUM) har opdaget en hidtil ukendt type friktion, den såkaldte desorptionspind. De fastgjorde en polymerkæd
Fysikere opdager en ny form for friktion i nanoverdenenUndersøgelse af nanosystemers friktionsadfærd, forskere fra Technische Universitaet Muenchen (TUM) har opdaget en hidtil ukendt type friktion, den såkaldte desorptionspind. De fastgjorde en polymerkæd -
 Nyt fænomen i nanodiske magnetiske hvirvlerMTXM-billeder af magnetiske komponenter i planet (a) og ude af planet (b) i et array af permalloy nanodiske. Magnetisk rotation i planet er vist med hvid pil (a). Kernepolarisering er markeret med sor
Nyt fænomen i nanodiske magnetiske hvirvlerMTXM-billeder af magnetiske komponenter i planet (a) og ude af planet (b) i et array af permalloy nanodiske. Magnetisk rotation i planet er vist med hvid pil (a). Kernepolarisering er markeret med sor
- Dronebaseret termisk billeddannelse og analyse for energieffektivitet
- Sådan finder du halvdelen af en fraktion
- Fem fakta om kinetisk energi
- Hvorfor arktisk jord kan glide væk
- Lav-energi RHIC elektronkøling får grønt lys, bogstaveligt talt
- Fysikere ved Mainz Universitet konstruerer prototype til ny komponent i ATLAS -detektoren


