Forskere bruger nanoteknologi til at ødelægge og forhindre tilbagefald af solid tumorkræft
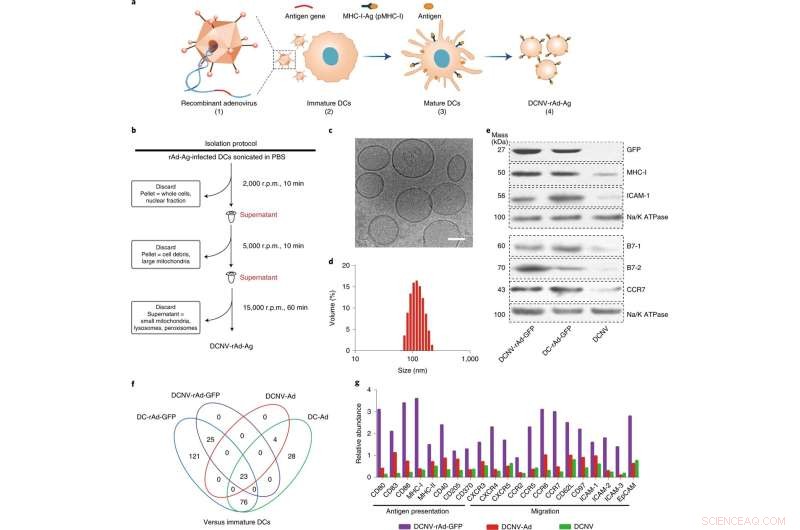
Generering og karakterisering af DCNV-rAd-Ag. a, Generering af DCNV'er afledt af adenovirus-inficerede modne dendritiske celler. (1) Generne af tumorspecifikt antigen blev gensplejset ind i adenovirusvektoren. (2) Rekombinant adenovirus inficerede de umodne DC2.4-celler for at udtrykke det modificerede antigen på celleoverfladen og stimulere det. (3) Differentiering, modning og antigenpræsentation. (4) Høst af den inducerede modne cellemembran og fremstilling af DCNV-rAd-Ag. b, Skematisk illustration af dannelsen af DCNV-rAd-Ag. c,d, kryo-elektronmikroskopi (c) og dynamiske lysspredningsanalyser (d) viste ensartet DCNV-rAd-Ag (ca. 108 nm gennemsnitlig diameter, polydispersitetsindeks =0,14) med en vesikellignende morfologi. Målestok, 50 nm. e, Western blot på membranproteiner fra DCNV-rAd-GFP demonstrerer et lignende proteinindhold på overfladen sammenlignet med det af forældrecellerne. Paneler c–e viser repræsentative resultater af to uafhængige eksperimenter med lignende resultater. f, Sammenligning af opregulerede immunrespons-relaterede proteiner i NV'er og DC'er. g, den relative overflod af antigenpræsentation og migrationsrelaterede proteiner på DCNV-rAd-GFP. r.p.m., omdrejninger i minuttet. CCR, CC kemokinreceptor; CXCR, C-X-C kemokinreceptor; EpCAM, epitelcellulært adhæsionsmolekyle; ICAM 1, intercellulært adhæsionsmolekyle 1; pMHC-I, peptid-major histokompatibilitetskompleks klasse I. Kredit:Nature Nanotechnology (2022). DOI:10.1038/s41565-022-01098-0
Mens mennesker over hele kloden ser frem til længere levealder, fortsætter maligne kræftformer med at udgøre en trussel mod menneskers sundhed. Udforskningen og udviklingen af immunterapi har til formål at søge nye gennembrud til behandling af solide tumorer.
Den vellykkede etablering af antitumorimmunitet kræver aktivering, udvidelse og differentiering af antigenspecifikke lymfocytter. Denne proces afhænger i høj grad af specifikke interaktioner mellem forskellige T-celler og antigen-præsenterende celler (APC'er) i kroppen. Imidlertid er eksisterende tumorvacciner, såsom neoantigenvacciner og forskellige vektorvacciner, alle afhængige af tilfældige interaktioner med APC'er i kroppen. Ydermere kan upassende interaktioner føre til, at andre immunreaktioner dæmpes.
Selvom immuncheckpoint-baseret immunterapi har vist sig at have et stort potentiale, reagerer kun en lille del af patienterne fuldt ud på denne terapi, og de relevante molekylære mekanismer skal undersøges yderligere. Denne leveringsmetode er dog kompleks og ineffektiv.
I en banebrydende udvikling har et team af videnskabsmænd ledet af Narat Muzayyin-formand professor Chen Xiaoyuan fra NUS Yong Loo Lin School of Medicine og professor Liu Gang fra Xiamen University formuleret en ny vaccine, som viste høj effektivitet i behandlingen af solide tumorer og opnåede fuldstændig fjernelse af solide tumorer og inducering af langvarig immunhukommelse. Dette forhindrer tilbagefald af tumorvækst, som patienten oprindeligt præsenterede for, og giver immunitet mod lignende tumortyper. Dette blev bevist gennem anvendelsen af denne vaccine på melanom tumormodeller. Deres resultater er offentliggjort i Nature Nanotechnology .
Holdet var i stand til at konstruere en dendritisk celle (en type APC) membran, der blev brugt til naturligt at stimulere immunsystemet og aktivere multi-dimensionel anti-tumor immunitet. Dette blev gjort gennem en antigen-selv-præsentation og immunosuppression reverserende nanovesikel-vaccineplatform, som fik holdet til at opfinde sin moniker, ASPIRE.
ASPIRE-vaccinesystemet kan hurtigt fremkalde passende, antigenspecifikke immunresponser på en måde, som traditionelle vaccinemetoder ikke kunne. Denne antigenpræsentationsmåde forbedrer i høj grad effektiviteten af immunaktivering, hvilket letter denne nye vaccines høje effektivitet i forhold til andre vacciner, der er tilgængelige i øjeblikket. Derudover kan vaccinen også aktivere både tidligere ueksponerede T-celler og udmattede T-celler, hvilket letter ASPIRE's overlegne antitumor-immunkapacitet.
"Vi er begejstrede for denne platformsteknologis potentiale for yderligere anvendelse i andre sygdomme også, såsom kronisk virusinfektion, hvor T-celleudmattelse ofte forekommer under infektion og forhindrer den optimale viruskontrol," sagde professor Chen. "Dernæst håber holdet at etablere en standard operationsprocedure for skaleret syntese af vaccinen med korrekt kvalitetskontrol af membranvesiklerne til klinisk oversættelse," tilføjede han.
Professor Chng Wee Joo, seniorkonsulent ved afdelingen for hæmatologi ved afdelingen for hæmatologi-onkologi i National University Cancer Institute, Singapore og myelomspecialist, sagde uafhængigt af undersøgelsen:"Kraftimmunterapiområdet tilbyder enormt håb for kræft. patienter. Der er dog nogle mangler ved de nuværende teknologier. Den nuværende innovation fra Prof Chen og hans kolleger overvinder nogle af disse mangler og forbedrer effektiviteten og
bæredygtigheden af immunresponset på disse behandlinger. Dette vil give en betydelig fremskridt, som vil have stor indflydelse på patienterne." + Udforsk yderligere
Ny vaccine nanoteknologi
 Varme artikler
Varme artikler
-
 Regioselektiv magnetisering muliggjorde chirale halvledende heteronanorodsen, Skematisk illustration af magnetisk induceret chiroptisk aktivitet. b, Model af materialiseret magnetit nanodomæne ved en spids af ZnxCd1-xS halvleder nanorod. Kredit:ZHUANG et al. Et USTC-hol
Regioselektiv magnetisering muliggjorde chirale halvledende heteronanorodsen, Skematisk illustration af magnetisk induceret chiroptisk aktivitet. b, Model af materialiseret magnetit nanodomæne ved en spids af ZnxCd1-xS halvleder nanorod. Kredit:ZHUANG et al. Et USTC-hol -
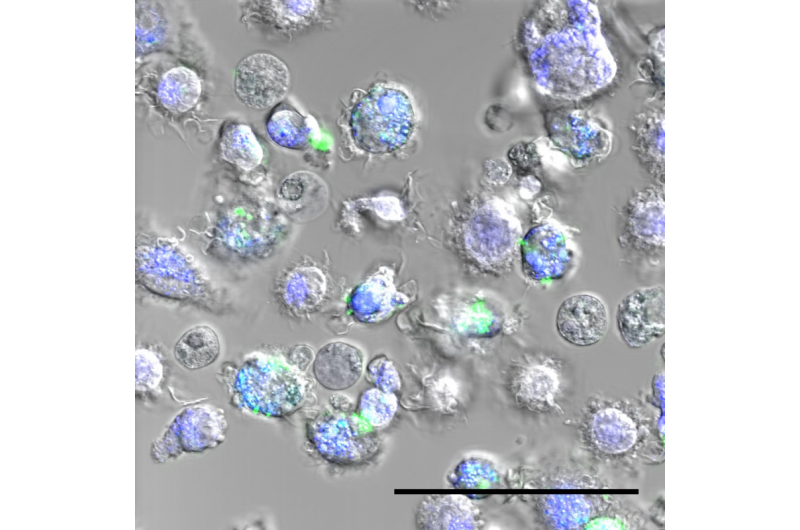 En banebrydende metode til screening af de mest nyttige nanopartikler til medicinMakrofager med nanopartikler, i grøn. Kredit:Laboratoire Bourquin – UNIFR/UNIGE Brugen af nanopartikler - små, grundstoffer på størrelse med virus, der er udviklet under laboratorieforhold - er
En banebrydende metode til screening af de mest nyttige nanopartikler til medicinMakrofager med nanopartikler, i grøn. Kredit:Laboratoire Bourquin – UNIFR/UNIGE Brugen af nanopartikler - små, grundstoffer på størrelse med virus, der er udviklet under laboratorieforhold - er -
 Mikroskopi fremskridt afslører uventet rolle for vand i energilagringsmaterialeAFM afslører, at strukturelt vand i wolframoxid resulterer i mindre deformationshastigheder fra ioninterkalering, et uventet fund om rollen som strukturelt vand, der kan muliggøre materialer med højer
Mikroskopi fremskridt afslører uventet rolle for vand i energilagringsmaterialeAFM afslører, at strukturelt vand i wolframoxid resulterer i mindre deformationshastigheder fra ioninterkalering, et uventet fund om rollen som strukturelt vand, der kan muliggøre materialer med højer -
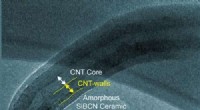 Super-nanorør:Bemærkelsesværdig spray-on-belægning kombinerer kulstof-nanorør med keramikDette er et mikrofotografi af en streng af en ny spray-on super-nanorør-komposit udviklet af National Institute of Standards and Technology (NIST) og Kansas State University. Den flervæggede nanorørs
Super-nanorør:Bemærkelsesværdig spray-on-belægning kombinerer kulstof-nanorør med keramikDette er et mikrofotografi af en streng af en ny spray-on super-nanorør-komposit udviklet af National Institute of Standards and Technology (NIST) og Kansas State University. Den flervæggede nanorørs
- Hvad er vintermonsoner?
- Genève-udstillingen har elektriske apparater, sportsvogne og en VW klitvogn
- Hvad er Genotype for Roan Color?
- Sådan bygges en kran til en skoleprojekt
- NASA undersøger CubeSat -mission for at løse venusisk mysterium
- Google betaler enorme summer for at bevare søgemaskinedominansen, siger DOJ


