Forskere udvikler lovende vaccinemetode mod tilbagevendende UVI
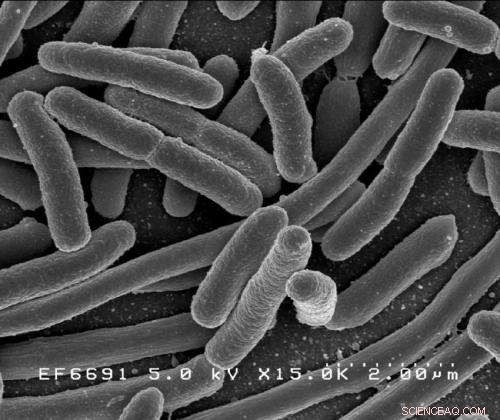
Escherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH
Forskere ved University of Texas i Dallas undersøger brugen af helcellevacciner til at bekæmpe urinvejsinfektion (UTI), en del af et forsøg på at tackle det stadig mere alvorlige problem med antibiotika-resistente bakterier.
Dr. Nicole De Nisco, assisterende professor i biologiske videnskaber, og Dr. Jeremiah Gassensmith, lektor i kemi og biokemi, demonstrerede for nylig brugen af metal-organiske rammer (MOF'er) til at indkapsle og inaktivere hele bakterieceller for at skabe et "depot" der gør det muligt for vaccinerne at holde længere i kroppen.
Den resulterende undersøgelse, offentliggjort online 21. september i American Chemical Societys tidsskrift ACS Nano , viste, at denne metode hos mus producerede væsentligt forbedret antistofproduktion og signifikant højere overlevelsesrater sammenlignet med standard helcellevaccinefremstillingsmetoder.
"Vaccination som en terapeutisk vej for tilbagevendende UTI'er er ved at blive udforsket, fordi antibiotika ikke længere virker," sagde De Nisco. "Patienter mister deres blærer for at redde deres liv, fordi bakterierne ikke kan dræbes af antibiotika eller på grund af en ekstrem allergi over for antibiotika, som er mere almindelig i den ældre befolkning, end folk måske er klar over."
Den amerikanske urologiske forening anslår, at 150 millioner UVI'er forekommer årligt på verdensplan, hvilket tegner sig for 6 milliarder dollars i medicinske udgifter. Hvis den ikke behandles med succes, kan en UVI føre til sepsis, som kan være dødelig.
Tilbagevendende UVI, sagde De Nisco, betragtes primært som et kvindesundhedsproblem, og selvom det er almindeligt – især hos postmenopausale kvinder – er det noget, mange kvinder ikke taler meget om.
"Hver efterfølgende infektion bliver sværere at behandle," sagde De Nisco. "Selv hvis du fjerner bakterierne fra blæren, fortsætter populationer andre steder og bliver normalt resistente over for det anvendte antibiotikum. Når patienter akkumulerer antibiotikaresistens, vil de i sidste ende løbe tør for muligheder."
De Niscos fortsatte udforskning af, hvordan UTI'er skrider frem og gentager sig hos ældre kvinder, er finansieret af et nyligt femårigt tilskud på 1,3 millioner dollars fra National Institutes of Health.
De Niscos samarbejde med Gassensmith begyndte i slutningen af 2018, efter at hun holdt en præsentation om mikrobiologien ved UTI for et udvalg for sikkerhedsprotokol på campus.
"Bagefter talte vi om min forskergruppes idé om at skabe bedre helcellevacciner ved at bevare antigener i dette slow-release depot," sagde Gassensmith. "På det tidspunkt havde vi ingen rigtige modeller at teste det med, og jeg syntes UTI var en meget god mulighed."
Vacciner virker ved at indføre en lille mængde dræbte eller svækkede sygdomsfremkaldende bakterier eller nogle af deres komponenter i kroppen. Disse antigener får immunsystemet til at producere antistoffer mod en bestemt sygdom. At bygge vacciner mod patogene bakterier er i sagens natur vanskeligt, fordi bakterier er væsentligt større og mere komplekse end vira. Det har været en stor udfordring at vælge, hvilke biologiske komponenter der skal bruges til at skabe antigener.
Derfor er det at foretrække at bruge hele cellen frem for kun at vælge et stykke af en bakterie, sagde Gassensmith.
"Vi kaster hele køkkenvasken efter dem, fordi det er det, din krop normalt ser, når den bliver inficeret," sagde han.
Helcelletilgangen har dog sine egne problemer.
"Vacciner, der bruger døde helcellebakterier, har ikke haft succes, fordi cellerne typisk ikke holder længe nok i kroppen til at producere langsigtede, holdbare immunresponser," sagde Gassensmith. "Det er grunden til vores MOF-antigendepot:Det tillader et intakt, dødt patogen at eksistere i vævet længere, som om det var en infektion, for at udløse en fuldskala immunsystemrespons."
Den metalorganiske ramme, som Gassensmiths team udviklede, indkapsler og immobiliserer en individuel bakteriecelle i en krystallinsk polymermatrix, der ikke kun dræber bakterien, men også bevarer og stabiliserer de døde celler mod høj temperatur, fugt og organiske opløsningsmidler.
I deres eksperimenter brugte forskerne en stamme af Escherichia coli . Der er ingen vacciner mod nogen patogen stamme af denne bakterie. Uropatogene E. coli forårsager omkring 80 % af alle samfundserhvervede UVI'er.
"Da vi udfordrede disse mus med en dødelig injektion af bakterier, efter at de var blevet vaccineret, overlevede næsten alle vores dyr, hvilket er en meget bedre ydeevne end med traditionelle vaccinemetoder," sagde Gassensmith. "Dette resultat blev gentaget flere gange, og vi er ret imponerede over, hvor pålideligt det er."
Selvom metoden endnu ikke er blevet testet på mennesker, sagde De Nisco, at den har potentialet til at hjælpe millioner af patienter.
"Denne undersøgelse om UVI var et bevis på, at helcellevacciner er mere effektive i denne ekstreme, dødelige sepsis-model," sagde De Nisco. "At vise, at dette virker mod tilbagevendende UVI ville være et betydeligt gennembrud."
Ud over tilbagevendende UVI eller urosepsis mener forskere, at antigen-depotmetoden kan anvendes bredt på bakterielle infektioner, herunder endokarditis og tuberkulose.
"Vi arbejder på at oversætte denne tilgang til TB, som er en meget anderledes organisme, men ligesom uropatogen E. coli , når det kommer ind i vævet, bliver det, og det kommer igen," sagde Gassensmith. "Det kræver en ny måde at tænke på, hvordan vacciner skal virke.
"Vaccineteknologi er omkring to århundreder gammel, og den har udviklet sig forbløffende lidt. Vi håber, at vores platform kan åbne op for at bruge eksisterende, velundersøgte patogener til at skabe mere rettet og konstrueret immunrespons." + Udforsk yderligere
Tilbagevendende UTI'er knyttet til skjult reservoir
 Varme artikler
Varme artikler
-
 Hexagonale bornitrider bemærkelsesværdig sejhed afsløretEt scanningselektronmikroskopbillede viser forgrenede revner i en enkelt krystal af 2D hexagonal bornitrid (h-BN). Eksperimenter og beregningsmodeller fra Rice University og Nanyang Technological Univ
Hexagonale bornitrider bemærkelsesværdig sejhed afsløretEt scanningselektronmikroskopbillede viser forgrenede revner i en enkelt krystal af 2D hexagonal bornitrid (h-BN). Eksperimenter og beregningsmodeller fra Rice University og Nanyang Technological Univ -
 Cellemembran på en chip kan fremskynde screening af lægemiddelkandidater for COVID-19Forskere har udviklet en menneskelig celles membran på en chip, der tillader kontinuerlig overvågning af, hvordan lægemidler og infektiøse midler interagerer med vores celler, og kan snart blive brugt
Cellemembran på en chip kan fremskynde screening af lægemiddelkandidater for COVID-19Forskere har udviklet en menneskelig celles membran på en chip, der tillader kontinuerlig overvågning af, hvordan lægemidler og infektiøse midler interagerer med vores celler, og kan snart blive brugt -
 Universal sekvens af Chern isolatorer i superledende magisk vinkel grafenEnergispektrum af magisk vinkel moire grafen i magnetfelt, viser magiske serier af Chern-isolatorer inde i fladbåndene og landau-overkørsler i de dispersive bånd. Kredit:ICFO Forskere fra ICFO, Pr
Universal sekvens af Chern isolatorer i superledende magisk vinkel grafenEnergispektrum af magisk vinkel moire grafen i magnetfelt, viser magiske serier af Chern-isolatorer inde i fladbåndene og landau-overkørsler i de dispersive bånd. Kredit:ICFO Forskere fra ICFO, Pr -
 En robot kaldet WANDA (med video)Emory Chan, med Berkeley Labs Molecular Foundry, instruerer WANDA, en revolutionær robot, der fremstiller nanokrystaller, at udføre komplekse arbejdsgange, der traditionelt kræver stor kemierfaring. (
En robot kaldet WANDA (med video)Emory Chan, med Berkeley Labs Molecular Foundry, instruerer WANDA, en revolutionær robot, der fremstiller nanokrystaller, at udføre komplekse arbejdsgange, der traditionelt kræver stor kemierfaring. (
- Hærens videnskabsmænd tager nye drejninger på kvanteforskning
- Første 3D-analyse af stenværktøjene til afrikanske jæger-samlere
- Isotopisk bevis for forbedrede fossile brændstoffers kilder til aerosol ammonium i byatmosfæren
- Elektronik kan du vikle rundt om din finger
- Vejen er klar:CORNING tapper neutroner til udvikling af nye glaskompositioner
- Ny dating af Nebra sky disk


