Dual-miRNA-udløst DNA-nanomaskine til påvisning og behandling af undertype af brystkræft
Brystkræft er den mest almindelige malignitet hos kvinder, der udgør en alvorlig trussel mod kvinders sundhed. På grund af brystkræfts høje inter- og intratumorale heterogenitet kan klinisk behandling og prognose variere meget hos patienter.
I øjeblikket er kemoterapi den vigtigste systemiske behandling af triple-negativ brystkræft (TNBC), en almindelig type brystkræft, som ikke har nogen af de receptorer, der almindeligvis findes i brystkræft. Imidlertid giver behandling med det ensartede højdosis kemoterapiregime uden molekylær subtypebestemmelse ofte suboptimal effekt, hvilket tilføjer yderligere byrde og ubehag for patienterne.
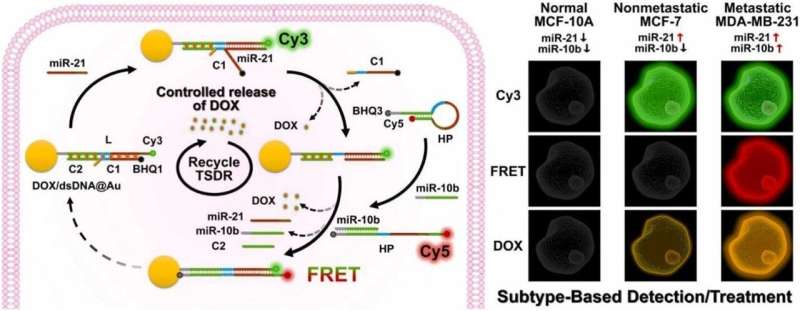
I en undersøgelse offentliggjort i Biomedicinsk Analyse , skitserer en gruppe forskere fra Kina en ny diskriminations- og behandlingstilgang - en dual-miRNA-udløst DNA-programmeret nanomaskine, der er i stand til at afbilde endogene miRNA-udtryk. Denne tilgang gør subtype-baseret detektion mulig og regulerer derved lægemiddelfrigivelse til kemoterapi.
"Til diagnosticering og subtypebestemmelse af brystkræft er histologisk undersøgelse af punkturbiopsiprøven 'guldstandarden', men det er invasivt og vanskeligt at realisere dynamisk overvågning af tumorprogression og prognose til behandlingsvejledning," forklarer undersøgelsens tilsvarende forfatter Yun Xiang , professor i luminescensanalyse og molekylær sansning ved Southwest University.
"Fluorescensbilleddannelsesteknikker er i stand til at visualisere og overvåge minimale molekylære ændringer, der forekommer på et tidligt stadium af cancere med høj opløsning og følsomhed. Enkelt miRNA-billeddannelse er dog ikke egnet til at skelne mellem kræftcelletyper."
Mens tidligere undersøgelser har vist, at dobbelt miRNA-udløst lægemiddelfrigivelse kan anvendes til kræftbehandling via de tåholdsmedierede strengforskydningsreaktioner (TSDR), skræddersyede behandlinger, såsom højdosis kemoterapi i TNBC og konventionel dosis kemoterapi i andre brystundertyper, er ikke blevet realiseret.
"Vi udviklede en DNA-programmeret nanomaskine til effektiv diskrimination og skræddersyet behandling af specifikke brystkræftcelletyper," siger Shunmei Li, førsteforfatter af undersøgelsen.
"Det er en responsiv terapistrategi over for de forskellige celletilstande. Denne intelligente nanomaskine med kontrolleret frigivelse af anticancerlægemiddel i specifikke kræftcelleundertyper kan reducere bivirkningen til normale celler og lette den målrettede terapi, som er lovende som en terapeutisk nanoplatform i præcis medicin."
Flere oplysninger: Shunmei Li et al, Dual-microRNA-udløst og DNA-programmeret nanomaskine til subtype-baseret detektion og skræddersyet behandling af brystkræftceller, Biomedicinsk analyse (2024). DOI:10.1016/j.bioana.2024.01.001
Leveret af KeAi Communications Co.
 Varme artikler
Varme artikler
-
 Forskere bruger uordnet stof til beregning, udviklende banebrydende nanopartikel boolesk logiknetvæ…Skematisk over enhedens layout og arbejdsprincip. Kredit:(c) 2015 Natur nanoteknologi (2015) doi:10.1038/nnano.2015.207 (Phys.org) – Naturlige computere, såsom udviklede hjerner og cellulære aut
Forskere bruger uordnet stof til beregning, udviklende banebrydende nanopartikel boolesk logiknetvæ…Skematisk over enhedens layout og arbejdsprincip. Kredit:(c) 2015 Natur nanoteknologi (2015) doi:10.1038/nnano.2015.207 (Phys.org) – Naturlige computere, såsom udviklede hjerner og cellulære aut -
 Elektronholografi afslører den overraskende skønhed ved magnetiske hvirvler i nanoskalaFigur 1:Høj opløsning, tredimensionel analyse af skyrmioner afslører en bemærkelsesværdig detaljeret magnetisk struktur. Kredit:H. S. Park et al. Magnetiske hvirvler i nanoskala kendt som skyrmion
Elektronholografi afslører den overraskende skønhed ved magnetiske hvirvler i nanoskalaFigur 1:Høj opløsning, tredimensionel analyse af skyrmioner afslører en bemærkelsesværdig detaljeret magnetisk struktur. Kredit:H. S. Park et al. Magnetiske hvirvler i nanoskala kendt som skyrmion -
 Alt-i-én transparente transistorerKredit:CC0 Public Domain Små justeringer i komponentforhold genererer elektronisk forskellige lag fra det samme materiale for at skabe transparente transistorer. Verdensomspændende efterspørgsel
Alt-i-én transparente transistorerKredit:CC0 Public Domain Små justeringer i komponentforhold genererer elektronisk forskellige lag fra det samme materiale for at skabe transparente transistorer. Verdensomspændende efterspørgsel -
 Undersøgelse undersøger, hvordan nanopartikler påvirker marine organismerJ. Evan Ward, professor i havvidenskab, viser besøgende live video af forskning i muslinger i hans laboratorium under en rundvisning i Marine Sciences Building. Foto af Peter Morenus (PhysOrg.com)
Undersøgelse undersøger, hvordan nanopartikler påvirker marine organismerJ. Evan Ward, professor i havvidenskab, viser besøgende live video af forskning i muslinger i hans laboratorium under en rundvisning i Marine Sciences Building. Foto af Peter Morenus (PhysOrg.com)
- 10 spørgsmål, som videnskaben ikke kan besvare endnu
- Hvad er Rosetta-stenen, og hvorfor artefakt er vigtigt?
- Kombineret tilgang til sondering af grænsefladeelektrokemi mere detaljeret
- Hvad frygter amerikanerne mest? Forskere udgiver 4. årlige Survey of American Fears
- Forskere lærer at styre grafen med lasere
- Forskning:COVID-19 har sandsynligvis forværret ulighederne for sorte studerende i L.A. County


