Nano-størrelse cellepartikler er lovende interventionsværktøj til behandling af infektionssygdomme, siger undersøgelse

COVID-19-pandemien viste vigtigheden af at være forberedt med lægemiddelinterventioner for at begrænse virale udbrud, der ellers kan have ødelæggende konsekvenser. I forberedelserne til den næste pandemi – eller sygdom X, er der et presserende behov for alsidige platformsteknologier, som med kort varsel kan genanvendes til at bekæmpe smitsomme udbrud.
Et team af forskere, ledet af adjunkt Minh Le fra Institut for Digital Medicin (WisDM) og Institut for Farmakologi ved Yong Loo Lin School of Medicine, National University of Singapore (NUS Medicine), opdagede, at partikler i nanostørrelse frigivet af celler, kaldet "ekstracellulære vesikler" (EV'er), kan bremse den virale smitteevne af SARS-CoV-2 – dens vildtype- og variantstammer – og potentielt andre infektionssygdomme.
Asst Prof Le sagde, "Vores undersøgelse viste, at disse celle-afledte nanopartikler er effektive bærere af lægemidler, der målretter mod virale gener præcist. Disse EV'er er derfor et effektivt værktøj til terapeutisk intervention hos patienter, der er inficeret med COVID-19 eller andre infektiøse sygdomme."
Undersøgelsen, udført i samarbejde med NUS Medicines Biosafety Level 3 (BSL3) Core Facility, Cancer Science Institute of Singapore ved National University of Singapore og School of Physical and Mathematical Sciences ved Nanyang Technological University (NTU), viste kraftig hæmning af COVID-19-infektion i laboratoriemodeller ved hjælp af en kombination af EV-baseret hæmning og anti-sense RNA-terapi medieret af antisense oligonukleotider (ASO'er).
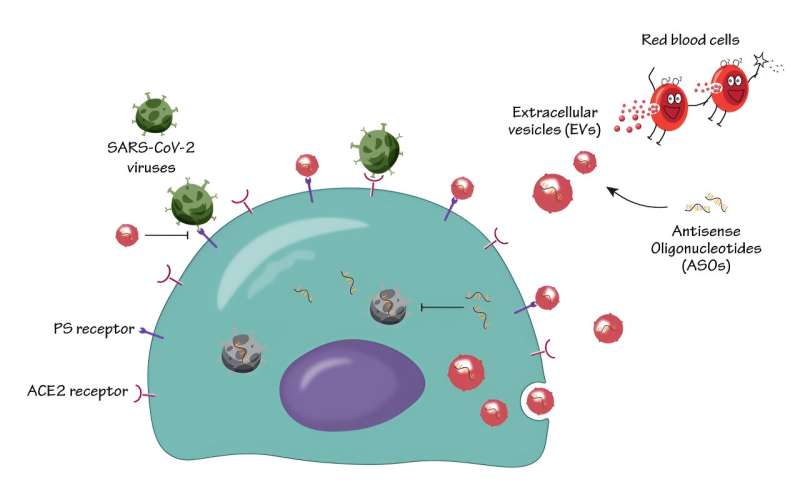
Et alsidigt værktøj, der kan anvendes på ethvert gen af interesse, ASO'er kan genkende og binde til komplementære områder af mål-RNA-molekyler og inducere deres hæmning og nedbrydning.
I undersøgelsen, offentliggjort i ACS Nano , brugte forfatterne menneskelige røde blodlegemer-afledte EV'er til at levere ASO'er til nøglesteder inficeret med SARS-CoV-2, hvilket resulterede i effektiv undertrykkelse af SARS-CoV-2-infektion og replikation.
Forskerne opdagede også, at elbiler udviste distinkte antivirale egenskaber, der er i stand til at hæmme phosphatidylserin (PS) receptor-medierede veje for virusinfektion - en nøglevej, der bruges af mange vira til at lette virusinfektion. Disse virale hæmmende mekanismer var anvendelige til flere varianter af SARS-CoV-2, inklusive delta- og omicron-stammerne, hvilket sikrede deres brede effektivitet mod SARS-CoV-2-infektion.
Resultaterne fra undersøgelsen peger på anti-sense RNA-terapi med ASO'er som en potentielt effektiv tilgang, der kan tjene til at bekæmpe fremtidige virale udbrud. Platformen, der blev udviklet til at levere ASO'er gennem EV'er for at målrette SARS-CoV-2 virale gener, kan let anvendes til at behandle andre virale infektioner ved at erstatte ASO-sekvenserne med dem, der er komplementære til de virale målgener.
Asst Prof Le og hendes kandidatstuderende Migara Jay og Gao Chang, de første forfattere af undersøgelsen, udvikler i øjeblikket mere potente kombinationer af ASO'er ved hjælp af kunstig intelligens-forudsigelsesmodeller for at opnå forbedret viral hæmning. Denne samarbejdsindsats omfatter et partnerskab med forskerholdene af lektor Edward Chow fra WisDM, NUS Medicine og NUS Medicines BSL3 Core Facility.
Lektor Justin Chu, direktør for BSL3 Core Facility ved NUS Medicine og medforfatter af undersøgelsen, tilføjede:"Denne bemærkelsesværdige ekstracellulære vesikelbaserede leveringsplatformteknologi kombineret med antiviral terapi er meget lovende til at bekæmpe en bred vifte af vira og endda sygdom X."
Sidstnævnte er en generel beskrivelse af nye og ukendte smitsomme trusler, såsom nye coronavirus. Udtrykket blev brugt til at advare og fremme udviklingen af platformsteknologier, herunder vacciner, lægemiddelterapier og diagnostiske tests, som hurtigt kunne tilpasses og derefter implementeres mod fremtidige epidemier og pandemiske udbrud. Assoc Prof Chu er også fra Infectious Diseases Translational Research Program ved NUS Medicine.
Professor Dean Ho, Provost's Chair Professor og direktør for WisDM ved NUS Medicine, sagde:"Dette arbejde bringer den skalerbare og veltolererede ekstracellulære vesikelbaserede lægemiddelleveringsplatform et vigtigt skridt nærmere kliniske valideringsstudier."
Flere oplysninger: Migara K. Jayasinghe et al., røde blodlegemer-afledte ekstracellulære vesikler viser endogene antivirale virkninger og forbedrer effektiviteten af antiviral oligonukleotidterapi, ACS Nano (2023). DOI:10.1021/acsnano.3c06803
Journaloplysninger: ACS Nano
Leveret af National University of Singapore
 Varme artikler
Varme artikler
-
 Planteinspiration kan føre til fleksibel elektronikEn plantestamme inspirerede forskere til at udvikle en ny, alsidig aerogel til mulig brug i bøjelige enheder. Kredit:American Chemical Society Alsidig, lette materialer, der er både stærke og mods
Planteinspiration kan føre til fleksibel elektronikEn plantestamme inspirerede forskere til at udvikle en ny, alsidig aerogel til mulig brug i bøjelige enheder. Kredit:American Chemical Society Alsidig, lette materialer, der er både stærke og mods -
 Næste generations elektronik:Udvider mulighederne med sølv nanotråde(L) Skematisk illustration af sølv nanotråd med glat, ultratynd guldskal, (R) Skematisk illustration af guldbelagt sølv nanotråd med ætsning, " eller poredannelse. Kredit:Khademhosseini Lab N
Næste generations elektronik:Udvider mulighederne med sølv nanotråde(L) Skematisk illustration af sølv nanotråd med glat, ultratynd guldskal, (R) Skematisk illustration af guldbelagt sølv nanotråd med ætsning, " eller poredannelse. Kredit:Khademhosseini Lab N -
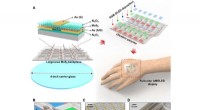 Aktiv matrix organisk lysemitterende diode display på menneskelig hudAMOLED-skærmen i fuld farve med MoS2-baseret bagside med stort område. (A) Skematisk illustration af den højtydende MoS2-baserede bagplade på et 4-tommers bæreglassubstrat, hvor et Al2O3-afdækningslag
Aktiv matrix organisk lysemitterende diode display på menneskelig hudAMOLED-skærmen i fuld farve med MoS2-baseret bagside med stort område. (A) Skematisk illustration af den højtydende MoS2-baserede bagplade på et 4-tommers bæreglassubstrat, hvor et Al2O3-afdækningslag -
 Bobler er de nye linser til lysstråler i nanoskalaDette er laboratoriebilleder af en lysstråle uden en bobleobjektiv, efterfulgt af tre eksempler på forskellige boblelinser, der ændrede lyset. Kredit:Tony Jun Huang, Penn State At bøje lysstråler
Bobler er de nye linser til lysstråler i nanoskalaDette er laboratoriebilleder af en lysstråle uden en bobleobjektiv, efterfulgt af tre eksempler på forskellige boblelinser, der ændrede lyset. Kredit:Tony Jun Huang, Penn State At bøje lysstråler
- NASA Mars rover begynder at samle sten på jagt efter fremmed liv
- Et problem eller en mulighed? App-baseret arbejde adskiller og isolerer medarbejdere fra deres kolle…
- En meteoroid smadrede ind i siden af et krater på Mars og startede derefter et jordskred
- Transportørers usikre procedurer gør livet nemt for SIM-byttetrickstere
- Forskellen mellem et bægerglas og en gradueret cylinder
- Undersøgelser viser, at urbanisering påvirker storme, nedbør trods omgivelserne


