Cystisk fibrosemedicin kan være 'livsændrende' for patienter:Nye billeder afslører, hvordan molekylerne virker
Cystisk fibrose er en invaliderende genetisk lidelse, der påvirker cirka 70.000 mennesker verden over. For nylig har udviklingen af en revolutionerende klasse af lægemidler kaldet CFTR-modulatorer bragt nyt håb til patienter ved effektivt at korrigere det defekte protein, der er ansvarlig for sygdommens symptomer. Disse lægemidler virker på et molekylært niveau, og nu har banebrydende billeder fanget de indviklede detaljer i deres interaktioner, hvilket giver enestående indsigt i deres livsændrende effekter.
I hjertet af cystisk fibrose ligger en mutation i CFTR-genet, som koder for et protein, der er ansvarligt for at regulere bevægelsen af salt og vand over cellemembraner. Dette dårligt fungerende protein får tykt slim til at samle sig i lungerne, hvilket fører til kroniske luftvejsinfektioner, åndedrætsbesvær og en forkortet forventet levetid.
CFTR-modulatorer, såsom Ivacaftor, Lumacaftor og andre, virker ved at målrette og stabilisere CFTR-proteinet, redde dets funktion og tillade det at arbejde mere effektivt. Indtil nu har de nøjagtige mekanismer for, hvordan disse lægemidler interagerer med proteinet, været uhåndgribelige.
Gennem banebrydende billeddannelsesteknikker såsom kryo-elektronmikroskopi og røntgenkrystallografi har forskere med succes visualiseret de strukturelle ændringer induceret af CFTR-modulatorer på molekylært niveau. De resulterende billeder afslører, hvordan disse lægemidler binder til specifikke steder på CFTR-proteinet, hvilket forårsager konformationelle ændringer, der i sidste ende genopretter dets korrekte funktion.
I tilfældet med Ivacaftor, for eksempel, viser billederne, hvordan lægemidlet binder sig til en lomme i CFTR-proteinet, og fungerer som en "molekylær lim", der stabiliserer dets struktur. Denne stabilisering fører til forbedret kanalindgang, hvilket muliggør en effektiv strøm af ioner og vand over cellemembranen.
Tilsvarende afslører billeder af Lumacaftors interaktion med CFTR, hvordan det hjælper med at korrigere proteinets foldning, så det kan nå sin funktionelle form. Ved at adressere de underliggende strukturelle defekter forbedrer Lumacaftor proteinets evne til at regulere passagen af ioner og vand.
Disse banebrydende billeder tjener som et vidnesbyrd om kraften i videnskabelig innovation til at forstå det molekylære grundlag for sygdom og bane vejen for målrettede behandlinger. Bevæbnet med denne viden kan forskere nu designe og udvikle mere effektive CFTR-modulatorer og potentielt udvide deres applikationer til at behandle andre genetiske lidelser, der involverer proteinfejlfoldning.
Rejsen til at optrevle de molekylære forviklinger af cystisk fibrose-lægemidler er langt fra slut, men hvert skridt fremad bringer nyt håb for patienter, der ivrigt venter på livsændrende behandlinger. Mens forskningen fortsætter med at blomstre, byder fremtiden på et enormt løfte om at forbedre livet for utallige individer, der er ramt af denne ødelæggende sygdom.
 Varme artikler
Varme artikler
-
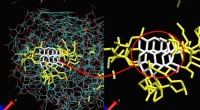 Ny model hjælper med at definere optimal temperatur og tryk for at smede nanoskala diamanterAt smede nanodiamanter, som har potentielle anvendelser inden for medicin, optoelektronik og kvanteberegning, forskere udsætter organiske eksplosive molekyler for kraftige detonationer i et kontroller
Ny model hjælper med at definere optimal temperatur og tryk for at smede nanoskala diamanterAt smede nanodiamanter, som har potentielle anvendelser inden for medicin, optoelektronik og kvanteberegning, forskere udsætter organiske eksplosive molekyler for kraftige detonationer i et kontroller -
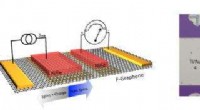 Banebrydende homøpitaksial grafentunnelbarriere/transportkanalanordningEt skematisk (venstre) og et optisk billede (til højre) af en af de homøpitaksiale fluorerede grafen/grafen-spinventilenheder. Det øverste lag af grafen bruges som tunnelbarriere. Det er fluoreret f
Banebrydende homøpitaksial grafentunnelbarriere/transportkanalanordningEt skematisk (venstre) og et optisk billede (til højre) af en af de homøpitaksiale fluorerede grafen/grafen-spinventilenheder. Det øverste lag af grafen bruges som tunnelbarriere. Det er fluoreret f -
 Nyt værktøj til tidlig påvisning af hypertensionI laboratoriet. Kredit:Sergey Gnuskov/NUST MISIS Russiske videnskabsmænd er kommet med et nyt værktøj til tidlig påvisning af hypertension. De anvendte overfladeforstærket Raman-spektroskopi drevet
Nyt værktøj til tidlig påvisning af hypertensionI laboratoriet. Kredit:Sergey Gnuskov/NUST MISIS Russiske videnskabsmænd er kommet med et nyt værktøj til tidlig påvisning af hypertension. De anvendte overfladeforstærket Raman-spektroskopi drevet -
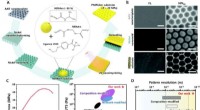 Stamcelleark høstet på kun to dageDesign af den bulk PNIPAAm nanopore-mønstrede overflade. (A) Diagram, der viser tre-trins nanoreplikationsprocessen bestående af aluminiumanodisering, nikkel nanoelektroformning, og UV nanoimprinting.
Stamcelleark høstet på kun to dageDesign af den bulk PNIPAAm nanopore-mønstrede overflade. (A) Diagram, der viser tre-trins nanoreplikationsprocessen bestående af aluminiumanodisering, nikkel nanoelektroformning, og UV nanoimprinting.
- Endnu et slag for fortolkningen af mørkt stof af det galaktiske centeroverskud
- Hvordan temperatur og luftfugtighed er relateret
- ESA opsender arktisk vejrsatellit i juni
- Verdens første demonstrator af grøn energilagring
- Ingeniør bruger gammel kunst med origami til at løse et meget moderne rumfartsproblem
- Du så det ikke komme:Ny forskning viser, at turbulente strømme kan være forårsaget af små trigg…


