Guld nanopartikel brugt til at erstatte virus i ny CRISPR-tilgang
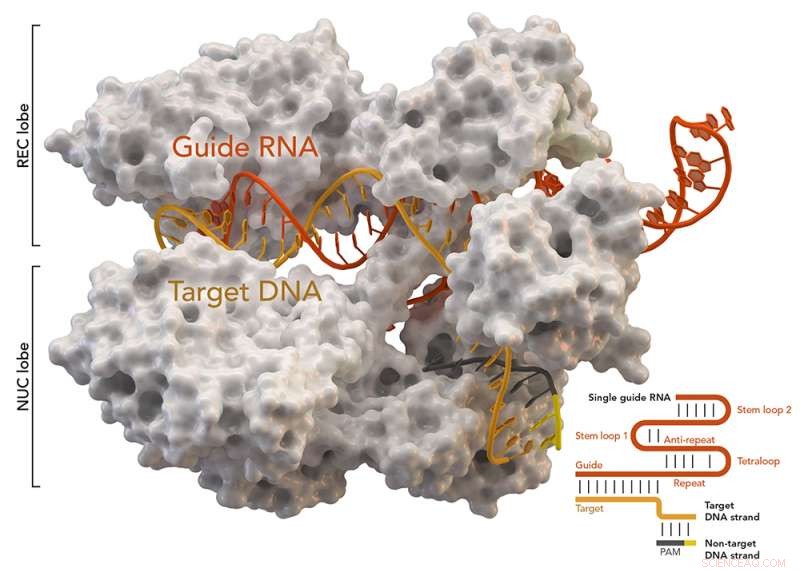
CRISPR-associeret protein Cas9 (hvid) fra Staphylococcus aureus baseret på Protein Database ID 5AXW. Kredit:Thomas Splettstoesser (Wikipedia, CC BY-SA 4.0)
(Phys.org) – Et team af forskere fra University of California og University of Tokyo har fundet en måde at bruge CRISPR-genredigeringsteknikken, der ikke er afhængig af en virus til levering. I deres papir offentliggjort i tidsskriftet Natur biomedicinsk teknik , gruppen beskriver den nye teknik, hvor godt det virker og forbedringer, der skal laves for at gøre det til et levedygtigt genredigeringsværktøj.
CRISPR-Cas9 har været i nyhederne på det seneste, fordi det giver forskere mulighed for direkte at redigere gener - enten deaktivere uønskede dele eller erstatte dem helt. Men på trods af mange succeshistorier, teknikken lider stadig af et stort underskud, der forhindrer den i at blive brugt som et ægte medicinsk værktøj - den laver nogle gange fejl. Disse fejl kan forårsage små eller store problemer for en vært, afhængigt af hvad der går galt. Tidligere forskning har antydet, at størstedelen af fejlene skyldes leveringsproblemer, hvilket betyder, at en erstatning for virusdelen af teknikken er påkrævet. I denne nye indsats, forskerne rapporterer, at de har opdaget netop sådan en erstatning, og det fungerede så godt, at det var i stand til at reparere en genmutation i en Duchenne muskeldystrofi-musemodel. Holdet har navngivet den nye teknik CRISPR-Gold, fordi en guld nanopartikel blev brugt til at levere de genredigerende molekyler i stedet for en virus.
Den nye pakke blev skabt ved at modificere en smule DNA for at få det til at klæbe til en guld nanopartikel og derefter et Cas9-protein og også en RNA-guide. Pakken blev derefter belagt med en polymer, der tjente som et indeslutningshylster - en, der også udløste endocytose (en form for celletransport) og hjalp molekylerne med at undslippe endosomerne, når de var inde i målcellerne. Molekylerne gik derefter i gang - Cas9 skar mål-DNA-strengen, guide-RNA'et viste, hvad der skulle gøres, og en DNA-streng blev placeret, hvor en mutation havde eksisteret. Resultatet var et gen fri for en mutation, der forårsager Duchennes muskelsvind.
Der er stadig et stort problem at løse med teknikken, dog – det virker kun i lokaliserede applikationer. Ideelt set en masse pakker vil blive sprøjtet ind i blodbanen, hvilket muliggør reparation af alle celletyper, såsom muskler svækket af et mutant gen.
© 2017 Phys.org
Sidste artikelAlgoritme forklarer, hvordan myrer skaber og reparerer stinetværk
Næste artikelTrofæjagt vil næppe påvirke evolutionen
 Varme artikler
Varme artikler
-
 Biologers nye bog beskriver en ny æra i undersøgelsen af evolutionHarvardbiolog Jonathan Losos, på billedet, der håndterer en amerikansk krokodilleskalle på MCZ, fortæller om sin nye bog, “Usandsynlige skæbner:Skæbne, Chance, og evolutionens fremtid. ” Kredit:Kris S
Biologers nye bog beskriver en ny æra i undersøgelsen af evolutionHarvardbiolog Jonathan Losos, på billedet, der håndterer en amerikansk krokodilleskalle på MCZ, fortæller om sin nye bog, “Usandsynlige skæbner:Skæbne, Chance, og evolutionens fremtid. ” Kredit:Kris S -
 Ørevoks som iskerner - låser op for fortiden skjult i hvalørepropperPukkelhvaler som disse har en varierende kost, som kan registreres i stabile kulstofisotoper lagdelt ind i ørevokspropperne, der er opbygget i løbet af deres liv. Kredit:Vicky Stein Farzaneh Manso
Ørevoks som iskerner - låser op for fortiden skjult i hvalørepropperPukkelhvaler som disse har en varierende kost, som kan registreres i stabile kulstofisotoper lagdelt ind i ørevokspropperne, der er opbygget i løbet af deres liv. Kredit:Vicky Stein Farzaneh Manso -
 Hvorfor DNA er det mest fordelagtige molekyle til genetisk materiale & hvordan RNA sammenligner det …Med undtagelse af visse vira bærer DNA snarere end RNA den arvelige genetiske kode i alt biologisk liv på Jorden. DNA er både mere elastisk og lettere repareret end RNA. Som et resultat tjener DNA som
Hvorfor DNA er det mest fordelagtige molekyle til genetisk materiale & hvordan RNA sammenligner det …Med undtagelse af visse vira bærer DNA snarere end RNA den arvelige genetiske kode i alt biologisk liv på Jorden. DNA er både mere elastisk og lettere repareret end RNA. Som et resultat tjener DNA som -
 Atrazin ændrer kønsforholdet i Blanchards cricketfrøerBlanchards cricketfrøer ( Acris blanchardi ) i amplexus. Kredit:Tyler D. Hoskins En undersøgelse, der for nylig blev offentliggjort i Miljøtoksikologi og kemi fandt ud af, at Blanchards cricke
Atrazin ændrer kønsforholdet i Blanchards cricketfrøerBlanchards cricketfrøer ( Acris blanchardi ) i amplexus. Kredit:Tyler D. Hoskins En undersøgelse, der for nylig blev offentliggjort i Miljøtoksikologi og kemi fandt ud af, at Blanchards cricke
- Svage sociale bånd en dræber for hanhvaler
- Duplikationer af ikke-kodende DNA kan have påvirket udviklingen af menneskespecifikke egenskaber
- Forskere afslører et nyt metal, hvor elektroner flyder med væskelignende dynamik
- Forskere transmitterer energi med laser i historisk strømstrålende demonstration
- Værktøjer lavet af mennesker i det gamle mesopotamia
- En ny måde at levere lysfølsomme lægemidler til at bekæmpe problemet med antibiotikaresistens


