Forskning afslører, hvordan celler genopbygges efter mitose

Illustration af nuklear F-actin, der arbejder på at omforme kernen og organisere genomet. Kredit:Claudia Stocker VividBiology
Når celler deler sig, de skal genopbygge deres kerne og organisere deres genom. Ny kollaborativ forskning fra University of Bristol viser, hvordan celler opnår dette gennem den uventede udbredelse af filamentøst actin (F-actin) til kernen.
Forskningen, udgivet online i Naturens cellebiologi , giver det første bevis på, at actinpolymerisation i kernen hjælper med at omforme kernen og reorganisere genomet efter celledeling (mitose).
Hos pattedyr, inklusive mennesker, cellekernen pakker og beskytter genomet. Når menneskelige celler deler sig, kernen skilles ad for at tillade adskillelse af kromosomerne. Når kromosomadskillelsen er fuldstændig, nye celler skal genopbygge deres kerne og organisere deres genom. denne proces, selvom det er vigtigt for livet, var dårligt forstået.
Dette arbejde er i samarbejde med professor Robert Grosse's Laboratory (University of Marburg, Tyskland), som afslørede dannelsen af forbigående og meget dynamisk F-actin i kernen af datterceller, da de begynder at genopbygge deres kerne efter mitose. Polymerisationen af actin (F-actin) sker let i cytoplasmaet af celler; hvor det tjener en meget vigtig funktion i at kontrollere celleform og gøre det muligt for celler at kravle rundt. Opdagelse af dette forbigående og dynamiske F-aktin i kernen kort efter celledeling, gav et hint om, at det kan være nødvendigt for at genopbygge kernen og reorganisere genomet.
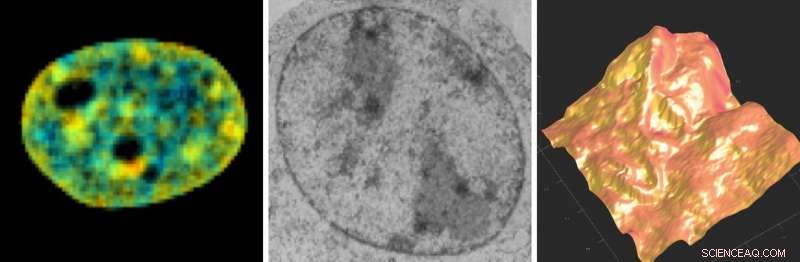
Cellebilleddannelsesmetoder udviklet og anvendt i denne undersøgelse. Fluorescens livstids billeddannelsesmikroskopi (FLIM), Elektronmikroskopi (EM), Atomkraftmikroskopi (AFM). Kredit:University of Bristol
Alice Sherrard med-førsteforfatter af denne undersøgelse og en ph.d.-studerende med Dr. Abderrahmane Kaidi, udviklet og implementeret komplementære og tværfaglige metoder til at visualisere nuklear struktur og genomorganisation efter celledeling. Ved at gøre sådan, Alice afslørede, at afbrydelse af dannelsen af F-actin resulterer i, at celler ikke kan udvide deres nukleare volumen såvel som deres manglende evne til at dekomprimere deres genom. På grund af disse defekter, celler bliver ineffektive til at hente genetisk information kodet i deres DNA; dermed, de deler sig langsommere.
Principal investigator Dr Abderrahmane Kaidi, en specialist i cancerbiologi ved University of Bristol's School of Cellular and Molecular Medicine, siger, at denne opdagelse fremmer vores grundlæggende viden om genomregulering i rum og tid, og kunne have store implikationer i forståelsen af kræft og degeneration.
"Denne forskning fremhæver vigtigheden af den spatiotemporale kontrol af genomorganisationen for normal cellefunktion, og vi fortsætter med at definere principperne, der regulerer disse processer og deres indvirkning på kræft og degeneration, " sagde Dr Kaidi.
 Varme artikler
Varme artikler
-
 Biologisk alder forklarer variationen i reaktioner på stressKredit:Shutterstock Gør flugt- eller kampmekanismerne udløst af reaktioner på stress, falde med alderen? Og hvis ja, er der en forskel mellem biologisk og kronologisk aldring? Spørgsmål, som ny fo
Biologisk alder forklarer variationen i reaktioner på stressKredit:Shutterstock Gør flugt- eller kampmekanismerne udløst af reaktioner på stress, falde med alderen? Og hvis ja, er der en forskel mellem biologisk og kronologisk aldring? Spørgsmål, som ny fo -
 Ny undersøgelse belyser, hvordan de tidligste former for liv udviklede sig på JordenVentiler til undervandsopvarmning. Kredit:US National Oceanic and Atmospheric Administration En ny undersøgelse ledet af ANU har belyst, hvordan de tidligste former for liv udviklede sig på Jorden
Ny undersøgelse belyser, hvordan de tidligste former for liv udviklede sig på JordenVentiler til undervandsopvarmning. Kredit:US National Oceanic and Atmospheric Administration En ny undersøgelse ledet af ANU har belyst, hvordan de tidligste former for liv udviklede sig på Jorden -
 Freud og Ødipus:Er noget stadig vigtigt?Ødipus-komplekset er tanken om, at små børn oplever et ubevidst ønske om deres forælder af modsat køn og jalousi over for deres forældre af samme køn. Noel Hendrickson/Getty Images Historien har ikke
Freud og Ødipus:Er noget stadig vigtigt?Ødipus-komplekset er tanken om, at små børn oplever et ubevidst ønske om deres forælder af modsat køn og jalousi over for deres forældre af samme køn. Noel Hendrickson/Getty Images Historien har ikke -
 Forskere sigter mod at forbedre tarmsundheden hos husdyrRyan Arsenault (i midten), adjunkt i husdyr- og fødevarevidenskab, med medlemmer af hans forskerhold Casey Johnson (til venstre) og Bridget Aylward (til højre). Kredit:Evan Krape/ University of Delawa
Forskere sigter mod at forbedre tarmsundheden hos husdyrRyan Arsenault (i midten), adjunkt i husdyr- og fødevarevidenskab, med medlemmer af hans forskerhold Casey Johnson (til venstre) og Bridget Aylward (til højre). Kredit:Evan Krape/ University of Delawa
- Mens 2 storme truer Gulf Coast, beboerne forbereder sig på syndflod
- Ingeniører udvikler prototype af billige, engangs lungeinfektionsdetektor
- Space-aktiveret app til piloter tager til skyerne
- Smarte enheder kan snart bruge deres ejere som en batterikilde
- Udvidelse af temperaturområdet for lithium-ion-batterier
- Microban Toxicity


