Ny forståelse af, hvordan proteiner fungerer
Proteiner er essentielle molekylære maskiner, der udfører en bred vifte af funktioner i celler. De spiller afgørende roller i alt fra at katalysere kemiske reaktioner til at transportere molekyler og yde strukturel støtte. De præcise mekanismer, hvormed proteiner udfører deres opgaver, er dog forblevet uhåndgribelige, hvilket hindrer bestræbelser på at manipulere dem til terapeutiske formål.
Forskerholdet, ledet af biokemiker og professor i molekylær- og cellebiologi Jennifer Doudna - som er almindeligt kendt for sit banebrydende arbejde med CRISPR-Cas9 genredigeringsteknologi - brugte en teknik kaldet kryo-elektronmikroskopi (cryo-EM) til at fange detaljeret billeder af proteiner i aktion. Cryo-EM gør det muligt for forskere at visualisere biologiske molekyler i deres oprindelige tilstand uden behov for krystallisering eller andre invasive teknikker.
Ved at kombinere cryo-EM med beregningsmodellering og biokemiske assays opnåede forskerne højopløsningsindsigt i de dynamiske konformationelle ændringer, som proteiner gennemgår under deres funktionelle cyklusser. Denne forståelse er beslægtet med at fange en række snapshots, der afslører de indviklede bevægelser og interaktioner i et protein, når det udfører sin udpegede opgave.
"For mange proteiner kender vi strukturen, men vi ved ikke, hvordan de virker. Ved at fange disse dynamiske proteinbevægelser kan vi nu begynde at forstå, hvordan proteiner fungerer på det mest fundamentale niveau," forklarede Doudna i en erklæring.
Forskerne fokuserede specifikt på en klasse af proteiner kaldet RNA-guidede nukleaser, som er involveret i genredigering og -regulering. Ved hjælp af cryo-EM var de i stand til at observere, hvordan disse nukleaser genkender og binder sig til specifikke RNA-sekvenser, og derefter manipulere RNA'et på præcise måder for at udføre deres cellulære funktioner.
Denne detaljerede forståelse af proteindynamik og mekanismer har umiddelbare implikationer for design af nye lægemidler og terapier. Ved at dechifrere den indviklede molekylære koreografi af proteiner, kan videnskabsmænd nu rationelt konstruere dem til at forbedre deres gavnlige funktioner eller undertrykke deres skadelige aktiviteter. For eksempel kunne denne tilgang føre til udvikling af mere effektive proteinterapier, enzymer til industrielle anvendelser og diagnostiske værktøjer til sygdomme forårsaget af proteindysfunktion.
Undersøgelsens resultater, offentliggjort i tidsskriftet Nature, repræsenterer et stort skridt fremad i forståelsen af proteinfunktion og giver et kraftfuldt værktøjssæt til at manipulere disse molekylære maskiner til gavn for menneskers sundhed og bioteknologi.
Som konklusion har det gennembrud opnået af forskere ved UC Berkeley revolutioneret vores forståelse af proteindrift på molekylært niveau. Ved at visualisere proteindynamik og mekanismer ved hjælp af cryo-EM besidder forskerne nu viden og værktøjer til at designe og konstruere proteiner med skræddersyede egenskaber, hvilket åbner nye veje for terapeutiske interventioner og teknologiske innovationer.
 Varme artikler
Varme artikler
-
 Designerproteiner, der pakker genetisk materiale, kan hjælpe med at levere genterapiLevering af genetisk materiale er en central udfordring i genterapi. Kredit:Kstudio, CC BY Hvis du nogensinde har købt en ny iPhone, du har oplevet god emballage. Den måde låget langsomt adskille
Designerproteiner, der pakker genetisk materiale, kan hjælpe med at levere genterapiLevering af genetisk materiale er en central udfordring i genterapi. Kredit:Kstudio, CC BY Hvis du nogensinde har købt en ny iPhone, du har oplevet god emballage. Den måde låget langsomt adskille -
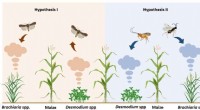 Hvordan push-pull ledsagende afgrøder hjælper med at håndtere den ødelæggende efterårshærormSkematisk repræsentation af et Push-Pull felt og forskningshypoteserne:(1) Ledsagende planteflygtige stoffer [Desmodium spp. mellemafgrøder (grønbladede desmodium, D. intortum eller sølvbladedesmodium
Hvordan push-pull ledsagende afgrøder hjælper med at håndtere den ødelæggende efterårshærormSkematisk repræsentation af et Push-Pull felt og forskningshypoteserne:(1) Ledsagende planteflygtige stoffer [Desmodium spp. mellemafgrøder (grønbladede desmodium, D. intortum eller sølvbladedesmodium -
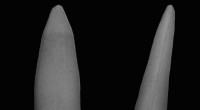 Savfiskfossiler tyder på, at tænder sandsynligvis er udviklet fra kropsskæl hos gamle fiskEn rostral dentikel af Ischyrhiza mia, en art, der tilhører en uddød gruppe af savfisk, der levede i nordamerikanske farvande i den sene kridtperiode for omkring 100 til 65 millioner år siden. Prøven
Savfiskfossiler tyder på, at tænder sandsynligvis er udviklet fra kropsskæl hos gamle fiskEn rostral dentikel af Ischyrhiza mia, en art, der tilhører en uddød gruppe af savfisk, der levede i nordamerikanske farvande i den sene kridtperiode for omkring 100 til 65 millioner år siden. Prøven -
 Hvad belysning af plantevækst kan betyde for kræftKredit:Pixabay/CC0 Public Domain At forstå, hvordan planter behandler lys, er nøglen til at forbedre afgrødeudbyttet. Lys hjælper planterne med at vide, hvornår de skal vokse og blomstre på det rig
Hvad belysning af plantevækst kan betyde for kræftKredit:Pixabay/CC0 Public Domain At forstå, hvordan planter behandler lys, er nøglen til at forbedre afgrødeudbyttet. Lys hjælper planterne med at vide, hvornår de skal vokse og blomstre på det rig
- NASA analyserer regnmængden fra orkanen Harveys, ser landfald
- Børn risikerer generationskatastrofe fra COVID:vagthund
- Bumperafgrøde af sorte huller i nyt gravitationsbølgepapir
- Forskere viser blænding af energiforbrug i deep learnings navn
- Hvilken slags indvirkning gør robotter på mennesker?
- Udåndede biomarkører kan afsløre lungesygdom


