Sådan beregnes galvaniseringstid:En trin-for-trin guide
Af Sean Mann | Opdateret 24. marts 2022
Elektroplettering belægger et ledende substrat med et tyndt metallag ved at drive ioner fra en elektrolyt gennem et elektrisk felt. Almindelig praksis i bilfremstilling af plader stål med kobber, nikkel og krom for at beskytte mod korrosion og vejrlig.
Trin 1:Identificer elektronbehovet
Undersøg halvreaktionen for at bestemme, hvor mange elektroner der er nødvendige for at afsætte et mol af målmetallet. For eksempel kræver deponering af kobber (Cu²⁺ → Cu) to elektroner pr. atom, dvs. to mol elektroner pr. mol kobber.
Trin 2:Beregn den samlede opladning
Den nødvendige ladning er givet af Faraday-ligningen:
Q = n(e) · F
hvor Q er ladningen i coulombs, n(e) er antallet af mol elektroner og F er Faraday-konstanten (96485 C mol⁻¹). Ved at bruge kobbereksemplet:
Q = 2 mol × 96485 C mol⁻¹ = 192970 C
Trin 3:Konverter opladning til tid
Den varighed, der kræves for at afsætte et mol metal ved en konstant strøm I følger:
t = Q / I
Med en 25-amp forsyning:
t = 192970 C / 25 A ≈ 7718 s ≈ 2,14 t
TL;DR
Du kan vende ligningerne om for at finde ud af, hvor meget metal der vil blive belagt for en given strøm og tid.
 Varme artikler
Varme artikler
-
 At forhindre 2020-kampagnens cyberangreb vil hverken være nemt eller billigtDenne 9. maj 2018, billedet viser en berøringsskærm af en stemmemaskine under tidlig afstemning i Sandy Springs, Ga. Hvorvidt kampagner har lært af cyberangrebene ved valget i 2016 er et kritisk spørg
At forhindre 2020-kampagnens cyberangreb vil hverken være nemt eller billigtDenne 9. maj 2018, billedet viser en berøringsskærm af en stemmemaskine under tidlig afstemning i Sandy Springs, Ga. Hvorvidt kampagner har lært af cyberangrebene ved valget i 2016 er et kritisk spørg -
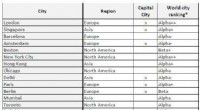 Top smarte byer er globale byer, ny forskning afslørerTabel 1. 27 byer i centrum af det globale smart city-netværk. Kredit:Joss et al. 2019 En hidtil uset global undersøgelse har analyseret og rangeret førende byer i det verdensomspændende smart city
Top smarte byer er globale byer, ny forskning afslørerTabel 1. 27 byer i centrum af det globale smart city-netværk. Kredit:Joss et al. 2019 En hidtil uset global undersøgelse har analyseret og rangeret førende byer i det verdensomspændende smart city -
 Hitachi flytter for at købe ABBs elnetenhed for 7 mia. USD:rapportAftalen ville gøre Hitachi til verdens næststørste producent af tungt elektrisk udstyr målt i omsætning Japanske Hitachi flytter for at købe den schweiziske ingeniørgigant ABBs elnetforretning for
Hitachi flytter for at købe ABBs elnetenhed for 7 mia. USD:rapportAftalen ville gøre Hitachi til verdens næststørste producent af tungt elektrisk udstyr målt i omsætning Japanske Hitachi flytter for at købe den schweiziske ingeniørgigant ABBs elnetforretning for -
 Opsamling af varme spildt i solpaneler til brug ved destillering af rent drikkevandUdsigterne for fremtidens PV-farm:ikke kun at generere elektricitet, men også producere ferskvand. Kredit:Wenbin Wang Et team af forskere ved King Abdullah University of Science and Technology har
Opsamling af varme spildt i solpaneler til brug ved destillering af rent drikkevandUdsigterne for fremtidens PV-farm:ikke kun at generere elektricitet, men også producere ferskvand. Kredit:Wenbin Wang Et team af forskere ved King Abdullah University of Science and Technology har
- Hvad er svaret på processen y, hvilke stof ændrer sig fra flydende gasstilstand?
- Hvornår landede de første mennesker på månen?
- Hvad er nogle moderne udviklinger inden for mikrobiologi?
- Hvilke typer sukker findes i DNA?
- Hvilken type organisme dværger alle andre med hensyn til artsdiversitet?
- COVID-19:Luftkvaliteten påvirker pandemien


