Forbedring af molekylær billeddannelse ved hjælp af en dyb læringstilgang
Kredit:Rensselaer Polytekniske Institut
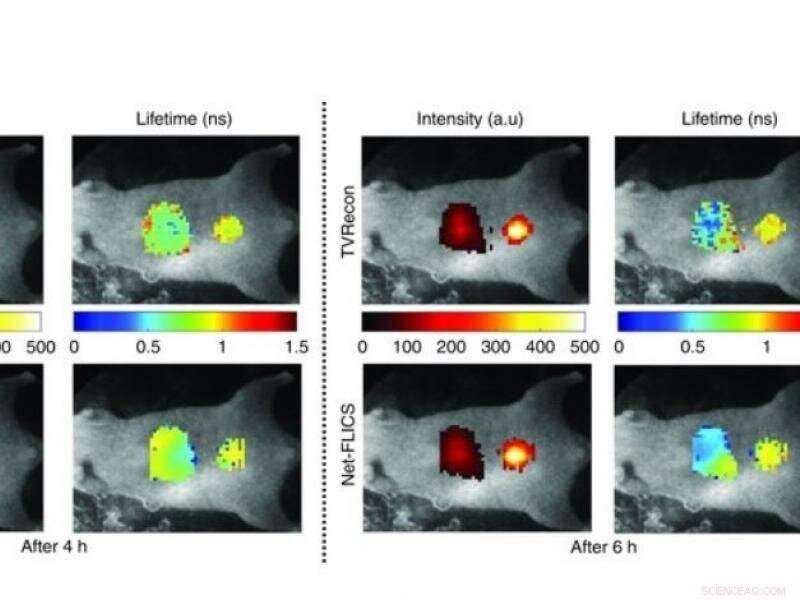
Generering af omfattende molekylære billeder af organer og tumorer i levende organismer kan udføres med ultrahurtig hastighed ved hjælp af en ny dyb læringstilgang til billedrekonstruktion udviklet af forskere ved Rensselaer Polytechnic Institute.
Forskerholdets nye teknik har potentialet til i høj grad at forbedre kvaliteten og hastigheden af billeddannelse i levende motiver og var i fokus for en artikel for nylig offentliggjort i Lys:Videnskab og applikationer , et naturtidsskrift.
Komprimeret sensing-baseret billeddannelse er en signalbehandlingsteknik, der kan bruges til at skabe billeder baseret på et begrænset sæt punktmålinger. For nylig, et forskerhold fra Rensselaer foreslog en ny instrumentel tilgang til at udnytte denne metode til at erhverve omfattende molekylære datasæt, som rapporteret i Naturfotonik . Mens denne tilgang gav mere komplette billeder, at behandle dataene og danne et billede kan tage timer.
Denne seneste metodologi udviklet hos Rensselaer bygger på det tidligere fremskridt og har potentialet til at producere billeder i realtid, samtidig med at kvaliteten og anvendeligheden af de producerede billeder forbedres. Dette kunne lette udviklingen af personaliserede lægemidler, forbedre klinisk diagnostik, eller identificere væv, der skal skæres ud.
Ud over at give et overordnet øjebliksbillede af det emne, der undersøges, herunder de organer eller tumorer, som forskere har målrettet visuelt ved hjælp af florescens, denne billeddannelsesproces kan afsløre information om den vellykkede intracellulære levering af lægemidler ved at måle nedbrydningshastigheden af fluorescensen.
For at muliggøre næsten realtidsvisualisering af molekylære hændelser, forskerholdet har udnyttet den seneste udvikling inden for kunstig intelligens. Den stærkt forbedrede billedrekonstruktion opnås ved hjælp af en dyb læringstilgang. Deep learning er et komplekst sæt algoritmer designet til at lære en computer at genkende og klassificere data. Specifikt, dette hold udviklede en foldet neural netværksarkitektur, som Rensselaer-forskerne kalder Net-FLICS, som står for fluorescence lifetime imaging med komprimeret sensing.
"Denne teknik er meget lovende for at få en mere præcis diagnose og behandling, " sagde Pingkun Yan, meddirektør for Biomedicinsk Imaging Center ved Rensselaer. "Denne teknologi kan hjælpe en læge med bedre at visualisere, hvor en tumor er og dens nøjagtige størrelse. De kan så præcist skære tumoren af i stedet for at skære en større del af og skåne de raske, normalt væv."
Yan udviklede denne tilgang sammen med den tilsvarende forfatter Xavier Intes, den anden meddirektør for Biomedical Imaging Center i Rensselaer, som er en del af Rensselaer Center for Bioteknologi og Tværfaglige Studier. Ph.d.-studerende Marien Ochoa og Ruoyang Yao støttede forskningen.
"I slutningen, målet er at oversætte disse til en klinisk setting. Normalt, når du har kliniske systemer, vil du gerne være så hurtig som muligt, " sagde Ochoa, da hun reflekterede over den hastighed, hvormed denne nye teknik gør det muligt for forskere at fange disse billeder.
Yderligere udvikling er påkrævet, før denne banebrydende nye teknologi kan bruges i et klinisk miljø. Imidlertid, dens fremskridt er blevet fremskyndet ved at inkorporere simulerede data baseret på modellering, en særlig specialitet for Intes og hans laboratorium.
"Til dyb læring har du normalt brug for en meget stor mængde data til træning, men for dette system har vi ikke den luksus endnu, fordi det er et meget nyt system, " sagde Yan.
Han sagde, at holdets forskning også viser, at modellering innovativt kan bruges til billeddannelse, præcist at udvide modellen til de reelle eksperimentelle data.
 Varme artikler
Varme artikler
-
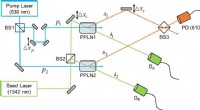 Eksperimentel bekræftelse af bølge-partikel dualitetTo SPDC krystaller, PPLN1 og PPLN2, pumpes og udsås samtidigt af den samme pumpe og frøkohærente lasere, henholdsvis, hvilket resulterer i emission af to signalfotoner s1 eller s2 til kvanteinterferen
Eksperimentel bekræftelse af bølge-partikel dualitetTo SPDC krystaller, PPLN1 og PPLN2, pumpes og udsås samtidigt af den samme pumpe og frøkohærente lasere, henholdsvis, hvilket resulterer i emission af to signalfotoner s1 eller s2 til kvanteinterferen -
 Ingeniører placerer enheder i molekyleskala i præcis orienteringForskere placerede mere end 3, 000 glødende måneformede nanoskala molekylære enheder til et blomsterformet instrument til indikering af lysets polarisering. Månerne i hvert af de 12 kronblade peger i
Ingeniører placerer enheder i molekyleskala i præcis orienteringForskere placerede mere end 3, 000 glødende måneformede nanoskala molekylære enheder til et blomsterformet instrument til indikering af lysets polarisering. Månerne i hvert af de 12 kronblade peger i -
 Ophidsede atomer kaster lys over anti-brint forskningEn positronstrålelinje transporterer positronerne fra kilden ind i hovedantibrintfælden. Kredit:Swansea University Swansea University-forskere, der arbejder ved CERN, har offentliggjort en undersø
Ophidsede atomer kaster lys over anti-brint forskningEn positronstrålelinje transporterer positronerne fra kilden ind i hovedantibrintfælden. Kredit:Swansea University Swansea University-forskere, der arbejder ved CERN, har offentliggjort en undersø -
 Vejrbestandig chip sigter mod at tage selvkørende teknologi, trådløs kommunikation til næste niv…Disse instrumenter i Ray Chens laboratorium blev brugt til at teste enheden. Kredit:University of Texas i Austin. Moderne kommunikationsteknologi, uanset brug, er afhængig af en lignende formel:en
Vejrbestandig chip sigter mod at tage selvkørende teknologi, trådløs kommunikation til næste niv…Disse instrumenter i Ray Chens laboratorium blev brugt til at teste enheden. Kredit:University of Texas i Austin. Moderne kommunikationsteknologi, uanset brug, er afhængig af en lignende formel:en
- Betydningen af fossiler
- Sådan finder du rektangelets længde og bredde, når området er angivet
- Matematiske spil, som du kan spille uden en Flash Player
- Opfindelser i 1947
- Svagt udbrud af en tiltagende millisekund røntgenpulsar observeret af astronomer
- Anvendelse af Goldilocks -princippet på DNA -struktur


