Forskere kontrollerer biofilmdannelse ved hjælp af optiske fælder
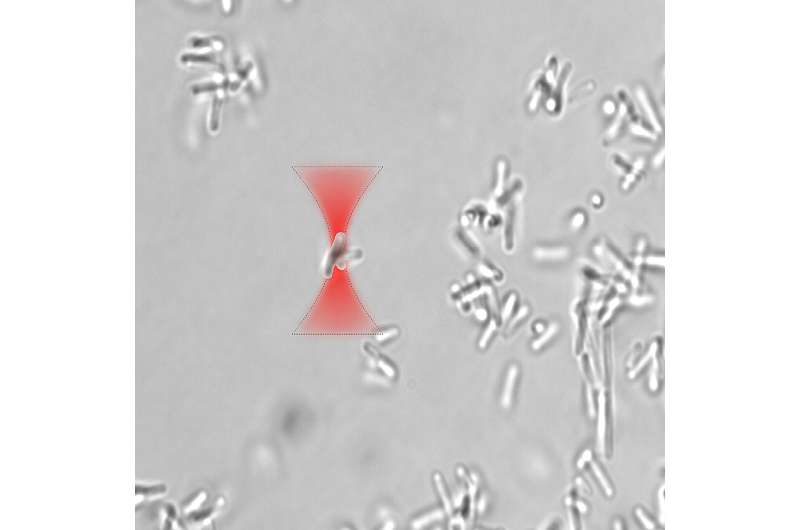
Biofilm - slimede lag, der dannes, når bakterier klæber sammen på en overflade - gør det muligt for bakterier at beskytte sig mod ekstreme miljøer og endda undgå antibiotika. I et nyt studie har forskere vist, at laserlys i form af optiske fælder kan bruges til at kontrollere biofilmdannelse. Resultaterne kunne gøre det muligt for forskere at udnytte disse mikrobielle lag til forskellige bioingeniørapplikationer.
"At producere mikroskopiske komponenter kræver normalt en meget teknisk fremstillingsproces, men vi fandt ud af, at en optisk pincet kan bruges til præcist at kontrollere placeringen af individuelle bakterier eller klynger af bakterier," siger leder af forskningsteamet Anna Bezryadina fra California State University Northridge. "Dette giver os mulighed for at påvirke vækstmønstrene for bakterielle strukturer på et mikroskopisk niveau med høj præcision."
I tidsskriftet Biomedical Optics Express , rapporterer forskerne deres eksperimenter med at bruge optiske fælder til at regulere bakteriel aggregering og udvikling af biofilm. De fandt ud af, at forskellige typer lasere kan bruges til at stimulere og undertrykke vækst af biofilm.
"Vi kan endda skabe en slags bakteriel legoklods, som kan flyttes rundt, sættes sammen og destrueres efter behov," sagde Bezryadina. "Dette arbejde kunne føre til nye typer bionedbrydelige materialer eller en ny generation af biofilm-baserede biosensorer, for eksempel."
Brug af lys til at kontrollere bakterievækst
Det meste biofilmforskning har fokuseret på mekaniske, kemiske og biologiske tilgange til at undertrykke og kontrollere biofilm. Selvom forskere har vist, at syntetiske og kemiske tilgange kan bruges til at aktivere og kontrollere biofilm og konstruere biofilm til specifikke rumlige strukturer, ønskede Bezryadina og hendes team at finde ud af, om optiske metoder kunne bruges til at kontrollere biofilmdynamik. For at opnå dette krævede det et tværfagligt team med ekspertise inden for avanceret optisk teknologi og mikrobiologi.
Forskerne eksperimenterede med Bacillus subtilis, en ikke-patogen bakterie, der naturligt danner biofilm. De brugte et miljø med lavt næringsindhold, der er fjendtligt over for B. subtilis, for at få bakterierne til at danne en biofilm. Efter at have opnået små biofilmklynger udførte de optiske fangsteksperimenter ved hjælp af enten en 473 nm blå laser eller en nær infrarød Ti:sapphire laser, der kunne indstilles fra 700 til 1000 nm.
De fandt ud af, at brug af en laser, der udsender ved en bølgelængde på 820 nm til 830 nm, muliggjorde langvarig optisk fangst af biofilmklynger, samtidig med at betydelig fotoskader blev minimeret. Men brugen af en laser ved 473 nm - en bølgelængde, der er stærkt absorberet af bakterierne - fik cellerne til at briste og biofilmklyngerne til at gå i opløsning. De observerede også, at de ideelle bakterieklynger til optisk manipulation bestod af tre til 15 celler.
Lav mønstre
Da forskerne studerede bakteriedynamik og biofilmdannelse ved hjælp af en optisk pincet ved 820 nm bølgelængde i en time, opdagede de, at bakterieklynger aggregerede nær optisk fangede klynger, klæbede til overfladen og begyndte at danne en mikrokoloni. De kunne også flytte optisk fangede bakterieklynger gennem prøven til en specifik position, hvilket kunne være nyttigt til at bygge strukturer ud af bakterier. NIR-laseren så ikke ud til at forstyrre biofilmdannelsen for bakterieklynger udsat for den højt fokuserede NIR-laser, hvilket indebærer, at NIR-bølgelængder i området 800 nm til 850 nm kunne bruges i længere perioder til optisk fangst, manipulation og mønsterdannelse af bakterieklynger.
"På trods af den tilsyneladende ukontrollerede bakterielle biofilmdannelse i naturen, viste vores arbejde, at bakteriel biofilmdannelse kan påvirkes af lys," sagde Bezryadina. "Dette papir repræsenterer det første skridt i det langsigtede projekt om at skabe mikroskopiske byggematerialer fra let tilgængelige ressourcer som bakterier. I fremtidige undersøgelser planlægger vi at bruge det, vi fandt, til at udvikle en proces til at konstruere strukturer fra bakterielle legoklodser."
Samlet set afslørede eksperimenterne en vis fleksibilitet i de nøjagtige vækstbetingelser, størrelser af klynger og bølgelængder, der er nødvendige for at manipulere biofilmene. Forskerne siger, at det måske også er muligt at bruge deres metodik med andre typer biofilmdannende mikroorganismer.
Flere oplysninger: Czarlyn Camba et al., Biofilmdannelse og manipulation med optisk pincet, Biomedicinsk Optics Express (2024). DOI:10.1364/BOE.510836
Journaloplysninger: Biomedicinsk Optics Express
Leveret af Optica
 Varme artikler
Varme artikler
-
 Forskere løser udfordringen med at forbedre fusionsydelsenSaskia Mordijck, en adjunkt i William &Marys fysikafdeling, ledet det multi-institutionelle forskerhold ved DIII-D National Fusion Facility, der udredede tre elementer i fusionsreaktionen. Deres arbej
Forskere løser udfordringen med at forbedre fusionsydelsenSaskia Mordijck, en adjunkt i William &Marys fysikafdeling, ledet det multi-institutionelle forskerhold ved DIII-D National Fusion Facility, der udredede tre elementer i fusionsreaktionen. Deres arbej -
 Spin-to-charge-konvertering opnår 95 % samlet qubit-udlæsningsnøjagtigheda) Energiniveauer brugt til at opnå SCC. b) Et skematisk diagram af SCC-udlæsning. c) excitationsspektret for nitrogen-tomrum (NV) centret anvendt her ved kryogen temperatur på 8 K K. d) Spin-flip-pro
Spin-to-charge-konvertering opnår 95 % samlet qubit-udlæsningsnøjagtigheda) Energiniveauer brugt til at opnå SCC. b) Et skematisk diagram af SCC-udlæsning. c) excitationsspektret for nitrogen-tomrum (NV) centret anvendt her ved kryogen temperatur på 8 K K. d) Spin-flip-pro -
 Forøgelse af optisk fiberkapacitet og kanaldatahastigheder i ubådskommunikationskablerKredit:CC0 Public Domain I bunden af Atlanterhavet ligger et væld af kabler, der bærer bundter af optiske fibre, der understøtter telekommunikation mellem kontinenter. MAREA -kablet betragtes so
Forøgelse af optisk fiberkapacitet og kanaldatahastigheder i ubådskommunikationskablerKredit:CC0 Public Domain I bunden af Atlanterhavet ligger et væld af kabler, der bærer bundter af optiske fibre, der understøtter telekommunikation mellem kontinenter. MAREA -kablet betragtes so -
 Sikker lysbaseret kommunikation gennem biologiske vævProfessor Marcos Katz team ved Uleåborgs universitet, Finland har for nylig demonstreret, hvordan lys kan bruges til at overføre data til og fra enheder i kroppen, såsom implantater. Synligt lysko
Sikker lysbaseret kommunikation gennem biologiske vævProfessor Marcos Katz team ved Uleåborgs universitet, Finland har for nylig demonstreret, hvordan lys kan bruges til at overføre data til og fra enheder i kroppen, såsom implantater. Synligt lysko
- Ny dual-resonans metode i 2-D materialer kan anspore fremskridt inden for fotonik
- Fungerer fleksibelt arbejde for australske forældre?
- En ny målerekord for det stærkeste magnetfelt i universet
- Surdej under mikroskop afslører mikrober, der er dyrket gennem generationer
- Celle på en chip afslører proteinadfærd
- Video:Sådan fungerer airbags


