Når en væske bevæger sig til gasformet tilstand, bærer den stor mængde varme?
* Ja, processen med en flydende, der skifter til en gas (fordampning) kræver en stor mængde varmeenergi. Dette skyldes, at molekylerne i et væske er nødt til at få nok energi til at bryde fri fra de attraktive kræfter, der holder dem sammen og bliver en gas. Denne energi absorberes fra omgivelserne, hvilket fører til en køleeffekt.
* Væsken selv ikke "bærer" denne varme. Varmen absorberes * under * faseændringen og bruges til at bryde bindingerne, der holder molekylerne sammen.
Her er en bedre måde at tænke over det på:
* Væsken * absorberer * varmeenergi under fordampning. Dette omtales som fordampningsvarmen .
* den resulterende gas * indeholder * mere energi end den originale væske. Dette skyldes, at molekylerne nu bevæger sig mere frit og har mere kinetisk energi.
Eksempler:
* kogende vand: Når vand koger, absorberer det varme fra ovnen eller det omgivende miljø. Denne absorberede energi bruges til at bryde brintbindingerne mellem vandmolekyler, hvilket giver dem mulighed for at flygte som damp. Dampen bærer derefter den absorberede varmeenergi væk.
* Fordampning: Selv ved stuetemperatur har nogle vandmolekyler nok energi til at bryde fri fra væsken og blive damp. Denne proces absorberer varme fra omgivelserne, hvorfor fordampning kan have en køleeffekt.
Kortfattet: Mens væsker ikke "bærer" varme, når de skifter til en gas, absorberer de en betydelig mængde varme under processen, som derefter indeholdes i gasmolekylerne.
Sidste artikelEr der noget hurtigere end lysets hastighed?
Næste artikelEr et magnetfelt omgivet af flytning af elektriske ladninger?
 Varme artikler
Varme artikler
-
 Genbesøger Clebschs tidlige artikler om strømmen af inkompressible væskerKredit:CC0 Public Domain Ny analyse af to nyligt oversatte artikler, første gang udgivet i 1850erne, vurderer de tidlige metoder brugt af Alfred Clebsch til at beskrive strømmen af inkompressibl
Genbesøger Clebschs tidlige artikler om strømmen af inkompressible væskerKredit:CC0 Public Domain Ny analyse af to nyligt oversatte artikler, første gang udgivet i 1850erne, vurderer de tidlige metoder brugt af Alfred Clebsch til at beskrive strømmen af inkompressibl -
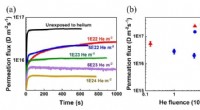 Foreksponering af helium hæmmer permeation af brintisotop i vægmaterialerFigur 1. (a) transiente penetrationskurver og (b) steady-state penetration. Kredit:Wang Lu Et forskerhold fra Hefei Institutes of Physical Science (HFIPS) fra det kinesiske videnskabsakademi (CAS)
Foreksponering af helium hæmmer permeation af brintisotop i vægmaterialerFigur 1. (a) transiente penetrationskurver og (b) steady-state penetration. Kredit:Wang Lu Et forskerhold fra Hefei Institutes of Physical Science (HFIPS) fra det kinesiske videnskabsakademi (CAS) -
 Undersøgelse af fanget ion-teknologi til næste generation af kvantecomputereIonQs fangede ionsystem. Kredit:Duke University, staq.pratt.duke.edu/ Kvantecomputere (QC) er klar til at drive vigtige fremskridt på flere domæner, herunder medicin, materialevidenskab og interne
Undersøgelse af fanget ion-teknologi til næste generation af kvantecomputereIonQs fangede ionsystem. Kredit:Duke University, staq.pratt.duke.edu/ Kvantecomputere (QC) er klar til at drive vigtige fremskridt på flere domæner, herunder medicin, materialevidenskab og interne -
 En interaktiv videnskabelig udstilling baseret på en virkelig gravitationsbølgedetektorMichelson-interferometeret installeret på Thinktank Birmingham Science Museum. Kredit:[billede leveret fra avisen] Gravitationsbølgeforskere har designet og bygget en interaktiv videnskabsudstilli
En interaktiv videnskabelig udstilling baseret på en virkelig gravitationsbølgedetektorMichelson-interferometeret installeret på Thinktank Birmingham Science Museum. Kredit:[billede leveret fra avisen] Gravitationsbølgeforskere har designet og bygget en interaktiv videnskabsudstilli
- Hvordan Saturns Atmosfære Sammenligner Med Jorden?
- Hvordan er en grad eller længdegrad yderligere opdelt?
- Hvor er den største U -formede dal i Europa?
- Hjælpere ved reden kan give moderfugle mulighed for at lægge mindre æg
- Klima forklaret:Hvordan hvide tage hjælper med at reflektere solens varme
- Indiens rigeste mand løfter sløret for bredbåndsplan


