Forskel mellem bevægelse af partikler i en fast og væske?
faste stoffer:
* Arrangement: Partikler er tæt pakket i et fast, regelmæssigt arrangement (krystallinsk struktur). Tænk på dem som pænt stablede appelsiner i en kasse.
* Bevægelse: Partikler vibrerer på plads, men de bevæger sig ikke frit forbi hinanden. Denne vibration øges med temperaturen, men partiklerne forbliver i deres faste positioner.
* Form og volumen: Faststoffer har en bestemt form og et bestemt volumen. De modstår ændringer i deres form.
væsker:
* Arrangement: Partikler er tættere sammen end i gasser, men de er ikke i et fast arrangement. Tænk på dem som kugler løst pakket i en taske.
* Bevægelse: Partikler kan bevæge sig forbi hinanden, glide og flyde. Denne bevægelse er mere energisk ved højere temperaturer.
* Form og volumen: Væsker har et bestemt volumen, men tag formen på deres beholder. De er mindre modstandsdygtige over for at forme ændringer end faste stoffer.
her er en simpel analogi:
* Forestil dig en mængde mennesker på en koncert:
* fast: Publikum står tæt pakket, alle er for det meste stationære, og der er lidt bevægelse undtagen for at svinge.
* væske: Publikum er stadig pakket sammen, men de bevæger sig og skifter rundt og flyder, mens de prøver at komme til scenen.
Key Takeaway: Den største forskel er bevægelsesfriheden. Partikler i faste stoffer er i det væsentlige låst på plads, mens partikler i væsker kan bevæge sig rundt i hinanden.
 Varme artikler
Varme artikler
-
 Ny undersøgelse undersøger fotonik til kunstig intelligens og neuromorfisk databehandlingKredit:CC0 Public Domain Forskere har givet en fascinerende ny indsigt i de næste skridt til at udvikle sig hurtigt, energieffektiv, fremtidige computersystemer, der bruger lys i stedet for elektr
Ny undersøgelse undersøger fotonik til kunstig intelligens og neuromorfisk databehandlingKredit:CC0 Public Domain Forskere har givet en fascinerende ny indsigt i de næste skridt til at udvikle sig hurtigt, energieffektiv, fremtidige computersystemer, der bruger lys i stedet for elektr -
 Udnyttelse af kaos kan hjælpe klimamodellering med at tage springet fremadKredit:CC0 Public Domain At forstå klimaets kaotiske variation og dets reaktion på klimaændringer kan hjælpe videnskabsmænd med bedre at forudsige ændringer, der stadig undslipper selv de mest sof
Udnyttelse af kaos kan hjælpe klimamodellering med at tage springet fremadKredit:CC0 Public Domain At forstå klimaets kaotiske variation og dets reaktion på klimaændringer kan hjælpe videnskabsmænd med bedre at forudsige ændringer, der stadig undslipper selv de mest sof -
 KITE-kode kunne drive nye kvanteudviklingerKredit:CC0 Public Domain Et forskningssamarbejde ledet af University of Yorks Department of Physics har skabt open source-software til at hjælpe med skabelsen af kvantematerialer, som igen kunne
KITE-kode kunne drive nye kvanteudviklingerKredit:CC0 Public Domain Et forskningssamarbejde ledet af University of Yorks Department of Physics har skabt open source-software til at hjælpe med skabelsen af kvantematerialer, som igen kunne -
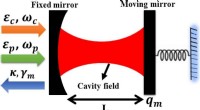 Langsom lys i et optisk hulrum med mekaniske resonatorer og spejleEt skematisk diagram af det positionsafhængige masseoptomekaniske system studeret i dette arbejde. Kredit:K Ullah og H Ullah Teoretiske fysikere Kamran Ullah og Hameed Ullah har vist, at et positi
Langsom lys i et optisk hulrum med mekaniske resonatorer og spejleEt skematisk diagram af det positionsafhængige masseoptomekaniske system studeret i dette arbejde. Kredit:K Ullah og H Ullah Teoretiske fysikere Kamran Ullah og Hameed Ullah har vist, at et positi
- Virkningerne af menneskelig aktivitet på carboncyklusen
- Simuleringer af, hvordan en virus pakker sit genetiske materiale, kan hjælpe med at designe nanocon…
- Vegan er den nye vegetar - hvorfor supermarkeder skal gå 'plantebaserede' og hjælpe med at redde p…
- Hvordan tusindårig nostalgi gav næring til succesen med 'Pokemon Go'
- Chokbølge fotograferet passerer gennem en enkelt celle med forbedret nanosekunds billedteknologi
- Hvordan virker lithium-ion-batterier?


