Hvordan arrangerede Dmitri Menedelyev elementer på hans første periodiske bord?
Her er en sammenbrud:
1. stigende atommasse: Han listede elementer i rækkefølge af stigende atommasse, startende med det letteste element, brint. Dette var det primære organiserende princip.
2. Lignende kemiske egenskaber: Han bemærkede tilbagevendende mønstre i elementernes kemiske egenskaber. Elementer med lignende egenskaber dukkede op med regelmæssige intervaller i hans bord.
3. Perioder og grupper: Mendeleev arrangerede elementer i rækker kaldet perioder og kolonner kaldet grupper . Elementer i den samme gruppe delte lignende kemiske egenskaber.
Det er vigtigt at bemærke, at Mendeleevs periodiske bord ikke var perfekt. Det havde nogle unøjagtigheder på grund af den begrænsede forståelse af atomstruktur på det tidspunkt. For eksempel placerede han Tellurium (TE) før jod (I), selvom jod har en lidt lavere atommasse. Dette var fordi han erkendte, at jod passede bedre i gruppe VII med de andre halogener baseret på dens kemiske egenskaber.
Nøglefunktioner i Mendeleevs periodiske tabel:
* forudsigelsesevne: Mendeleev forlod huller i sit bord for elementer, der endnu ikke skulle opdages. Han brugte de periodiske tendenser til at forudsige egenskaberne for disse uopdagede elementer.
* basis for moderne periodisk tabel: Mendeleevs bord lagde grundlaget for den moderne periodiske tabel, der er baseret på atomnummer i stedet for atommasse.
Hans innovative arbejde revolutionerede forståelsen af kemiske elementer og deres forhold og gav en ramme for fremtidige opdagelser inden for kemi.
Sidste artikelHvad er 17ft 34 konverteret til meter?
Næste artikelHvad er processen med at se et eksperiment og bemærke, hvad der sker?
 Varme artikler
Varme artikler
-
 Ultrahurtig magnetisk omskiftning med potentiale til at transformere fiberoptisk kommunikationKredit:Trinity College Dublin Forskere ved CRANN og Trinitys School of Physics har opdaget, at et nyt materiale kan fungere som en superhurtig magnetisk switch. Når den rammes af successive ultra
Ultrahurtig magnetisk omskiftning med potentiale til at transformere fiberoptisk kommunikationKredit:Trinity College Dublin Forskere ved CRANN og Trinitys School of Physics har opdaget, at et nyt materiale kan fungere som en superhurtig magnetisk switch. Når den rammes af successive ultra -
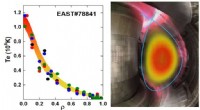 Kinesisk fusionsværktøj skubber forbi 100 millioner graderPlasmaelektrontemperaturen over 100 millioner grader opnået i 2018 på EAST. Kredit:EAST Team The Experimental Advanced Superconducting Tokamak (EAST), kaldet den kinesiske kunstige sol, opnåede e
Kinesisk fusionsværktøj skubber forbi 100 millioner graderPlasmaelektrontemperaturen over 100 millioner grader opnået i 2018 på EAST. Kredit:EAST Team The Experimental Advanced Superconducting Tokamak (EAST), kaldet den kinesiske kunstige sol, opnåede e -
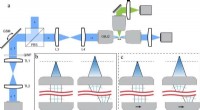 Konvertering af lateral scanning til aksial fokusering for at fremskynde 3D-mikroskopien, En kollimeret laserstråle leveres i opsætningen af en strålesplitter (BS) og på et galvanometrisk scanningsspejl (GSM), som er afbildet i det bageste fokalplan for et luftobjekt (OBJ1). Ved at s
Konvertering af lateral scanning til aksial fokusering for at fremskynde 3D-mikroskopien, En kollimeret laserstråle leveres i opsætningen af en strålesplitter (BS) og på et galvanometrisk scanningsspejl (GSM), som er afbildet i det bageste fokalplan for et luftobjekt (OBJ1). Ved at s -
 Forskere 3-D-printer små flerfarvede mikrostrukturerVed at justere antallet af lag af flerfarvede harpikser, forskerne kunne justere lysabsorbansen for hver del af en struktur. Dette gjorde det muligt for dem at skabe sort i mikrostrukturer som denne k
Forskere 3-D-printer små flerfarvede mikrostrukturerVed at justere antallet af lag af flerfarvede harpikser, forskerne kunne justere lysabsorbansen for hver del af en struktur. Dette gjorde det muligt for dem at skabe sort i mikrostrukturer som denne k
- Populær betyder ikke indflydelsesrig blandt cambodjanske landmænd
- Brug af kunstig intelligens til at generere 3D-hologrammer i realtid
- Løsning af spændinger på overfladen af polymerblandinger
- Hvad viste William Observation og eksperimenter?
- Hvad spiser Angelfish i naturen?
- Hvad er atomnummeret på CH4?


