Hvorfor krummer menisk af vand i glasskurver opad?
Her er en sammenbrud:
* samhørighed: Vandmolekyler har en stærk tiltrækning til hinanden på grund af hydrogenbinding. Denne styrke trækker dem sammen og skaber overfladespænding.
* Adhæsion: Vandmolekyler har også en tiltrækning til glasoverfladen. Denne styrke kaldes vedhæftning.
I tilfælde af vand og glas:
* Adhæsion er stærkere end samhørighed: Tiltrækningen mellem vandmolekyler og glasset er stærkere end tiltrækningen mellem vandmolekyler selv.
* konkave menisk: Denne stærkere vedhæftning trækker vandmolekylerne opad langs glasoverfladen og skaber en konkav menisk (buet opad).
Hvorfor sker dette?
Forestil dig vandmolekyler i kanten af vandsøjlen, der berører glasset. De trækkes op af glasset, men trukkes også sidelæns ved vandmolekylerne ved siden af dem.
* Fordi vedhæftning er stærkere, vinder den opadgående træk, hvilket resulterer i, at vandet klatrer op ad glasset.
* Dette skaber en konkav kurve på overfladen.
Kontrast med kviksølv:
På den anden side danner Mercury en konveks menisk (buet nedad). Dette skyldes, at de sammenhængende kræfter mellem kviksølvmolekyler er stærkere end de klæbende kræfter mellem kviksølv og glas.
Kortfattet:
Menisken af vandkurver opad på grund af de stærkere klæbemiddelkræfter mellem vand og glas og trækker vandmolekylerne opad langs glasoverfladen.
Sidste artikelEr faseændringer i materien permanent?
Næste artikelBiografi om Newton i 200 ord?
 Varme artikler
Varme artikler
-
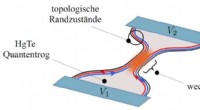 Topologisk nanoelektronikEn kvantebrønd indsnævres i midten til en kvantepunktkontakt. Würzburg -fysikere har produceret denne enhed ved hjælp af nye metoder til nanostrukturering. Kredit:Christoph Fleckenstein / University o
Topologisk nanoelektronikEn kvantebrønd indsnævres i midten til en kvantepunktkontakt. Würzburg -fysikere har produceret denne enhed ved hjælp af nye metoder til nanostrukturering. Kredit:Christoph Fleckenstein / University o -
 Første enkeltkrystal organometalliske perovskit optiske fibreSingle-Crystal Organometallic Perovskite Optisk Fiber. Kredit:Dr Lei Su På grund af deres meget høje effektivitet til at transportere elektriske ladninger fra lys, er perovskiter kendt som næste ge
Første enkeltkrystal organometalliske perovskit optiske fibreSingle-Crystal Organometallic Perovskite Optisk Fiber. Kredit:Dr Lei Su På grund af deres meget høje effektivitet til at transportere elektriske ladninger fra lys, er perovskiter kendt som næste ge -
 Hvordan Bali kunne lære verden at administrere sine begrænsede ressourcerKredit:Pixabay/CC0 Public Domain Vand er en begrænset ressource. Som sådan er effektive måder at administrere og optimere vandreserver på i fællesskab, afgørende for vores nutid og fremtid. Men hvo
Hvordan Bali kunne lære verden at administrere sine begrænsede ressourcerKredit:Pixabay/CC0 Public Domain Vand er en begrænset ressource. Som sådan er effektive måder at administrere og optimere vandreserver på i fællesskab, afgørende for vores nutid og fremtid. Men hvo -
 Forskere lokker til partikler til dannelse af hvirvler ved hjælp af magnetfelterForskere ved Argonne National Laboratory skabte små hvirvlende hvirvler ud af magnetiske partikler, giver indsigt i den adfærd, der styrer sådanne systemer - hvilket åbner nye muligheder for materiale
Forskere lokker til partikler til dannelse af hvirvler ved hjælp af magnetfelterForskere ved Argonne National Laboratory skabte små hvirvlende hvirvler ud af magnetiske partikler, giver indsigt i den adfærd, der styrer sådanne systemer - hvilket åbner nye muligheder for materiale
- Give Titan Saturn sin hældning?
- Nanoklynger organiserer sig selv i centimeterskala hierarkiske samlinger
- Kan der være liv på Jupiters måner?
- Ny undersøgelse viser producenter, hvor og hvordan man dyrker celluloseholdige biobrændstofafgrød…
- Forskere hævder, at alle højenergiske kosmiske neutrinoer er født af kvasarer
- Er helium godt for miljøet?


