Hvad skete der med antallet af valanceelektroner bevæger sig fra venstre højre ved periodisk tabel?
Her er hvorfor:
* valenselektroner er elektronerne i den yderste skal af et atom. Dette er de elektroner, der er involveret i kemisk binding.
* perioder På den periodiske tabel repræsenterer antallet af elektronskaller, et atom har.
* grupper (Kolonner) Repræsenterer antallet af valenselektroner, som et atom har.
Når du bevæger dig fra venstre mod højre over en periode:
1. Protoner i kernen øges: Dette øger atomets positive ladning.
2. Elektroner føjes til den samme skal: De tilsatte elektroner tiltrækkes af den øgede positive ladning af kernen.
3. Antallet af valenselektroner øges: Dette skyldes, at de nye elektroner føjes til den yderste skal, hvilket gør dem til valenselektroner.
Lad os for eksempel se på den anden periode:
* lithium (Li): 1 Valenselektron
* beryllium (BE): 2 valenselektroner
* bor (b): 3 Valenselektroner
* carbon (c): 4 valenselektroner
* nitrogen (n): 5 Valenselektroner
* ilt (O): 6 Valenselektroner
* fluor (F): 7 Valenselektroner
* neon (NE): 8 Valenselektroner (en fuld ydre skal)
Derfor øges antallet af valenselektroner, når du bevæger dig fra venstre til højre over det periodiske tabel, hvilket afspejler den stigende positive ladning af kernen og tilsætning af elektroner til den yderste skal.
Sidste artikelHvor mange meter er 60 tommer?
Næste artikelHvor mange inches er 100 meter?
 Varme artikler
Varme artikler
-
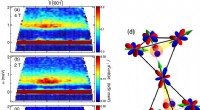 Omrøring af en kvante-spin-væske med uorden0 (venstre) nær absolut nul (temperatur). Variationen i intensitet med stigende magnetfelt (nedefra til top) indikerer, at en svag lidelse kan forhindre frysning af centrifugering og fremme en kvantes
Omrøring af en kvante-spin-væske med uorden0 (venstre) nær absolut nul (temperatur). Variationen i intensitet med stigende magnetfelt (nedefra til top) indikerer, at en svag lidelse kan forhindre frysning af centrifugering og fremme en kvantes -
 Maskinlæring baner vejen for smartere partikelacceleratorerStabsforsker Daniele Filippetto arbejder på elektronspredningsapparatet med høj gentagelseshastighed. Kredit:Thor Swift/Berkeley Lab Forskere har udviklet en ny maskinlæringsplatform, der gør de al
Maskinlæring baner vejen for smartere partikelacceleratorerStabsforsker Daniele Filippetto arbejder på elektronspredningsapparatet med høj gentagelseshastighed. Kredit:Thor Swift/Berkeley Lab Forskere har udviklet en ny maskinlæringsplatform, der gør de al -
 Små magneter afslører store hemmelighederIgor Barsukov er assisterende professor i fysik ved UC Riverside. Kredit:Barsukov lab, UC Riverside Et internationalt forskerhold ledet af en fysiker ved University of California, Riverside, har i
Små magneter afslører store hemmelighederIgor Barsukov er assisterende professor i fysik ved UC Riverside. Kredit:Barsukov lab, UC Riverside Et internationalt forskerhold ledet af en fysiker ved University of California, Riverside, har i -
 Elastiske dyser kunne skabe mere stabile væskestrålerKredit:Pixabay/CC0 Public Domain Indtil nu har der været lidt opmærksomhed på væskestrømmen gennem deformerbare elastiske dyser. Ny forskning offentliggjort i The European Physical Journal Special
Elastiske dyser kunne skabe mere stabile væskestrålerKredit:Pixabay/CC0 Public Domain Indtil nu har der været lidt opmærksomhed på væskestrømmen gennem deformerbare elastiske dyser. Ny forskning offentliggjort i The European Physical Journal Special
- Hvor grønt er miljøvenligt fyrværkeri?
- Partikler fanget i snoede materialer og identificerede kvantefingeraftryk
- Online kirke:Ministerier bruger VR, apps til at levere digitale tjenester og virtuelle dåb
- Hvad ville der ske, hvis en solstorm ramte Jorden?
- Køretøjsbremser producerer ladede partikler, der kan skade folkesundheden, siger undersøgelse
- eBays nye Managed Delivery har til formål at konkurrere med Amazon


