Hvad ville der ske med mængden af en ballon, hvis trykket steg?
* Boyle's lov: Denne grundlæggende gaslov siger, at volumen af en gas er omvendt proportional med dens tryk under forudsætning af konstant temperatur. Dette betyder, at når trykket øges, falder volumenet, og vice versa.
* ballondynamik: Balloner er i det væsentlige fleksible containere fyldt med luft. Når trykket inde i ballonen øges, kolliderer luftmolekylerne hyppigere og med større kraft mod ballonens indre overflade. Denne ydre kraft strækker ballonmaterialet og får ballonen til at udvide sig. Imidlertid komprimerer det øgede tryk også luften indeni, hvilket fører til et fald i volumen.
I resuméet ville stigningen i tryk resultere i en mindre ballon.
Vigtig note: Dette forhold gælder, så længe temperaturen forbliver konstant. Hvis temperaturen stiger, kan volumenet stige på trods af trykforøgelsen, da gasmolekylerne bevæger sig hurtigere og udøver mere kraft på ballonen.
Sidste artikelHvad betyder stivhed?
Næste artikelHvordan er et spektrofotometer kalibreret?
 Varme artikler
Varme artikler
-
 Jagt mørk energi med gravitationsresonansspektroskopiKredit:CC0 Public Domain Mørk energi menes i vid udstrækning at være drivkraften bag universets accelererende ekspansion, og flere teorier er nu blevet foreslået for at forklare dens undvigende na
Jagt mørk energi med gravitationsresonansspektroskopiKredit:CC0 Public Domain Mørk energi menes i vid udstrækning at være drivkraften bag universets accelererende ekspansion, og flere teorier er nu blevet foreslået for at forklare dens undvigende na -
 Så meget pres som Uranus-kernen:Den første forskning og undersøgelse af materialesyntese i terapa…Strukturer og egenskaber af materialer ved ekstremt høje tryk og temperaturer er stadig stort set terra incognita. Prof. Leonid Dubrovinsky og hans forskningspartnere bruger en laseropvarmet to-trins
Så meget pres som Uranus-kernen:Den første forskning og undersøgelse af materialesyntese i terapa…Strukturer og egenskaber af materialer ved ekstremt høje tryk og temperaturer er stadig stort set terra incognita. Prof. Leonid Dubrovinsky og hans forskningspartnere bruger en laseropvarmet to-trins -
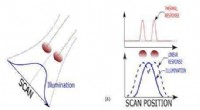 Superopløsning på alle skalaer med aktiv termisk detektionScanningsbelysning, termisk respons og superopløsningsfaktor. (a) To objekter belyses af en scanningsfokuseret energikilde med en størrelse større end objekterne eller afstanden mellem dem. (b) Den te
Superopløsning på alle skalaer med aktiv termisk detektionScanningsbelysning, termisk respons og superopløsningsfaktor. (a) To objekter belyses af en scanningsfokuseret energikilde med en størrelse større end objekterne eller afstanden mellem dem. (b) Den te -
 Random access memory på en lavenergidiæt:Forskere udvikler grundlag for en ny hukommelseschipPrototypen af en antiferromagnetisk magnetoelektrisk hukommelseschip, som blev opfundet af forskere fra Dresden og Basel. Den består af et tyndt lag chromoxid (Cr2O3) til lagring af data, ovenpå fas
Random access memory på en lavenergidiæt:Forskere udvikler grundlag for en ny hukommelseschipPrototypen af en antiferromagnetisk magnetoelektrisk hukommelseschip, som blev opfundet af forskere fra Dresden og Basel. Den består af et tyndt lag chromoxid (Cr2O3) til lagring af data, ovenpå fas
- Dekarbonisering af energiforsyningen ved at bruge samfundskraft
- Hvad er det tredje trin i jorddannelse?
- En større fremtid:Forskere siger, at rekorder vil blive slået
- Elektronisk handske tilbyder menneskelignende funktioner til brugere af håndproteser
- Eksperimenter viser, at kanter ikke er nødvendige for at realisere en usædvanlig kvanteeffekt
- Smeltende glas fra usmeltelige forbindelser


