Hvordan ændrer opvarmning af en gas i stiv beholder sit tryk?
* kinetisk molekylær teori: Den kinetiske molekylære teori om gasser siger, at gasmolekyler konstant er i tilfældig bevægelse og kolliderer med hinanden og væggene i deres beholder. Jo højere temperatur, jo hurtigere bevæger disse molekyler sig.
* øgede kollisioner: Når gasmolekylerne bevæger sig hurtigere, kolliderer de hyppigere med containerens vægge og med større kraft.
* trykdefinition: Tryk er defineret som den kraft, der udøves pr. Enhedsareal. Da kollisionerne er hyppigere og kraftfulde, øges trykket inde i beholderen.
Tænk på det på denne måde: Forestil dig en flok små kugler, der hopper rundt i en kasse. Hvis du opvarmer kassen, bevæger kuglerne sig hurtigere og rammer kassens vægge oftere og med mere kraft, hvilket skaber mere pres inde i boksen.
Vigtig note: Denne forklaring antager, at beholderen er virkelig stiv, og dens volumen forbliver konstant. Hvis beholderen kunne udvide, ville noget af det øgede tryk lettes af beholderen, der ekspanderer.
Sidste artikelDen ændring, der ikke er en fysisk, er?
Næste artikelHvad er de grundlæggende videnskabsprocesser?
 Varme artikler
Varme artikler
-
 Forskere bekræfter et nyt magisk tal for neutronerKredit:CC0 Public Domain Et internationalt samarbejde ledet af forskere fra University of Hong Kong, RIKEN (Japan), og CEA (Frankrig) har brugt RI Beam Factory (RIBF) ved RIKEN Nishina Center for
Forskere bekræfter et nyt magisk tal for neutronerKredit:CC0 Public Domain Et internationalt samarbejde ledet af forskere fra University of Hong Kong, RIKEN (Japan), og CEA (Frankrig) har brugt RI Beam Factory (RIBF) ved RIKEN Nishina Center for -
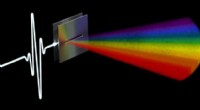 Forskere løser linkopdagelsesproblem for terahertz-datanetværkStråling af varierende frekvenser udgår fra en utæt bølgeleder i forskellige vinkler. Denne regnbue af frekvenser er grundlaget for et linkopdagelsessystem til fremtidige terahertz-datanetværk. Kredit
Forskere løser linkopdagelsesproblem for terahertz-datanetværkStråling af varierende frekvenser udgår fra en utæt bølgeleder i forskellige vinkler. Denne regnbue af frekvenser er grundlaget for et linkopdagelsessystem til fremtidige terahertz-datanetværk. Kredit -
 Computational modellering afslører anatomisk fordeling af træk på downhill skiløbereKredit:Mitch Gunn/Shutterstock Minimering af luftmodstand og friktion med sne er nøglen til elitepræstationer i alpint skiløb. Eksperimenter i vindtunneller har afsløret det samlede træk, skiløber
Computational modellering afslører anatomisk fordeling af træk på downhill skiløbereKredit:Mitch Gunn/Shutterstock Minimering af luftmodstand og friktion med sne er nøglen til elitepræstationer i alpint skiløb. Eksperimenter i vindtunneller har afsløret det samlede træk, skiløber -
 Hvordan COVID-19 hosteskyer rejser i nærvær og fravær af ansigtsmasker:undersøgelseVolumen af hostesky, der genereres af et menneske, stiger med tiden på grund af, at den omgivende luft trækkes ind i den (nederst). Ændring i skyens volumen som funktion af afstanden fra munden (øve
Hvordan COVID-19 hosteskyer rejser i nærvær og fravær af ansigtsmasker:undersøgelseVolumen af hostesky, der genereres af et menneske, stiger med tiden på grund af, at den omgivende luft trækkes ind i den (nederst). Ændring i skyens volumen som funktion af afstanden fra munden (øve
- Stort nyt palæoklimatologisk studie viser, at den globale opvarmning er steget 6, 500 års afkølin…
- Rollen af tidsmæssige udsving for swingfølelsen i jazzmusik
- Forskere indser lydløs foton-ekko-protokol
- Den amerikanske Fed ser beskeden vækst trods udbredt handelsangst
- Regnskovens reaktion på deglaciation påvirket af australske indfødte befolkninger, viser undersø…
- NASA analyserer Kammuris kraftige nedbør


