Hvor hurtigt spreder ting sig i væsker sammenlignet med gasser?
* Partikeltæthed: Væsker har meget højere partikeltætheder end gasser. Molekylerne er pakket meget tættere sammen.
* Intermolekylære kræfter: Væsker har stærkere intermolekylære kræfter (attraktioner mellem molekyler) end gasser. Disse kræfter holder molekylerne sammen og hindrer deres bevægelse og spredning.
* diffusion: Diffusion er processen med at sprede sig på grund af tilfældig bevægelse. I gasser kan molekyler rejse meget længere mellem kollisioner på grund af svagere intermolekylære kræfter og større afstand. I væsker er kollisioner hyppigere, hvilket bremser diffusionsprocessen.
Eksempler:
* lugt: En stærk lugt fra en gas spreder sig hurtigt over et rum. En væske med en stærk duft vil tage meget længere tid at diffundere og blive mærkbar.
* farvestof: En dråbe farvestof placeret i et glas vand vil langsomt sprede sig og tage sig tid til at farve hele volumenet. I en luftcontainer ville det samme farvestof sprede sig meget hurtigere.
Undtagelser:
Mens den generelle regel er, at spredning er langsommere i væsker, er der undtagelser:
* Temperatur: Højere temperaturer øger molekylær bevægelse og accelererer diffusion i både væsker og gasser.
* omrøring: Mekanisk blanding kan dramatisk fremskynde spredningen af stoffer i væsker.
Sammenfattende på grund af deres tættere pakning og stærkere intermolekylære kræfter spreder ting generelt meget langsommere i væsker end i gasser.
Sidste artikelHvilke af love forklarer konceptets tyngdekraft?
Næste artikelHvor hurtigt er en Megahertz?
 Varme artikler
Varme artikler
-
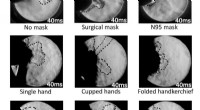 Effektiviteten af stofmasker afhænger af typen af belægningSchlieren billeder af hoste med forskellige grader af ansigtsdækning. Kredit:Padmanabha Prasanna Simha, Indiske rumforskningsorganisation Måneder inde i COVID-19-pandemien, at bære en maske, mens
Effektiviteten af stofmasker afhænger af typen af belægningSchlieren billeder af hoste med forskellige grader af ansigtsdækning. Kredit:Padmanabha Prasanna Simha, Indiske rumforskningsorganisation Måneder inde i COVID-19-pandemien, at bære en maske, mens -
 Bakterier ved, hvordan de udnytter kvantemekanik, undersøgelse finderEn gruppe forskere ved University of Chicago opdagede, at visse bakterier bevidst bruger kvantemekanikkens regler til at redde deres fotosyntetiske udstyr fra skader ved ilt. Kredit:Greg Engel Fot
Bakterier ved, hvordan de udnytter kvantemekanik, undersøgelse finderEn gruppe forskere ved University of Chicago opdagede, at visse bakterier bevidst bruger kvantemekanikkens regler til at redde deres fotosyntetiske udstyr fra skader ved ilt. Kredit:Greg Engel Fot -
 Intet bevis for påvirkning af mørkt stof på kraften mellem kernerHD+ molekylære ioner (gule og røde prikkerpar:proton og deuteron; elektronen er ikke vist) suspenderet i et ultrahøjt vakuum mellem atomære ioner (blå prikker), som er immobiliseret ved hjælp af en la
Intet bevis for påvirkning af mørkt stof på kraften mellem kernerHD+ molekylære ioner (gule og røde prikkerpar:proton og deuteron; elektronen er ikke vist) suspenderet i et ultrahøjt vakuum mellem atomære ioner (blå prikker), som er immobiliseret ved hjælp af en la -
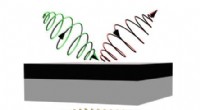 Fysikere mestrer uudforsket elektronegenskabSkematisk viser kontrol af dalens egenskaber i 2-D halvledere indlejret i mikrohulrum. Kredit:Zheng Sun Mens ladnings- og centrifugeringsegenskaberne for elektroner er meget udbredt i moderne tekn
Fysikere mestrer uudforsket elektronegenskabSkematisk viser kontrol af dalens egenskaber i 2-D halvledere indlejret i mikrohulrum. Kredit:Zheng Sun Mens ladnings- og centrifugeringsegenskaberne for elektroner er meget udbredt i moderne tekn
- Svamperesistens i planter forbundet med arvelige forskelle i mikrobiota-overflod
- Kan du høre mig nu? Hvordan det indre øres sensorer er lavet
- Er frysepunktets fysiske egenskab en ændring kemisk eller ændring?
- Øjeblikkelig vandrensningsmetode millioner af gange bedre end kommerciel tilgang
- Hvorfor ser vi en fuldmåne hver aften?
- Somalisk-amerikanske Amazon-arbejdere kræver bedre forhold


