Hvad sker der med virkelige gasser, når de når absolut nul?
* kvantemekanik: Ved absolut nul forudsiger klassisk fysik, at al molekylær bevægelse ville ophøre. Imidlertid dikterer kvantemekanik, at selv ved absolut nul har partikler stadig et minimumsmængde energi kaldet "nulpunktsenergi". Denne energi forhindrer, at molekyler nogensinde virkelig bliver helt bevægelige.
* faseovergange: Før de når absolut nul, ville reelle gasser overgå til en væske eller endda en fast tilstand. Den specifikke temperatur, hvorpå dette sker, afhænger af gassen og dens tryk.
* Eksperimentelle begrænsninger: At nå absolut nul er eksperimentelt umuligt. Vi kan komme ekstremt tæt (inden for et par millioner af en grad), men den energi, der kræves for at fjerne den sidste lille mængde varme, bliver uoverkommeligt stor.
Hvad sker der teoretisk:
Hvis vi hypotetisk kunne nå absolut nul med en rigtig gas, kan der forekomme flere ting:
* Nulvolumen: Klassisk ville gasmolekylerne have nul kinetisk energi og dermed nulvolumen. Dette er imidlertid ikke fysisk realistisk på grund af kvanteeffekter.
* Perfekt ordre: Molekylerne ville være i deres lavest mulige energitilstand og perfekt ordnet. Dette ville være en meget usandsynlig og ustabil tilstand.
Kortfattet:
Selvom vi ikke kan eksperimentelt nå absolut nul med reelle gasser, er det vigtigt at forstå, at konceptet styres af kvantemekanik, og at det at nå denne temperatur ville resultere i teoretiske, men ikke fysisk opnåelige scenarier.
 Varme artikler
Varme artikler
-
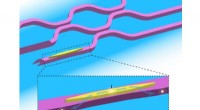 Ny arkitektur kan vise sig at være afgørende for højtydende kvantefotoniske kredsløbArkitekturen i dette hybrid kvantefotoniske kredsløb er blandt de første, der på en enkelt chip kombinerede en pålidelig generator af individuelle fotoner - en kvantepunkt (rød prik), her indlejret i
Ny arkitektur kan vise sig at være afgørende for højtydende kvantefotoniske kredsløbArkitekturen i dette hybrid kvantefotoniske kredsløb er blandt de første, der på en enkelt chip kombinerede en pålidelig generator af individuelle fotoner - en kvantepunkt (rød prik), her indlejret i -
 Mere end en ujævn tur:Turbulens giver fugle et boostKredit:Piotr Siedlecki/public domain De fleste fornuftige flyrejsende frygter turbulens. Et lille atmosfærisk hikke kan ryste fly, rasle nerver og spilde drikkevarer. En undersøgelse ledet af Corn
Mere end en ujævn tur:Turbulens giver fugle et boostKredit:Piotr Siedlecki/public domain De fleste fornuftige flyrejsende frygter turbulens. Et lille atmosfærisk hikke kan ryste fly, rasle nerver og spilde drikkevarer. En undersøgelse ledet af Corn -
 Papir afslører teorien bag ALPHA antihydrogen -gennembrudALPHA -teamet på ALPHA -anlægget, CERN. Kredit:CERN Ny forskning af et team fra Aarhus, Swansea, og Purdue Universities har gjort det muligt for nylige eksperimenter at foretage den første måling
Papir afslører teorien bag ALPHA antihydrogen -gennembrudALPHA -teamet på ALPHA -anlægget, CERN. Kredit:CERN Ny forskning af et team fra Aarhus, Swansea, og Purdue Universities har gjort det muligt for nylige eksperimenter at foretage den første måling -
 Nye soliton laserpulser leverer høj energi på en billionion af et sekundDr. Antoine Runge i et laboratorium på School of Physics ved University of Sydney. Kredit:Louise Cooper/University of Sydney Forskere har udviklet en ny type laser, der kan levere store mængder en
Nye soliton laserpulser leverer høj energi på en billionion af et sekundDr. Antoine Runge i et laboratorium på School of Physics ved University of Sydney. Kredit:Louise Cooper/University of Sydney Forskere har udviklet en ny type laser, der kan levere store mængder en
- hvorfor findes økosystemer ikke i nepa?
- Hvor findes alluvial jord i Indien?
- Ramme til at spore individuelle kulstofatomers vej
- Hvor ender dine online shopping returneringer? I skraldespanden, finder ny forskning
- Hvem formulerede den elektromagnetiske bølgeteori?
- Ultratynde kvantelyskilder:Forskere viser excitoniske interaktioner, der øger effektiviteten af s…


