Hvad er drivkraften for strømning af elektroner i batertries?
Her er en sammenbrud:
* Elektrokemisk potentiale: Hver elektrode i et batteri har et specifikt elektrokemisk potentiale, som er et mål for dens tendens til at vinde eller miste elektroner.
* spænding: Forskellen i elektrokemisk potentiale mellem de to elektroder skaber en spænding, der driver strømmen af elektroner.
* Elektronstrøm: Elektroner strømmer naturligvis fra et område med højere potentiale til et område med lavere potentiale. I et batteri betyder det, at elektroner strømmer fra den negative elektrode (anode) til den positive elektrode (katode).
* Kemiske reaktioner: Strømmen af elektroner er drevet af kemiske reaktioner, der forekommer ved elektroderne. Disse reaktioner involverer oxidation af anoden (tab af elektroner) og reduktion af katoden (forstærkning af elektroner).
Kortfattet: Forskellen i elektrokemisk potentiale eller spænding mellem de to elektroder skaber drivkraften for elektroner til at strømme fra anoden til katoden, hvilket driver enheden tilsluttet batteriet.
 Varme artikler
Varme artikler
-
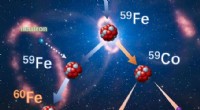 Undersøgelse kaster lys over stjernernes oprindelse af jernnuklider60 Fe-nukleosyntese i massive stjerner. Kredit:LI Yutian Forskere fra Institute of Modern Physics (IMP) ved det kinesiske videnskabsakademi og deres samarbejdspartnere har for nylig gjort store f
Undersøgelse kaster lys over stjernernes oprindelse af jernnuklider60 Fe-nukleosyntese i massive stjerner. Kredit:LI Yutian Forskere fra Institute of Modern Physics (IMP) ved det kinesiske videnskabsakademi og deres samarbejdspartnere har for nylig gjort store f -
 Nye forbindelser mellem kvanteberegning og maskinlæring i beregningskemiKredit:CC0 Public Domain Quantum computing lover at forbedre vores evne til at udføre nogle kritiske beregningsopgaver i fremtiden. Maskinlæring ændrer den måde, vi bruger computere på i vores nuv
Nye forbindelser mellem kvanteberegning og maskinlæring i beregningskemiKredit:CC0 Public Domain Quantum computing lover at forbedre vores evne til at udføre nogle kritiske beregningsopgaver i fremtiden. Maskinlæring ændrer den måde, vi bruger computere på i vores nuv -
 Søger efter manglende antistof:En vellykket start på målinger med Belle IIModel af Belle II-detektoren:Elektroner og deres antipartikler, positronerne, accelereres i SuperKEKB-ringen og støder sammen i Belle IIs kerne. Kredit:KEK/Belle II Siden 25. marts har 2019, Belle
Søger efter manglende antistof:En vellykket start på målinger med Belle IIModel af Belle II-detektoren:Elektroner og deres antipartikler, positronerne, accelereres i SuperKEKB-ringen og støder sammen i Belle IIs kerne. Kredit:KEK/Belle II Siden 25. marts har 2019, Belle -
 Et 3-D-kamera til sikrere autonomi og avanceret biomedicinsk billeddannelseI denne nye metode, genstande i forskellig afstand fra objektivet vil komme i fokus på forskellige punkter inde i kameraet. Kredit:Stephen Alvey, University of Michigan Forskere har demonstreret b
Et 3-D-kamera til sikrere autonomi og avanceret biomedicinsk billeddannelseI denne nye metode, genstande i forskellig afstand fra objektivet vil komme i fokus på forskellige punkter inde i kameraet. Kredit:Stephen Alvey, University of Michigan Forskere har demonstreret b
- Kortlivede lyskilder opdaget på himlen
- Den globale appelsinjuicekrise er forårsaget af sygdom og dårligt vejr:Sådan holder du det på mo…
- Hvilken gas er brændstoffet til en rød gigantisk stjerne?
- Dyserig brandmand er en robot, ligner en drage
- Hvordan bruges lydenergi til at producere og transmitteret?
- Tests viser lys fremtid for gadonanorør i stamcellesporing


