Hvad er en ændring af staten?
* fast: Har en fast form og volumen.
* væske: Har et fast volumen, men tager formen på sin beholder.
* gas: Har ingen fast form eller volumen og udvides til at fylde sin beholder.
Her er nogle almindelige eksempler på statsændringer:
* smeltning: Fast til væske (f.eks. Is, der smelter i vandet)
* Frysning: Væske til fast (f.eks. Vandfrysning i is)
* fordampning: Væske til gas (f.eks. Vandkogning i damp)
* kondens: Gas til væske (f.eks. Dampkondensering i vanddråber)
* sublimering: Fast til gas (f.eks. Tøris, der sublimerer til kuldioxidgas)
* afsætning: Gas til fast (f.eks. Frost, der dannes på en kold overflade)
Nøglepunkter om statsændringer:
* Energi er involveret: Statsændringer kræver enten absorption eller frigivelse af energi.
* endotermiske processer: Kræv energiindgang (smeltning, fordampning, sublimering).
* eksotermiske processer: Slip energi (frysning, kondens, afsætning).
* temperatur forbliver konstant: Under en tilstandsskift forbliver stoffet konstant konstant, selvom energi tilføjes eller fjernes.
* Fasediagrammer: Disse diagrammer illustrerer betingelserne (temperatur og tryk), hvor forskellige stoftilstande findes, og hvordan de overgår.
At forstå statsændringer er afgørende inden for forskellige områder, herunder:
* Kemi: Reaktioner kan involvere statsændringer, der påvirker deres satser og udbytter.
* meteorologi: Vejrmønstre er stærkt påvirket af tilstandsændringer, som dannelse af skyer og nedbør.
* teknik: Mange industrielle processer, som destillation og køling, er afhængige af statsændringer.
Fortæl mig, hvis du gerne vil have flere detaljer om en bestemt tilstandsændring eller relaterede koncepter!
 Varme artikler
Varme artikler
-
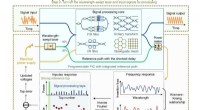 Verdens første selvkalibrerede fotoniske chip:En udveksling for optiske datamotorvejeKonceptuelt diagram af den selvkalibrerende integrerede bredbånds-PIC. Kredit:Xingyuan Xu et al., Nature Photonics (2022). DOI:10.1038/s41566-022-01020-z Forskning ledet af Monash og RMIT Universit
Verdens første selvkalibrerede fotoniske chip:En udveksling for optiske datamotorvejeKonceptuelt diagram af den selvkalibrerende integrerede bredbånds-PIC. Kredit:Xingyuan Xu et al., Nature Photonics (2022). DOI:10.1038/s41566-022-01020-z Forskning ledet af Monash og RMIT Universit -
 Værktøj lavet af lys:Nobelvindende laservidenskab, forklaretGerard Mourou fra Frankrig var en af tre forskere, der vandt 2018 Nobels fysikpris for opfindelser inden for laserfysik Efter at tre forskere tirsdag vandt Nobelprisen i fysik for banebrydende o
Værktøj lavet af lys:Nobelvindende laservidenskab, forklaretGerard Mourou fra Frankrig var en af tre forskere, der vandt 2018 Nobels fysikpris for opfindelser inden for laserfysik Efter at tre forskere tirsdag vandt Nobelprisen i fysik for banebrydende o -
 Vi har skabt en enhed, der kunne tillade øjeblikkelig sygdomsdiagnose, mens den passer ind i din te…Kredit:Shutterstock Infektionssygdomme som malaria er fortsat en førende dødsårsag i mange regioner. Dette skyldes til dels, at folk der ikke har adgang til medicinske diagnostiske værktøjer, der k
Vi har skabt en enhed, der kunne tillade øjeblikkelig sygdomsdiagnose, mens den passer ind i din te…Kredit:Shutterstock Infektionssygdomme som malaria er fortsat en førende dødsårsag i mange regioner. Dette skyldes til dels, at folk der ikke har adgang til medicinske diagnostiske værktøjer, der k -
 Fjernbetjening af varme nanokilder bevægelse og termisk inducerede væskestrømme ved hjælp af lys…en, Flere guld-NPer (kugler med en radius på 200 nm) er begrænset af en ringformet laserfælde (bølgelængde på 532 nm) og transporteres optisk omkring den. Disse NPer samles hurtigt til en stabil grupp
Fjernbetjening af varme nanokilder bevægelse og termisk inducerede væskestrømme ved hjælp af lys…en, Flere guld-NPer (kugler med en radius på 200 nm) er begrænset af en ringformet laserfælde (bølgelængde på 532 nm) og transporteres optisk omkring den. Disse NPer samles hurtigt til en stabil grupp
- Hvordan er varmeforbrænding af paraffin sammenlignet med propan?
- Månen kan ikke ses fra Jorden i hvilken fase?
- Hvorfor opløses faste stoffer hurtigere i syre?
- Er solflader farlige for mennesker?
- Måleren er defineret som det, der rejste af i absolut vakuum 1299792458 af et sekund?
- Biofysikere blander uforenelige komponenter i en nanofiber


