Til hvilket af følgende gælder første lovtermodynamik?
Her er hvorfor:
* Den første lov om termodynamik siger, at energi ikke kan oprettes eller ødelægges, kun overføres eller transformeres.
* Dette grundlæggende princip styrer energiens opførsel i alle systemer, fra det mindste atom til den største galakse.
Eksempler på, hvordan det gælder:
* Kemiske reaktioner: Energi konserveres under kemiske reaktioner. For eksempel omdannes brændstofens kemiske energi til varme og lysenergi.
* Mekaniske systemer: Energien fra et bevægende objekt bevares. For eksempel, når en bold kastes, konverteres dens kinetiske energi til potentiel energi, når den stiger og derefter tilbage til kinetisk energi, når den falder.
* biologiske systemer: Levende organismer bruger energi fra mad til at opretholde livsprocesser. Denne energi transformeres og overføres inden for organismen.
Derfor er den første lov om termodynamik et universelt princip, der gælder for alle systemer i universet.
Sidste artikelHvem foreslog bølgemodellen for et atom?
Næste artikelHvad er defineret som en styrke, der handler over afstand?
 Varme artikler
Varme artikler
-
 Halvvejs til høj lysstyrkeEn ny stråleabsorber til de zoner, hvor bjælkerne injiceres fra SPS, blev samlet og testet sidste sommer. Dette er en af de udviklinger, der blev præsenteret på High-Luminosity LHC-årsmødet. Kredit:
Halvvejs til høj lysstyrkeEn ny stråleabsorber til de zoner, hvor bjælkerne injiceres fra SPS, blev samlet og testet sidste sommer. Dette er en af de udviklinger, der blev præsenteret på High-Luminosity LHC-årsmødet. Kredit: -
 Detektorforbedringer opgraderer videnskabelige muligheder for SNS- og HFIR-instrumenterDetektorer hos SNS og HFIR hjælper forskere med at studere spredte neutroner for bedre at forstå materialernes natur. Et ORNL-team designer detektorer, der er skræddersyet til at opfylde specifikation
Detektorforbedringer opgraderer videnskabelige muligheder for SNS- og HFIR-instrumenterDetektorer hos SNS og HFIR hjælper forskere med at studere spredte neutroner for bedre at forstå materialernes natur. Et ORNL-team designer detektorer, der er skræddersyet til at opfylde specifikation -
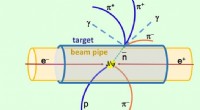 Forskere foreslår ny kilde til sjældne subatomære partiklerSkematisk diagram af antineutronproduktion og interaktion med en proton i målet. Kredit:IHEP Et papir baseret på fælles forskning af prof. Yuan Changzheng fra Institute of High Energy Physics ved
Forskere foreslår ny kilde til sjældne subatomære partiklerSkematisk diagram af antineutronproduktion og interaktion med en proton i målet. Kredit:IHEP Et papir baseret på fælles forskning af prof. Yuan Changzheng fra Institute of High Energy Physics ved -
 Designet af W7-X fusionsenheden gør det muligt at overvinde forhindringer, finder forskerePPPL -fysiker Novimir Pablant. Kredit:Elle Starkman/PPPL Office of Communications. En vigtig hindring for fusionsanordninger kaldet stellaratorer - snoede faciliteter, der søger at udnytte de fusi
Designet af W7-X fusionsenheden gør det muligt at overvinde forhindringer, finder forskerePPPL -fysiker Novimir Pablant. Kredit:Elle Starkman/PPPL Office of Communications. En vigtig hindring for fusionsanordninger kaldet stellaratorer - snoede faciliteter, der søger at udnytte de fusi
- Er det virkelig varmere nu end nogensinde i 100.000 år?
- Hvad strækker sig indefra skorpe til den nedre atmosfære?
- Hvor mange atomer er der i 0,5 mol AR?
- Salt er dannet af positivt ladet natrium, og negativt klor er ladningen på salt negativt en ægte B…
- En lavine af vold:Analyse afslører forudsigelige mønstre i væbnede konflikter
- De geokemiske cyklusser er det?


