Hvad ville der være sket, hvis Rutherford brugte et andet metal end guld i sit alfa -spredningseksperiment?
Hvorfor guld?
* højt atomnummer: Guld har et meget højt atomnummer (79), hvilket betyder, at det har en stor, tæt kerne. Dette øger chancen for en alfa -partikel, der interagerer med kernen, hvilket fører til mærkbar spredning.
* formbarhed: Guld er meget formbart, hvilket gør det muligt for det at blive hamret i ekstremt tynde lagner (kun få atomer tykke). Dette maksimerer chancen for alfa -partikler, der passerer gennem folien og interagerer med individuelle atomer.
Hvad ville der være sket med andre metaller?
* metaller med lavere atomnumre:
* mindre spredning: Metaller med lavere atomantal har mindre, mindre tætte kerner. Dette ville resultere i, at færre alfa -partikler afbøjes markant, hvilket gør det sværere at observere fænomenet med tilbagespredning (partikler, der hopper direkte tilbage).
* Mere transmission: Flere alfa -partikler ville passere lige gennem folien med ringe eller ingen afbøjning, da de ikke ville støde på kernen så ofte.
* metaller med lignende atomnumre:
* lignende resultater, men med variationer: Metaller som platin eller bly har, mens de har lignende atomnumre, har forskellige densiteter og krystalstrukturer. Dette kan resultere i mindre forskelle i spredningsmønstrene, hvilket gør det lidt sværere at fortolke dataene.
implikationer for Rutherfords fund:
* reduceret tilbagespredning: Brug af metaller med lavere atomnumre har muligvis ikke givet stærkt nok bevis for eksistensen af en tæt, positivt ladet kerne. Dette kunne have forsinket opdagelsen af atomets struktur.
* forskellige spredningsmønstre: Det specifikke mønster af spredte alfa -partikler ville være anderledes, hvilket kræver yderligere analyse og fortolkning for at nå de samme konklusioner om atomstrukturen.
* vanskeligheder med at fortolke resultater: Den svagere spredning og mindre fremtrædende tilbagespredning ville have gjort det mere udfordrende at udlede eksistensen af en kerne og dens positive ladning.
Konklusion:
Mens Rutherfords eksperiment kunne have været udført med andre metaller, var guld det optimale valg på grund af dets høje atomnummer og formbarhed. Disse egenskaber sikrede den mest fremtrædende spredning og tilbagespredning, hvilket gav stærkt bevis for atomets nukleare model. Brug af forskellige metaller ville have ført til mindre definitive resultater og potentielt forsinket de afgørende opdagelser fra Rutherford.
 Varme artikler
Varme artikler
-
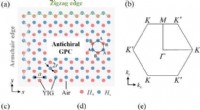 Konfigurerbar topologisk stråleopdeling via antikiral gyromagnetisk fotonisk krystalFig. 1. Konstruktion af antichiral gyromagnetisk fotonisk krystal. (a) Skematisk illustration af antichiral gyromagnetisk fotonisk krystal. (b) Den første Brillouin-zone af honeycomb-gitter. (c) Ikke-
Konfigurerbar topologisk stråleopdeling via antikiral gyromagnetisk fotonisk krystalFig. 1. Konstruktion af antichiral gyromagnetisk fotonisk krystal. (a) Skematisk illustration af antichiral gyromagnetisk fotonisk krystal. (b) Den første Brillouin-zone af honeycomb-gitter. (c) Ikke- -
 Nyt fund af partikelfysik kan hjælpe med at forklare fraværet af antimaterialeSkitse af dimensionsreduktion. Kredit:Helsinki Universitet Ved hjælp af computersimuleringer, forskere i partikelfysik kan muligvis forklare, hvorfor der er mere stof end antimateriale i universet
Nyt fund af partikelfysik kan hjælpe med at forklare fraværet af antimaterialeSkitse af dimensionsreduktion. Kredit:Helsinki Universitet Ved hjælp af computersimuleringer, forskere i partikelfysik kan muligvis forklare, hvorfor der er mere stof end antimateriale i universet -
 Ny højhastighedsmetode til spektroskopiske målingerKonceptuelt billede af metoden til brug af spektralt varierende polarisationstilstande til højhastighedsspektroskopiske målinger. Kredit:Frédéric Bouchard / National Research Council of Canada. Fo
Ny højhastighedsmetode til spektroskopiske målingerKonceptuelt billede af metoden til brug af spektralt varierende polarisationstilstande til højhastighedsspektroskopiske målinger. Kredit:Frédéric Bouchard / National Research Council of Canada. Fo -
 Anvendelse af ikke-Bravais-gitter til lysstyringsteknologiFørste BIC-tilstand fra magnetiske (grønne pile) dipoler. Kredit:Kyoto University En ny lysmanipulerende teknologi er blevet udviklet af et internationalt team, herunder Kyoto University, som kan a
Anvendelse af ikke-Bravais-gitter til lysstyringsteknologiFørste BIC-tilstand fra magnetiske (grønne pile) dipoler. Kredit:Kyoto University En ny lysmanipulerende teknologi er blevet udviklet af et internationalt team, herunder Kyoto University, som kan a
- Hvilken type energi indeholder ting?
- Mikroskopisk liv i den saltholdige jord i naturparken Marismas del Odiel
- Den måde, floder fungerer på, afspejler deres økologiske status, undersøgelse finder
- Temp på denne planet -13c og 37c?
- Hvorfor griner folk, når de bliver kildet?
- Fejlblokkebjerge dannes, når store skorpeblokke er?


