Forståelse af ikke-kovalente kræfter:nøgleinteraktioner i kemi og biologi
Her er nogle nøglepunkter om ikke-kovalente kræfter:
Typer af ikke-kovalente kræfter:
* Brintbinding: Dette er den stærkeste type ikke-kovalent interaktion, der involverer en speciel dipol-dipol-interaktion mellem et brintatom, der er kovalent forbundet med et meget elektronegativt atom (som oxygen eller nitrogen) og et elektronpar i det enlige par af et andet elektronegativt atom. Eksempler inkluderer hydrogenbindingen mellem vandmolekyler og baseparringen i DNA.
* Ioniske interaktioner: Disse forekommer mellem modsat ladede ioner. Denne tiltrækning er relativt stærk i vand og spiller en nøglerolle i dannelsen af salte og stabiliseringen af proteiner.
* Van der Waals-interaktioner: Disse er svage kræfter, der opstår fra midlertidige fluktuationer i elektronfordelingen omkring molekyler. De kan yderligere kategoriseres i:
* Dipol-dipol-interaktioner: Disse forekommer mellem polære molekyler med permanente dipoler.
* London Dispersion Forces: Disse forekommer mellem alle molekyler, selv ikke-polære, på grund af midlertidige dipoler induceret af elektronfluktuationer.
* Hydrofobe interaktioner: Disse er ikke teknisk en kraft, men snarere et resultat af ikke-polære molekylers tendens til at undgå kontakt med vand. De er afgørende for proteinfoldning og membrandannelse.
Karakteristika for ikke-kovalente kræfter:
* Svagere end kovalente bindinger: De kan lettere forstyrres af ændringer i temperatur eller pH.
* Retningsbestemt: De udviser en specifik retning og geometri, som er vigtig for dannelsen af specifikke strukturer som proteinfolder.
* Fælles stærk: Mens individuelle ikke-kovalente bindinger er svage, kan deres kombinerede effekt være betydelig.
Betydningen af ikke-kovalente kræfter:
* Biologiske processer: De er vigtige for:
* Proteinfoldning og stabilitet
* Enzym-substrat interaktioner
* DNA replikation og transkription
* Celle-celle genkendelse
* Membrandannelse
* Materialevidenskab: De påvirker egenskaberne af polymerer, plast og andre materialer.
Eksempler på ikke-kovalente kræfter i aktion:
* Vand: Hydrogenbinding mellem vandmolekyler er ansvarlig for dets høje kogepunkt og overfladespænding.
* DNA: Hydrogenbindinger mellem de nitrogenholdige baser holder de to DNA-strenge sammen.
* Proteinfoldning: Et komplekst samspil af hydrofobe interaktioner, hydrogenbindinger og ioniske interaktioner driver foldningen af proteiner til deres funktionelle tredimensionelle former.
Samlet set er ikke-kovalente kræfter afgørende for strukturen, funktionen og interaktionen af molekyler i biologiske og kemiske systemer. Deres styrke og retningsbestemthed giver mulighed for en bred vifte af forskelligartede og komplekse interaktioner, der understøtter selve livet.
 Varme artikler
Varme artikler
-
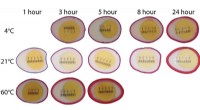 Brug af marinerede æg til at demonstrere diffusionSammenligning af farvestofindtrængning i æggehviderne ved forskellige temperaturer. Kredit:Carson Emeigh, Hyeonggeun Luke Bak, Dilziba Kizghin og Haipeng Zhang Marinerede eller syltede æg nydes af
Brug af marinerede æg til at demonstrere diffusionSammenligning af farvestofindtrængning i æggehviderne ved forskellige temperaturer. Kredit:Carson Emeigh, Hyeonggeun Luke Bak, Dilziba Kizghin og Haipeng Zhang Marinerede eller syltede æg nydes af -
 Undersøgelse af kvantevakuum:Trafikprop i tomt rumDetaljeret visning af den centrale del af eksperimentet om undercyklus kvanteelektrodynamik. Galliumselenidemitterende krystal ses i det lyse område til højre. Her, en ultrakort laserpuls inducerer en
Undersøgelse af kvantevakuum:Trafikprop i tomt rumDetaljeret visning af den centrale del af eksperimentet om undercyklus kvanteelektrodynamik. Galliumselenidemitterende krystal ses i det lyse område til højre. Her, en ultrakort laserpuls inducerer en -
 Uventet observation af is ved lav temperatur, højtryksspørgsmål vandteoriForskere ved Oak Ridge National Laboratory, der studerede superkolde vandtilstande, opdagede en vej til den uventede dannelse af tæt, krystallinske isfaser, der menes at eksistere ud over Jordens græn
Uventet observation af is ved lav temperatur, højtryksspørgsmål vandteoriForskere ved Oak Ridge National Laboratory, der studerede superkolde vandtilstande, opdagede en vej til den uventede dannelse af tæt, krystallinske isfaser, der menes at eksistere ud over Jordens græn -
 Forskning afslører indre funktion af flydende krystallerEt eksempel på flydende krystaller i den nematiske fase, hvor deres stavlignende molekyler stiller sig op på en uordnet, men alligevel parallel måde. Kredit:Wikimedia Commons Flydende krystaller b
Forskning afslører indre funktion af flydende krystallerEt eksempel på flydende krystaller i den nematiske fase, hvor deres stavlignende molekyler stiller sig op på en uordnet, men alligevel parallel måde. Kredit:Wikimedia Commons Flydende krystaller b
- Hvilken specifik organisme er afhængig af endocytose?
- DET sker:Facebook beklager Xi Jinpings navnefalske
- Hvilken dato blev den første solcellepanel opfundet?
- Hvad har processerne med fotosyntese og celle respiration til fælles?
- Hvor mange mol chloridioner er i 3,12 ZnCl2?
- Når det ses under et sammensat lysmikroskop på lav effekt, vises bogstavet P som?


