Forståelse af intermolekylære kræfter:Sammenligning af sammensatte styrker
1. Type af IMF:
* Brintbinding: Den stærkeste type IMF, dannet mellem et hydrogenatom bundet til et stærkt elektronegativt atom (O, N eller F) og et ensomt elektronpar på et andet elektronegativt atom.
* Dipol-dipol-interaktioner: Opstår mellem polære molekyler på grund af de permanente dipoler, de besidder.
* London Dispersion Forces (LDF): Til stede i alle molekyler som følge af midlertidige fluktuationer i elektronfordelingen, der skaber midlertidige dipoler. LDF-styrken øges med molekylstørrelse og overfladeareal.
* Ion-dipol-interaktioner: Opstår mellem ioner og polære molekyler.
2. Molekylær struktur:
* Form: Lineære molekyler har stærkere LDF end forgrenede molekyler på grund af større overfladeareal.
* Polaritet: Polære molekyler har stærkere IMF'er end ikke-polære molekyler på grund af dipol-dipol-interaktioner.
* Størrelse: Større molekyler har stærkere LDF på grund af øget elektronskystørrelse og polariserbarhed.
3. Molekylvægt:
* Tungere molekyler har generelt stærkere LDF på grund af øget elektronskystørrelse.
Her er en generel retningslinje til sammenligning af IMF'er:
* Brintbinding> Dipol-dipol> London Dispersion Forces
Eksempel:
* Vand (H2O) vs. Metan (CH4): Vand har hydrogenbinding på grund af tilstedeværelsen af O-H-bindinger, mens metan kun har LDF. Derfor har vand stærkere IMF'er og et højere kogepunkt.
For effektivt at sammenligne den relative styrke af IMF'er i to forbindelser skal du følge disse trin:
1. Identificer den dominerende IMF i hver forbindelse.
2. Overvej den molekylære struktur og størrelse af hver forbindelse.
3. Sammenlign IMF'ernes styrke baseret på ovenstående faktorer.
Husk:
* Stærkere IMF'er fører til højere smeltepunkter, kogepunkter og fordampningsentalpi.
* Jo mere polært og større et molekyle er, jo stærkere er dets IMF'er sandsynligvis.
Ved at analysere disse faktorer kan du foretage informerede sammenligninger om den relative styrke af intermolekylære kræfter i forskellige forbindelser.
Sidste artikelElektronladning:Forstå den elementære ladning (-1.602 x 10^-19 C)
Næste artikelBorhårdhed:Forstå dens styrke og anvendelser
 Varme artikler
Varme artikler
-
 Kritisk overgangsteori viser flimmer i hjertet før atrieflimrenBimodal fordeling af hjertestater og hjertestatus flimrer før starten af atrieflimren. Kredit:Yew Wai Liew Påvirker op til 4% af patienterne ældre end 65 år, atrieflimren er blandt de mest almin
Kritisk overgangsteori viser flimmer i hjertet før atrieflimrenBimodal fordeling af hjertestater og hjertestatus flimrer før starten af atrieflimren. Kredit:Yew Wai Liew Påvirker op til 4% af patienterne ældre end 65 år, atrieflimren er blandt de mest almin -
 Ny energimåler åbner døren for in-situ, overvågning i realtid af lasere med høj effektDette spejl er en kraftskala, der relaterer kraften fra en laser, der skinner på det, til strømmen (dvs. lysstyrken) for den laser. Forskere ved NIST udvikler disse enheder til at integrere i laserbas
Ny energimåler åbner døren for in-situ, overvågning i realtid af lasere med høj effektDette spejl er en kraftskala, der relaterer kraften fra en laser, der skinner på det, til strømmen (dvs. lysstyrken) for den laser. Forskere ved NIST udvikler disse enheder til at integrere i laserbas -
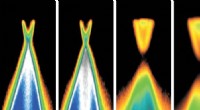 Manglende forbindelse mellem nye topologiske faser af stof opdagetBismut-dopingen er øget fra 0 % (venstre) til 2,2 % (højre). Målinger ved BESSY II viser, at dette fører til øgede båndgab. Kredit:HZB Fysikere på BESSY II har undersøgt en klasse af materialer, d
Manglende forbindelse mellem nye topologiske faser af stof opdagetBismut-dopingen er øget fra 0 % (venstre) til 2,2 % (højre). Målinger ved BESSY II viser, at dette fører til øgede båndgab. Kredit:HZB Fysikere på BESSY II har undersøgt en klasse af materialer, d -
 Ny lysforstærker kan booste potentialet i fotonikWafer med både passive komponenter af siliciumnitrid og de nye forstærkere af erbium-doteret aluminiumoxid. Kredit:University of Twente En ny lysforstærker udviklet ved University of Twente øger i
Ny lysforstærker kan booste potentialet i fotonikWafer med både passive komponenter af siliciumnitrid og de nye forstærkere af erbium-doteret aluminiumoxid. Kredit:University of Twente En ny lysforstærker udviklet ved University of Twente øger i
- Hvad er et eksempel på en nettokraft?
- Hvad er en stråle af sollys?
- Hvad er de tre mest almindelige typer bjerg giver en kort beskrivelse og et eksempel hver.?
- Forskere undersøger, hvordan mennesker reagerer på røg fra skovbrande
- Hvilken form dannes konstellationen cetus?
- Kun 2 % af de sorte Chicagoanklager om politiforseelse blev fastholdt


