Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandling

Fra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Research Institute
Ved hjælp af avanceret massespektrometri teknologi, forskere fra Florida-campus af The Scripps Research Institute (TSRI) har udviklet en molekylær model, der kan give en ny ramme for at forbedre designet af osteoporosebehandlinger.
"På grund af vores aldrende befolkning, disse former for terapi er i stor efterspørgsel, " sagde studieleder Patrick R. Griffin, medformand for TSRI Institut for Molekylær Medicin. Forskningen blev offentliggjort i dag i tidsskriftet Naturkommunikation .
Ved at bruge en teknologi kendt som HDX, som Griffin-laboratoriet har drevet ind i mainstream-proteinanalyse, forskerne leverede de første dynamiske øjebliksbilleder af et primært mål for osteoporosebehandlinger:en receptor, der regulerer calciumniveauet for at opretholde sunde knogler.
Brugen af nuværende lægemidler, der er rettet mod denne receptor - kaldet vitamin D-receptoragonister - er begrænset, fordi brugen kan resultere i hypercalcæmi, en tilstand, der kan svække knogler og endda forårsage nyresten, på grund af for meget kalk i blodbanen.
For at løse dette problem, forskere har brug for et klarere billede af strukturen af D-vitamin-receptoren. Vitamin D-receptorkomplekset regulerer knoglemineralisering ved at kontrollere et gen kendt som BGLAP, som er målet for 1α, 25-dihydroxyvitamin D3 (1, 25D3), den aktive hormonelle version af vitamin D. Desværre, øgede niveauer på 1, 25D3 aktiverer også et calciumregulerende gen kaldet TRPV6, hvilket fører til hypercalcæmi.
Griffin og hans kolleger håber at eliminere denne trussel ved at udvikle 1, 25D3-analoger (kendt som dissocierede vitamin D-receptorligander eller VDRM'er), der differentielt målretter mod BGLAP-gener, samtidig med at man undgår TRPV6.
"Idéen er, at hvis vi kunne fingeraftrykke, hvordan disse forskellige ligander interagerer med D-vitamin-receptoren, vi kunne levere en slags køreplan for at hjælpe med at udvikle dem, der kun udløser ikke-hypercalcæmi-genet, " sagde Griffin.
Indtil nu, at udvikle mere selektive forbindelser er blevet hæmmet af det faktum, at ingen forstod den strukturelle mekanisme, der får dem til at virke.
"Denne undersøgelse viser, at det er muligt at udvikle et lægemiddel, der kan ændre visse aspekter af komplekset for at undgå problematisk aktivering af TRPV6 - og undersøgelsen peger på nye måder at designe potentielle terapeutiske midler til at behandle osteoporose sikkert og mere effektivt, " bemærkede Griffin.
Griffin og hans kolleger udførte en detaljeret sammenlignende biofysisk undersøgelse af hundredvis af forbindelser, alle med forskellige kemiske strukturer.
"Vores resultater giver øjebliksbilleder af distinkte konformationelle ensembler af receptoren, hvilket gør det muligt at antage forskellige orienteringer afhængigt af sammensatte struktur, DNA og co-aktivator binding, " sagde TSRI Research Associate Jie Zheng, undersøgelsens første forfatter. "Denne undersøgelse viser den molekylære mekanisme af en selektiv D-vitamin-receptormodulator versus agonister, og hvordan de driver forskellige interaktioner med co-regulatorer, når de er forbundet med sekvensspecifikke DNA'er."
Forskerne brugte hydrogen-deuterium-udveksling (HDX) massespektrometri, en høj præcision, højsensitiv kortlægningsteknik, der har vist sig at være en robust metode til at undersøge proteinkonformationel eller forme skiftende dynamik inden for sammenhæng med ligand og protein/protein-interaktioner.
HDX kan vise de specifikke områder af proteinkomplekset, der ændres ved interaktion med specifikke ligander, i dette tilfælde vitamin D-receptorkomplekset, information, som kan bruges til at udlede strukturelle ændringer, der er resultatet af en specifik interaktion.
 Varme artikler
Varme artikler
-
 Enkeltcelletest kan afsløre præcis, hvordan lægemidler dræber kræftcellerD 2 O-probet CANcer-følsomhedstest Ramanometri (D 2 O-CANST-R) Kredit:LIU Yang Kræftceller er smarte, når det kommer til medicin mod kræft, udvikler sig og bliver resistente over for selv de s
Enkeltcelletest kan afsløre præcis, hvordan lægemidler dræber kræftcellerD 2 O-probet CANcer-følsomhedstest Ramanometri (D 2 O-CANST-R) Kredit:LIU Yang Kræftceller er smarte, når det kommer til medicin mod kræft, udvikler sig og bliver resistente over for selv de s -
 Secret of britisk chokoladefremstilling inspirerer til opdagelse af ny laktoseformKredit:CC0 Public Domain En ny form for krystallinsk laktose er blevet opdaget ved hjælp af en del af teknikken, der giver britisk chokolade sin unikke appel. Den nye form for laktose, en ingredi
Secret of britisk chokoladefremstilling inspirerer til opdagelse af ny laktoseformKredit:CC0 Public Domain En ny form for krystallinsk laktose er blevet opdaget ved hjælp af en del af teknikken, der giver britisk chokolade sin unikke appel. Den nye form for laktose, en ingredi -
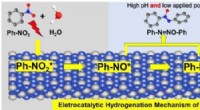 Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly
Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly -
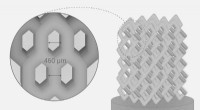 Forskere udviklede en ny metode til fremstilling af knogleimplantaterKnogleimplantat. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Design, Fremstilling, and Materials (CDMM) har udviklet en metode til at designe og fremstille kompleksformede kera
Forskere udviklede en ny metode til fremstilling af knogleimplantaterKnogleimplantat. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Design, Fremstilling, and Materials (CDMM) har udviklet en metode til at designe og fremstille kompleksformede kera
- NASA konstaterer, at den tropiske storm Irondros har fordrevet kraftig nedbør
- Forskere lokaliserer forældrenes lynnedslag af sprites
- High Definition Earth-Viewing nyttelast når end-of-life på stationen, overstiger den forventede le…
- Hurtige nanorobotter kunne en dag rense jord og vand, levere stoffer
- Indfødte samfund bevæger sig væk fra offentlige forsyningsselskaber
- Centrifugeringsstrømme skifter ved terahertz -frekvenser


