Elektronisk entropi forbedrer vandspaltning

Kredit:George Hodan/public domain
Forskere har længe vidst, at cerium er det bedste element at bruge, når man spalter vand til brint og ilt - en nøgleteknik til at skabe brintgas til brændstof. Men hvorfor, Nemlig, cerium er så vellykket har været langt mindre forstået.
Nu har et Northwestern University-hold under ledelse af Chris Wolverton opdaget, at ceriums elektroniske entropi, som skabes, når en elektron skifter mellem forskellige tilstande i en elektronskal, er den underliggende årsag til dens succes. Denne opdagelse kan hjælpe forskere med bedre at udnytte ceriums entropi til vandspaltningsteknologier.
"For at vandspaltning skal være hurtig nok til at være praktisk, du har brug for en stor mængde entropi, " sagde Wolverton, professor i materialevidenskab og teknik i Northwesterns McCormick School of Engineering. "Det viser sig, at cerium er magi for entropi."
Støttet af det amerikanske energiministerium, forskningen blev for nylig offentliggjort i Naturkommunikation . Shahab Naghavi, en postdoc i Wolverton Research Group, fungerede som avisens første forfatter.
Siden 1970'erne, forskere har udråbt potentialet i en "brintøkonomi, ", hvor brint ville erstatte benzin for at brænde jordtransport. Når det brændes, brints eneste biprodukt er vand, gør det miljømæssigt renere og mere energieffektivt end dets fossile brændstoffer. Ren brintgas, imidlertid, er meget sjælden i jordens atmosfære.
"Problemet er:hvordan får man brinten i første omgang?" spurgte Wolverton. "I øjeblikket, du skal brænde kulbrinter, men det producerer kuldioxid."
Spaltning af vand (eller damp) kunne rent og effektivt producere nok ren brint til at gøre brintøkonomien til en sand mulighed. At spalte brint fra ilt, forskere bruger varme genereret af solstråling og ceriumoxid, eller ceria. Brug af sollys til at opvarme ceria til 1, 000- til 1, 500 grader Celsius driver en række reaktioner, der får brint til at spalte fra.
Wolverton og andre vidste tidligere, at entropi var nøglen til at gøre denne reaktion mulig, men de var ikke i stand til at finde kilden til ceriums entropi. "De fleste troede, at entropi var forårsaget af blanding af ilt eller vibrationer fra varmen, " sagde Wolverton. "Men vi fandt ud af, at det er en anden kilde, og det er ikke, hvad du måske tror."
For at den kemiske reaktion, der driver vandspaltning, skal lykkes, cerium i oxidet skal få en elektron. Og den enkelte elektron giver anledning til en masse entropi.
"Hvis der er flere steder for elektronen, der giver anledning til elektronisk entropi, " Wolverton forklarede. "Elektronen kan gå fra en tilstand til en anden til en anden og skaber uorden på den elektroniske skala, og dermed, entropi."
Ceriums familie af grundstoffer - kendt som sjældne jordarter - har naturligvis flere elektrontilstande, som elektronen kan bevæge sig omkring. Wolvertons hold beregnede den elektroniske entropi af alle 17 sjældne jordarter og opdagede, at cerium viste den største mængde.
"I lang tid, vi har vidst, at cerium er godt til vandspaltning, men vi vidste ikke helt hvorfor " sagde Wolverton. "Nu ved vi delvist hvorfor, og det åbner muligheder for fremtidigt arbejde."
 Varme artikler
Varme artikler
-
 Side-by-side afsætning af atomisk flade halvlederplader forbedrer solcellekonverteringseffektivitet…Solenergikonvertering ved hjælp af en lateral WSe2-MoS2 heterojunction. Kredit:© 2017 WILEY VCH Supertynde fotovoltaiske enheder understøtter solteknologien, og der søges derfor meget efter gevins
Side-by-side afsætning af atomisk flade halvlederplader forbedrer solcellekonverteringseffektivitet…Solenergikonvertering ved hjælp af en lateral WSe2-MoS2 heterojunction. Kredit:© 2017 WILEY VCH Supertynde fotovoltaiske enheder understøtter solteknologien, og der søges derfor meget efter gevins -
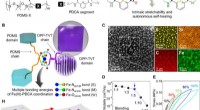 Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter
Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter -
 Bladguld kunne hjælpe med at diagnosticere virusinfektioner i lav-ressource indstillingerEn billig elektrode lavet af bladguld kunne bruges til at hjælpe med at opdage virusinfektioner i miljøer med lav ressource; en skilling (venstre) vises til sammenligning af størrelse. Kredit:Tilpasse
Bladguld kunne hjælpe med at diagnosticere virusinfektioner i lav-ressource indstillingerEn billig elektrode lavet af bladguld kunne bruges til at hjælpe med at opdage virusinfektioner i miljøer med lav ressource; en skilling (venstre) vises til sammenligning af størrelse. Kredit:Tilpasse -
 Forskere trykker regnbuefarvestoffer på skinnende chokoladeKredit:ETH Zürich ETH-forskere får chokolade til at skinne i regnbuefarver uden tilsætning af farvestoffer. De har fundet en måde at præge en speciel struktur på overfladen af chokoladen for at
Forskere trykker regnbuefarvestoffer på skinnende chokoladeKredit:ETH Zürich ETH-forskere får chokolade til at skinne i regnbuefarver uden tilsætning af farvestoffer. De har fundet en måde at præge en speciel struktur på overfladen af chokoladen for at
- Havbefrugtning af usædvanlige mikrober strækker sig til de kolde farvande i Ishavet
- Dinosaurknogler er hjemsted for mikroskopisk liv
- Forvirring og dårlige beskeder førte til hamstring, eksperter foreslår
- Et videnskabsprojekt ved hjælp af Cold Vs. Hot Tennis Balls
- Ny højhastighedstest viser, hvordan antibiotika kombineres for at dræbe bakterier
- Hvorfor lejlighedsboere har brug for indendørs planter


