Klikkemi-reaktioner kan øge kræftbekæmpende lægemiddelstyrke
Kredit:ACS
Forskere ved The Scripps Research Institute (TSRI) har udviklet en hurtig og nem måde til samtidig at modificere snesevis af lægemidler eller molekyler for at forbedre deres sygdomsbekæmpende egenskaber. Ved at bruge tilgangen, videnskabsmænd byttede en kemisk gruppe ud med en anden i 39 kræftlægemidler - og opdagede under laboratorieforhold, at de kemisk ændrede versioner af tre af stofferne havde mere potent anti-kræftaktivitet.
Resultaterne, offentliggjort i dag i Journal of the American Chemical Society , afsløre en kraftfuld anvendelse af såkaldt "klikkemi" til lægemiddelopdagelse.
"Normalt skal man lave tusinder eller millioner af molekyler og gennemgå en stor screeningsproces for at finde et eller to molekyler, der er interessante og måske virker, " siger Peng Wu, PhD, en TSRI lektor og en af undersøgelsens hovedforfattere. "Med denne nye tilgang, du kan spare tid og penge ved at starte med lægemidler og molekyler, du ved allerede er aktive, og spørge, om en hurtig modifikation gør nogen af dem bedre."
"Vores resultater tyder på, at vi vil være i stand til at tage et lægemiddel og gøre det mere potent, hurtigere handlende, og forhåbentlig med bedre biotilgængelighed, " tilføjer nobelpristageren K. Barry Sharpless, PhD, som var med til at lede undersøgelsen.
Skarpt, TSRI W.M. Keck professor i kemi, først udtænkt af klikkemi i 1990'erne. Klikkemi er betegnelsen for simple molekylære reaktioner, der hver især kan udføres i én beholder, uforstyrret af vand, og generere kun ét stabilt produkt med højt udbytte. Sharpless sammenligner metoden med at dekorere molekyler som juletræer, tilføje en ny funktionel "pynt" til en af et molekyles grene, som han kalder "klikbare hubs".
"I stedet for at forfølge kundeemner, som er den traditionelle metode, SuFEx klikkemi handler om at forbinde lovende lægemiddelkandidater direkte med mål, " siger Sharpless.
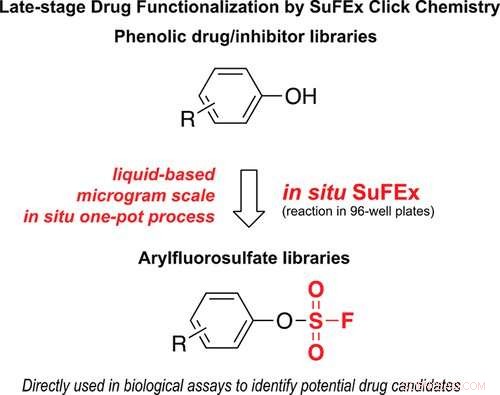
En af de seneste klikkemi-reaktioner udviklet af Sharpless' gruppe var Sulphur (VI) Fluoride Exchange (SuFEx), som omdanner enhver phenol kemisk gruppe til et fluorsulfat. Fordi fluorsulfater har nogle fordele i forhold til phenoler - herunder tættere binding til proteiner, og mindre evne til at blive modificeret i cellen - SuFEx-reaktionen tilbyder en måde at potentielt forbedre phenollægemidler.
Imidlertid, transformationen er typisk afhængig af sulfurylfluoridgas, hvilket gør det svært at udføre på mange forskellige molekyler på samme tid; hver reaktion skal udføres i sin egen kolbe.
I det nye blad, Sharpless og Wu viser, at sulfurylfluoridgas kan opløses i et organisk opløsningsmiddel for at lave en flydende form af det reagens, der er nødvendigt for SuFEx. "Nu, pludselig, vi kan bruge dette i high-throughput eksperimenter, " siger Wu.
For at teste reaktionens nytte ved opdagelse af lægemidler, Skarpt, Wu og deres kolleger lagde 39 eksisterende kræftlægemidler indeholdende phenoler på plader, tilføjet den flydende version af sulfurylfluorid til hver brønd, og eksponerede kræftceller for både de originale forbindelser og de resulterende fluorsulfatversioner. I tre tilfælde, det nye fluorsulfat-lægemiddel dræbte flere kræftceller end den originale version. Når den er ændret med SuFEx, brystkræftlægemidlet Fulvestrant havde en stor effekt på østrogenreceptorer i brystkræftceller, og kræftlægemidlet Combretastatin A4 var 70 gange mere potent mod tyktarmskræftceller.
Ved nærmere undersøgelse, forskerne opdagede, at de nye molekyler bandt sig bedre til deres molekylære mål og var mindre tilbøjelige til at blive metaboliseret af cellerne.
"Vi mener, at vores tilgang generelt er anvendelig til modifikation af lægemidler uden for kun kræftmedicin, " siger Wu. Holdet bruger allerede den nye high-throughput SuFEx til at modificere lægemidler rettet mod immunsystemets T-celler, tilføjer han.
 Varme artikler
Varme artikler
-
 Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømningFigur 1:(a) Skematisk diagram over høj gennemløb, (b) fysisk skygge maske. Kredit:© Science China Press Multikomponentmaterialer er blandt de mest lovende materialer inden for teknik og biomedicin
Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømningFigur 1:(a) Skematisk diagram over høj gennemløb, (b) fysisk skygge maske. Kredit:© Science China Press Multikomponentmaterialer er blandt de mest lovende materialer inden for teknik og biomedicin -
 Årsag til katodenedbrydning identificeret for nikkelrige materialerMedlemmer af Brookhaven-teamet vises ved NSLS-IIs ISS-strålelinje, hvor en del af undersøgelsen blev udført. På billedet forfra og bagfra ses Eli Stavitski, Xiao-Qing Yang, Xuelong Wang, og Enyuan Hu.
Årsag til katodenedbrydning identificeret for nikkelrige materialerMedlemmer af Brookhaven-teamet vises ved NSLS-IIs ISS-strålelinje, hvor en del af undersøgelsen blev udført. På billedet forfra og bagfra ses Eli Stavitski, Xiao-Qing Yang, Xuelong Wang, og Enyuan Hu. -
 blodig, freaky, cool:Marine sneglegift kunne forbedre insulin til diabetespatienterEn keglesnegl venter på, at en fisk svømmer forbi. Kredit:University of Utah Health Selvom den er moderat mobil, marine keglesnegle har perfektioneret flere strategier til at fange bytte. Nogle fi
blodig, freaky, cool:Marine sneglegift kunne forbedre insulin til diabetespatienterEn keglesnegl venter på, at en fisk svømmer forbi. Kredit:University of Utah Health Selvom den er moderat mobil, marine keglesnegle har perfektioneret flere strategier til at fange bytte. Nogle fi -
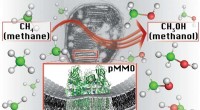 Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
- Forskere bruger mikroorganismer til at fremstille funktionel bakteriel cellulose in situ
- Kontaktløs og rumligt struktureret køling ved at dirigere termisk stråling
- Ny model til evaluering af lanceringer af banemarkssystemer
- En halv milliard år gammel mærkelig vidunderorm får endelig sin plads i livets træ
- Mikroplast i drikkevand er ikke en sundhedsrisiko lige nu:WHO
- Træning af kirurger som hunde, icky penge vinder 2019 Ig Nobels


