Sammenligning af vandisomerers kemi
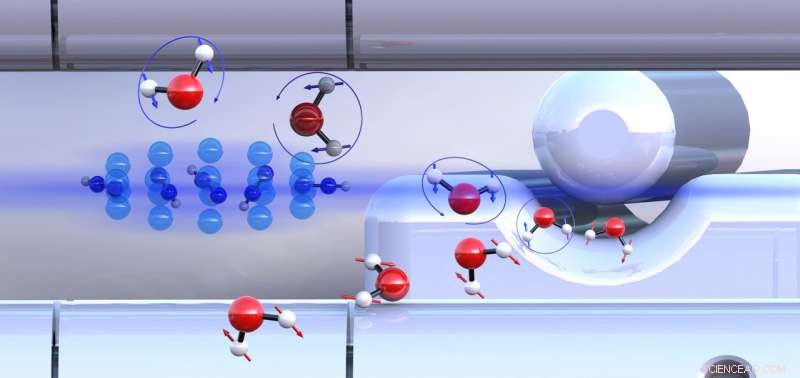
Forsorterede ortho-vand- og para-vand-molekyler med forskelligt orienterede nukleare spins (blå eller røde pile) reagerer med diazenyliumioner (i midten til venstre) ved forskellige hastigheder. Kredit:Universitetet i Basel
Vandmolekyler findes i to forskellige former med næsten identiske fysiske egenskaber. For første gang, det er lykkedes forskere at adskille de to former for at vise, at de kan udvise forskellige kemiske reaktiviteter. Disse resultater blev rapporteret af forskere fra universitetet i Basel og deres kolleger i Hamborg i det videnskabelige tidsskrift Naturkommunikation .
Fra et kemisk perspektiv, vand er et molekyle, hvor et enkelt oxygenatom er forbundet med to brintatomer. Det er mindre kendt, at vand findes i to forskellige former (isomerer) på molekylært niveau. Forskellen ligger i den relative orientering af de to brintatomers nukleare spins. Afhængigt af om spins er justeret i samme eller modsatte retning, man henviser til ortho- eller para-vand.
Eksperimenter med sorterede vandmolekyler
Forskergruppen ledet af professor Stefan Willitsch fra universitetet i Basel's afdeling for kemi har undersøgt, hvordan de to former for vand adskiller sig med hensyn til deres kemiske reaktivitet - deres evne til at gennemgå en kemisk reaktion. Begge isomerer har næsten identiske fysiske egenskaber, hvilket gør deres adskillelse særligt udfordrende.
Denne adskillelse blev muliggjort af en metode baseret på elektriske felter udviklet af professor Jochen Küpper fra Hamburg Center for Free-Electron Laser Science. Ved at bruge denne tilgang, forskerne var i stand til at igangsætte kontrollerede reaktioner mellem de "forudsorterede" vanisomerer og ultrakolde diazenyliumioner ("protoneret nitrogen") holdt i en fælde. Under denne proces, en diazenyliumion overfører sin proton til et vandmolekyle. Denne reaktion observeres også i det interstellare rums kemi.
Øget reaktivitet
Det blev påvist, at para-vand reagerer omkring 25 procent hurtigere end orto-vand. Denne effekt kan forklares ud fra, at kernespin også påvirker rotationen af vandmolekylerne. Som resultat, forskellige tiltrækningskræfter virker mellem reaktionspartnerne. Para-vand er i stand til at tiltrække sin reaktionspartner stærkere end ortho-formen, hvilket fører til en øget kemisk reaktivitet. Computersimuleringer bekræftede disse eksperimentelle resultater.
I deres eksperimenter, forskerne arbejdede med molekyler ved meget lave temperaturer tæt på det absolutte nulpunkt (ca. -273°C). Dette er ideelle betingelser for præcist at forberede individuelle kvantetilstande og definere energiindholdet i molekylerne, og at forårsage en kontrolleret reaktion mellem dem. Willitsch forklarer den eksperimentelle tilgang:"Jo bedre man kan kontrollere tilstanden af de molekyler, der er involveret i en kemisk reaktion, jo bedre kan de underliggende mekanismer og dynamikker i en reaktion undersøges og forstås."
 Varme artikler
Varme artikler
-
 Østers:et dyr, to limØsters adhæsion ændres efter metamorfose fra larver til unge begynder. Profilen af en to måneder gammel østers er vist her. Kredit:Purdue University foto/Jonathan Wilker Østers bygger omfattende
Østers:et dyr, to limØsters adhæsion ændres efter metamorfose fra larver til unge begynder. Profilen af en to måneder gammel østers er vist her. Kredit:Purdue University foto/Jonathan Wilker Østers bygger omfattende -
 Sporingsmekanismer for krystallisering i realtidAlkaliske opløsninger af aluminium og natriumioner danner komplekse geler (se eksempel) sammensat af aluminiummetalcenternetværk. Under krystallisation, disse netværk frigiver ioner, hvis struktur påv
Sporingsmekanismer for krystallisering i realtidAlkaliske opløsninger af aluminium og natriumioner danner komplekse geler (se eksempel) sammensat af aluminiummetalcenternetværk. Under krystallisation, disse netværk frigiver ioner, hvis struktur påv -
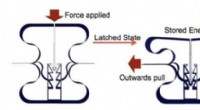 Forskere designer materiale, der kan lagre energi som et ørnegrebDen skraldende byggeklods, der kunne indlejres i de nye materialer. Efter lodret kompression, det holder materialer kollapset, og kan frigive deres energi på side-vejs pull. Kredit:Stoyan Smoukov
Forskere designer materiale, der kan lagre energi som et ørnegrebDen skraldende byggeklods, der kunne indlejres i de nye materialer. Efter lodret kompression, det holder materialer kollapset, og kan frigive deres energi på side-vejs pull. Kredit:Stoyan Smoukov -
 Kunstig intelligens fremskynder fotodynamiske simuleringerIllustration til undersøgelsen, som dukkede op på et af forsiderne til Kemisk videnskab:Kunstige neurale netværk hjælper med drastisk at accelerere simuleringer af fotoinducerede processer. Kredit:Jul
Kunstig intelligens fremskynder fotodynamiske simuleringerIllustration til undersøgelsen, som dukkede op på et af forsiderne til Kemisk videnskab:Kunstige neurale netværk hjælper med drastisk at accelerere simuleringer af fotoinducerede processer. Kredit:Jul
- Kemikere kortlægger en kunstig molekylær selvsamlingsvej med livets kompleksitet
- Forskere skaber kinetisk tøj til at overvåge kropsbevægelser
- skelsættende opdagelse i guld nanorod ustabilitet
- Analyse af talesprog og 3-D ansigtsudtryk for at måle sværhedsgraden af depression
- Mod sikrere, atomreaktorer med lang levetid-metaldesign kan øge strålingsresistensen med 100 gange
- Sjove eksperimenter for det periodiske bord


