Forskere skaber atomlimpistol for at bygge bedre nukleinsyreterapi
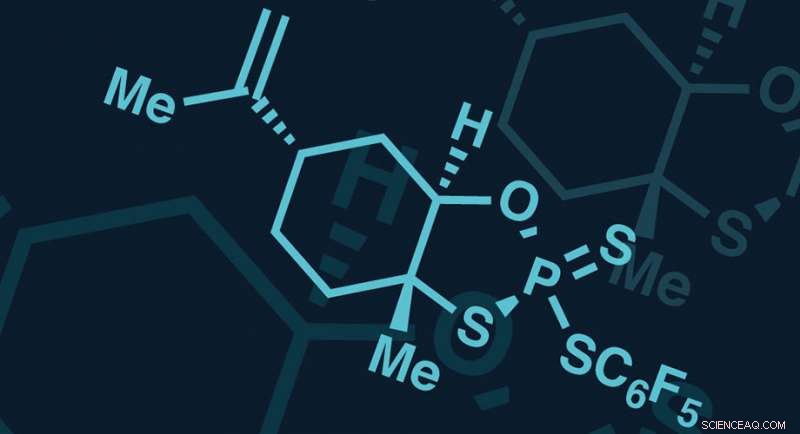
Kredit:Scripps Research Institute
Når det kommer til visse molekyler, form gør hele forskellen. Formen af limonen, for eksempel, en forbindelse fremstillet af citrusfrugter, bestemmer, om det smager af appelsinjuice eller terpentin. I tilfælde af terapi, 3D-formen af et molekyle kan være afgørende for aktivitet.
Nu, forskere ved Scripps Research og Bristol-Myers Squibb har skabt et kraftfuldt nyt værktøj til præcis styring af 3-D-arkitekturen - også kaldet stereokemi - af koblinger kendt som thiophosphater, fundet i nogle lovende nye lægemidler, der retter sig mod genetiske molekyler og andre sygdomsmål, ifølge en avis offentliggjort i dag i Videnskab .
Kaldt phosphor-svovl inkorporering (PSI, for kort), den første teknologi af sin slags fungerer som en atomlimpistol, binding af nukleosider til oligomerer med specifikke, forudprogrammerede rumlige konfigurationer ved thiophosphatbindingen. Thiophosphat-bindingerne er analoger til naturens metode til at forbinde nukleosider og tilbyder flere fordele for lægemiddeludvikling, men tilføj kompleksiteten af stereokemi ved phosphoratomet. PSI giver en hidtil uset, billig og enkel metode til at muliggøre udviklingen af enkelte isomerer af disse forbindelser, som kan have hundredtusindvis af stereoisomerer.
"Thiophosphatbaserede nukleotidforbindelser repræsenterer et bemærkelsesværdigt terapeutisk potentiale, men vores forståelse af disse systemer er blevet forhindret i en manglende evne til let at kontrollere stereokemien af thiophosphat under lægemiddelsyntese, " siger Phil Baran, Ph.D., en Scripps Research professor og seniorforsker om undersøgelsen. "PSI giver en robust og stereostyret metode til at syntetisere oligonukleotidlægemidler, giver os mulighed for at skabe, analysere og fremstille stereoisomerer af en lægemiddelkandidat på måder, som tidligere kun var mulige med dyre og ineffektive metoder."
Martin Eastgate, Ph.D., co-senior forfatter på Videnskab papir og ledende videnskabsmand på Bristol-Myers Squibb-holdet, siger, at ved at tilvejebringe en enkel og generaliseret metode til at kontrollere stereokemien af de fosforcentrerede bindinger, kaldet thiophosphatbindinger, PSI overvinder en betydelig hindring for at opdage den næste generation af innovative lægemidler.
"Opfindelsen af disse stereoselektive, enkel, skalerbare og stabile reagenser giver en løsning på dette komplekse problem, " siger Eastgate, gruppedirektør og leder af kemisk forskning i Bristol-Myers Squibbs organisation for kemisk og syntetisk udvikling. "Vi håber, at opfindelsen af PSI-reagensklassen vil vise sig at være en muliggørende teknologi for det videnskabelige samfund."
At bygge den lange kæde af nukleotider, der er til stede i oligonukleotider, den nuværende fremstillingsteknik er afhængig af det unaturlige, men meget reaktiv, phosphor(III) oxidationstilstand. En af de største begrænsninger ved at anvende standard P(III)-kemi til thiophosphatsyntese er mangel på kontrol over 3-D-formen af det nye fosforbaserede stereocenter.
"At bruge P(III) kemi til at producere selv en beskeden mængde af forbindelsen som en enkelt stereoisomer er udfordrende, gør det vanskeligt fuldt ud at vurdere indvirkningen af molekylær form på biologisk funktion, " siger Justine deGruyter, en Scripps Research kandidatstuderende og en af de første forfattere på Videnskab papir. For at overvinde disse begrænsninger, Bristol-Myers Squibb og Scripps forskerne udforskede ved hjælp af en anden form for fosfor, P(V), som længe blev undgået af syntetiske kemikere på grund af dets lave reaktivitet. Mens P(V) generelt er mindre reaktiv end P(III), hvilket kan gøre det mere udfordrende at bruge til at bygge molekyler i laboratoriet, forskerne havde mistanke om, at dens overlegne stabilitet kunne udmønte sig i langt bedre kontrol over den tredimensionelle molekylære form under syntese.
I løbet af to år, Scripps og Bristol-Myers Squibb-holdene samarbejdede om at udvikle en effektiv metode til at bruge P(V) til at producere ønskede stereoisomerer af molekyler. De fokuserede på at finde en måde at binde sammen kæder af nukleosider med et sporløst reagens, der ikke ville efterlade uønskede atomer. Resultatet af dette var reagenset PSI.
Forskerne har brugt PSI til at generere rene stereoisomerer af cykliske dinukleotider (CDN'er), grundlaget for CDN-lægemiddelkandidater, der har skabt meget begejstring som en ny type cancerimmunterapi. CDN-lægemidler retter sig mod et protein kaldet STING (STimulator af INTErferon-gener) for at aktivere kroppens immunsystem mod kræft.
"CDN'er viser utroligt løfte om at aktivere immunsystemet mod kræftformer, men indtil nu var der ingen enkel måde at kontrollere deres stereokemi på, " siger Kyle Knouse, en kandidatstuderende i Barans laboratorium og førsteforfatter på Videnskab papir. "Evnen til effektivt og billigt at skabe rene stereoisomerer vil give et kraftfuldt værktøj til at fremme CDN-forskning."
I tilfælde af CDN'er, og ASO-lægemidler, Evnen til at fremstille en enkelt stereoisomer vil gøre det muligt for videnskabsmænd at udforske, hvilke former af stofferne der er mest terapeutisk effektive og generere disse stereoisomerer til klinisk brug. En anden fordel ved PSI er, at den er sporløs, dermed undgår man tiden og omkostningerne ved at skulle fjerne det fra lægemiddelproduktet under fremstillingen.
Bristol-Myers Squibb og Scripps forskerne er begejstrede for at fortsætte med at udforske andre måder at bruge disse reagenser til at bygge komplekse molekyler.
 Varme artikler
Varme artikler
-
 Ny forbindelse kan forhindre bakterier i at forårsage sygdomMichael Federle, lektor i medicinsk kemi og farmakognosi ved UIC College of Pharmacy. Kredit:UIC/Roberta Dupuis-Devlin En undersøgelse offentliggjort i Journal of Biological Chemistry er den før
Ny forbindelse kan forhindre bakterier i at forårsage sygdomMichael Federle, lektor i medicinsk kemi og farmakognosi ved UIC College of Pharmacy. Kredit:UIC/Roberta Dupuis-Devlin En undersøgelse offentliggjort i Journal of Biological Chemistry er den før -
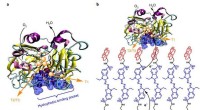 Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side
Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side -
 Gennembrud af kemisk syntese lover fremtiden for antibiotikaKredit:CC0 Public Domain University of Colorado Boulder kemiforskere har udviklet en ny måde at syntetisere og optimere en naturligt forekommende antibiotisk forbindelse, der en dag kan bruges til
Gennembrud af kemisk syntese lover fremtiden for antibiotikaKredit:CC0 Public Domain University of Colorado Boulder kemiforskere har udviklet en ny måde at syntetisere og optimere en naturligt forekommende antibiotisk forbindelse, der en dag kan bruges til -
 Selektiv koncentration af kationiske arterKredit:Pohang University of Science &Technology (POSTECH) Prøveforbehandlingsprocesser såsom koncentration eller klassificering er afgørende for at finde sporstoffer til stede i en væske. I videns
Selektiv koncentration af kationiske arterKredit:Pohang University of Science &Technology (POSTECH) Prøveforbehandlingsprocesser såsom koncentration eller klassificering er afgørende for at finde sporstoffer til stede i en væske. I videns
- Moss opdager hurtigt, sporer luftforurenende stoffer i realtid
- Rapport:Selv i mere forskellige distrikter, skoleadskillelse eksisterer stadig
- Greta Thunberg:Verdens ungdommelige klimabevidsthed
- Mønsterfejlfrie nanokrystalfilm med nanometeropløsning
- Interessante Fakta om Quartzite
- 10 bemærkelsesværdige eksoplaneter


