Bæredygtig, stærkt selektiv biokatalytisk omdannelse af aldehyder til carboxylsyrer
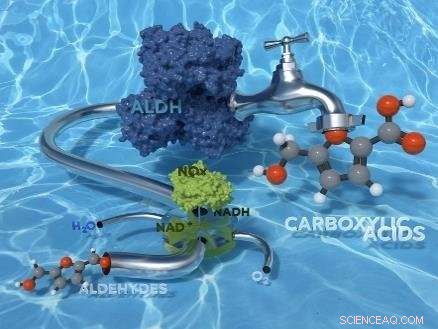
Forsidebillede af den aktuelle udgave af Green Chemistry med HIMS/Biocat -forskningen.
Forskere fra University of Amsterdams Van't Hoff Institute for Molecular Sciences (HIMS) har udviklet den første levedygtige biokatalytiske 'grønne' proces til kemoselektiv oxidation af aldehyder til carboxylsyrer. Papiret, der beskriver forskningen, fremgår af den aktuelle udgave af tidsskriftet Grøn kemi .
Oxidationen af aldehyder til carboxylsyrer er en vigtig og industrielt relevant kemisk reaktion, for eksempel med hensyn til syntese af lægemidler og biobaserede polymerer. Nuværende oxidationsprocedurer kræver rigelig brug af giftige kemiske reagenser og producerer ofte uønskede biprodukter.
På jagt efter forbedring af det miljømæssige fodaftryk for aldehydoxidation, forskellige nye syntetiske metoder er blevet undersøgt. Indtil nu, imidlertid, der er ikke udviklet en økonomisk levedygtig procedure, der er baseret på miljømæssigt godartede reagenser og/eller opløsningsmidler, og det kombinerer en forhøjet produktivitet med en perfekt selektivitet (hvilket betyder, at kun ønskede aldehydfunktionelle grupper oxideres, dermed minimere eller endda helt undgå dannelsen af uønskede biprodukter).
Godartet biokatalyse
Som et interessant 'grønt' alternativ, biokatalytisk, enzymbaserede metoder til oxidation af funktionelle grupper viser milde reaktionsbetingelser (omgivelsestemperatur og atmosfærisk tryk) i et vandigt miljø, og de opnår generelt meget gode selektiviteter. Desuden, de kan udnytte molekylært oxygen som en godartet oxidant.
HIMS -forskerteamet ledet af DrFrancesco Mutti har nu med succes undersøgt brugen af aldehyddehydrogenaseenzymer til oxidation af aldehyder til carboxylsyrer. I en artikel, der for nylig blev accepteret af RSC-tidsskriftet med stor indflydelse Grøn kemi , forskerne præsenterer en undersøgelse af tre rekombinante aldehyddehydrogenaser, der stammer fra kvæglinser og bakterierne Escherichia coli og Pseudomonas putida. Til regenerering af det katalytiske NAD+ coenzym, de anvendte H 2 O danner NAD-oxidase fra Streptococcus mutans. Den endelige bio-oxidation kører i vandig phosphatbuffer, under milde reaktionsbetingelser (40 ° C og atmosfærisk tryk) og forbruger kun dioxygen fra luft som oxidant.
Omfattende undersøgelse
For at undersøge potentialet for de tre enzymer, forskerne udførte en omfattende undersøgelse, hvor de testede enogtres strukturelt forskellige aldehyder. Størstedelen af disse substrater (alifatiske, aryl alifatisk, benzyl-, hetero-aromatiske og bicykliske aldehyder) blev omdannet med udbytter på langt over 60% og i mange tilfælde endda over 99%. De eneste undtagelser var nogleortho-substituerede benzaldehyder og to bicykliske heteroaromatiske aldehyder.
I alle tilfælde, kemoselektiviteten var perfekt:intet andet produkt blev påvist undtagen den forventede carboxylsyre. Dette betyder, at andre oxiderbare funktionaliteter (såsom hydroxyldelen, alkengrupper, arylgrupper, og svovl samt nitrogen -heteroatomer) forblev uberørte.
Hele celler
Da det til praktiske anvendelser foretrækkes at anvende hele celler frem for rensede enzymer, undgå tidskrævende og dyre rensningstrin, forskerne undersøgte også bio-oxidation medE. coli lyofiliserede hele celler såvel som hvileceller. Det viste sig, at tilskud af NAD+coenzym og NOx genanvendelsesenzym i nogle tilfælde kan udelades, da den mikrobielle vært producerer tilstrækkelig mængde coenzym, som kan genbruges af endogene E. coli -enzymer.
Forskerne konkluderer, at aldehyddehydrogenaser har potentiale til at blive det første valg for kemoselektiv oxidation af aldehyder til carboxylgrupper. Deres biokatalytiske metode er særligt attraktiv for oxidation af aldehyddele i molekyler, der besidder yderligere oxiderbare grupper. Fremtidig forskning vil fokusere på at forbedre enzymernes tolerance over for substratkoncentration og langsigtet stabilitet for at muliggøre endnu bredere anvendelse af disse enzymer.
 Varme artikler
Varme artikler
-
 Forskere beskriver strukturen af et potentielt luminescerende stofStrukturen af det nye stof. Kredit:Maksim Molokeev. En fysiker fra Siberian Federal University (SFU) og Kirensky Institute of Physics Federal Research Center KSC SB RAS (IF) har beskrevet strukt
Forskere beskriver strukturen af et potentielt luminescerende stofStrukturen af det nye stof. Kredit:Maksim Molokeev. En fysiker fra Siberian Federal University (SFU) og Kirensky Institute of Physics Federal Research Center KSC SB RAS (IF) har beskrevet strukt -
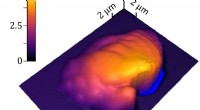 Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord
Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord -
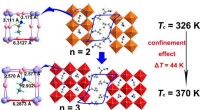 Forskere erhverver høj-Curie-temperatur lagdelt metalhalogenid ferroelektrik via bur-indesluttede e…Skematisk illustration af strategien. Kredit:Prof. LUO Junhuas gruppe Todimensionelle (2-D) organiske uorganiske hybridperovskit (OIHP) ferroelektriske stoffer har tiltrukket sig stor opmærksomhed
Forskere erhverver høj-Curie-temperatur lagdelt metalhalogenid ferroelektrik via bur-indesluttede e…Skematisk illustration af strategien. Kredit:Prof. LUO Junhuas gruppe Todimensionelle (2-D) organiske uorganiske hybridperovskit (OIHP) ferroelektriske stoffer har tiltrukket sig stor opmærksomhed -
 ABS af molekylære motorerHarald Platta, Rebecca Brinkmeier og Thomas Mastalski (fra venstre) i laboratoriet på Ruhr-Universität Bochum. Kredit:RUB, Kramer Peroxisomer er celleorganeller, der udfører en række funktioner, h
ABS af molekylære motorerHarald Platta, Rebecca Brinkmeier og Thomas Mastalski (fra venstre) i laboratoriet på Ruhr-Universität Bochum. Kredit:RUB, Kramer Peroxisomer er celleorganeller, der udfører en række funktioner, h
- Hvorfor har Winchester Mystery House ingen trapper?
- Nyopdaget enzym bruger en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugt
- Sådan trækkes blandede tal med Regrouping
- Hvorfor falder trykket, når volumen stiger?
- Hvordan tænder gadebelysningen automatisk om natten?
- Gør verden varmere:Indier forventede AC -eksplosion


