Supersimuleringer giver frisk indsigt i serotoninreceptorer
Kredit:A. James Clark School of Engineering, University of Maryland
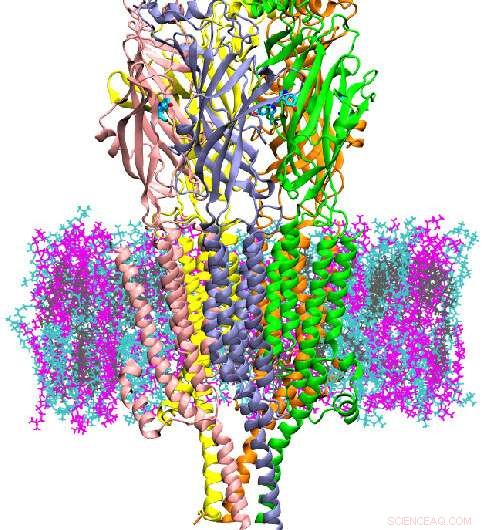
Forskere ved University of Maryland (UMD) og National Institute of Standards and Technology (NIST) har opdaget en måde at opdage den molekylære mekanisme, hvorved 5HT3A, en serotoninreceptor placeret ved neuronsynapsen, er aktiveret. At have en molekylær model af denne aktivering vil tillade test af farmaceutiske hæmmere ved hjælp af computermodeller i stedet for traditionelle eksperimenter, potentielt reducere omkostningerne og tiden ved screening af nye lægemidler.
Undersøgelsen ledet af Jeffery Klauda, en professor i kemisk og biomolekylær teknik (ChBE) ved University of Maryland (UMD), blev offentliggjort i Procedurer fra National Academy of Sciences ( PNAS ) i dag. Nicholas Guros, en ChBE kandidat forskningsassistent, tjente som førsteforfatter på undersøgelsen og blev co-rådgivet af Arvind Balijepalli, en maskiningeniør hos NIST.
5HT3A er en type protein kendt som en ionkanal, involveret i depression, angst og målrettet mod at reducere kemoterapi-induceret kvalme. Det regulerer strømmen af ioner ved den post-synaptiske kløft af neuroner. Forfatterne udførte computersimuleringer af 5HT3A i op til 20 mikrosekunder - meget længere end tidligere simuleringer udført for
"Hvis du tænker på molekylær dynamik (MD) som et molekylært mikroskop, dette betyder, at vi er i stand til at observere aktiveringsmekanismen i x10 længere end tidligere, " sagde Guros. "Nye beregningsevner kan give kraften til at observere den molekylære aktivering af komplekse proteiner på væsentligt længere tidsskalaer. Jo længere denne tidsskala, jo bedre validering kan vi have af eksperimentelle resultater for at vise, at MD-modeller er en robust metode til at studere protein og teste lægemidler."
Aktivering og desensibilisering af proteiner som 5HT3A sker over millisekunder, så mens tættere på den sande tidsskala, forskere er stadig noget bagud med at observere hele proteinets transportcyklus. Dette studie, imidlertid, var i stand til at give indsigt i virkningerne af serotoninbinding på udvikling af en præaktiv tilstand af 5HT3A, og hvordan membranlipiddiversitet påvirker proteinstruktur og funktion.
Meget simuleringsplads til at udforske med disse modeller er tilbage, og det er kun blevet gjort muligt i de sidste par år med fremskridt i beregningskraft. Specifikt, denne undersøgelse blev udført ved hjælp af en tilskudsbaseret tildeling på Anton2-supercomputeren, der vedligeholdes af Pittsburgh Supercomuting Center (PSC) og sponsoreret af DE Shaw-forskning. Traditionelle højtydende computerressourcer ville ikke være i stand til at nå tidsskalaen for denne undersøgelse.
Da computerhastighed og effekt stiger i fremtiden, gruppen håber at studere virkningerne af lægemidler, såsom granisetron eller ondansetron, i et forsøg på præcist at modellere deres virkninger på proteinet og undersøge andre målrettede terapier.
 Varme artikler
Varme artikler
-
 Mikrofluid chip til analyse af enkeltcellerKredit:Wiley Et par små celler, der er forskellige fra resten, kan have en stor effekt. For eksempel, enkelte kræftceller kan være resistente over for en bestemt kemoterapi - hvilket forårsager et
Mikrofluid chip til analyse af enkeltcellerKredit:Wiley Et par små celler, der er forskellige fra resten, kan have en stor effekt. For eksempel, enkelte kræftceller kan være resistente over for en bestemt kemoterapi - hvilket forårsager et -
 Miniaturiseret massespektrometer til Mars-udforskning har et enormt potentialeKredit:Brigham Young University BYU-forskere har skabt en miniaturiseret, bærbar version af et værktøj, der nu er i stand til at analysere Mars atmosfære - og det er blot en af dets utallige anv
Miniaturiseret massespektrometer til Mars-udforskning har et enormt potentialeKredit:Brigham Young University BYU-forskere har skabt en miniaturiseret, bærbar version af et værktøj, der nu er i stand til at analysere Mars atmosfære - og det er blot en af dets utallige anv -
 Ålegræssyre og resveratrol produceret af cellefabrikker for første gangSom et bevis på konceptet for sulfateringsprocessen i cellefabrikker, forskerne ville producere zosterinsyre. Denne syre findes i marinaplanten ålegræs og er et kraftigt antifoulingmiddel. Kredit:Chri
Ålegræssyre og resveratrol produceret af cellefabrikker for første gangSom et bevis på konceptet for sulfateringsprocessen i cellefabrikker, forskerne ville producere zosterinsyre. Denne syre findes i marinaplanten ålegræs og er et kraftigt antifoulingmiddel. Kredit:Chri -
 Forskere udvikler nyt system til undersøgelse af nye krydsbårne sygdommeKredit:stock.adobe.com Krydsbårne sygdomme er stigende, og især en dukker op i USA og Canada. Human babesiose er en infektion, der kan forårsage en række symptomer og endda døden. Lidt er kendt om
Forskere udvikler nyt system til undersøgelse af nye krydsbårne sygdommeKredit:stock.adobe.com Krydsbårne sygdomme er stigende, og især en dukker op i USA og Canada. Human babesiose er en infektion, der kan forårsage en række symptomer og endda døden. Lidt er kendt om
- 10 ting, vi troede var sande før den videnskabelige metode
- Sådan beregner du, hvor længe et batteri vil vare
- Hvordan påvirker udslæt fra andre væsner direkte mennesker?
- De fleste amerikanere undervurderer mindretalers miljøhensyn - også mindretal
- NASA investerede i at knække jordens kulstofpuslespil
- Kunne mennesker leve i lava -rør på månen?


