Omvendt brændselscelle omdanner affaldskulstof til værdifulde produkter med rekordhastigheder

Venstre mod højre:Adnan Ozden, Joshua Wicks, og F. Pelayo García de Arquer er blandt teammedlemmerne, der har designet en elektrolysator, der omdanner CO 2 til værdifulde produkter 10 gange hurtigere end tidligere versioner. Kredit:U of T Engineering/Daria Perevezentsev
Brændselsceller omdanner kemikalier til elektricitet. Nu, et ingeniørteam fra University of Toronto har tilpasset teknologi fra brændselsceller til at gøre det omvendte:udnytte elektricitet til at lave værdifulde kemikalier fra affaldskulstof (CO 2 ).
"I årtier, talentfulde forskere har udviklet systemer, der omdanner elektricitet til brint og tilbage igen, " siger professor Ted Sargent, en af de ledende forfattere af papiret udgivet i Videnskab . "Vores innovation bygger på denne arv, men ved at bruge kulstofbaserede molekyler, vi kan tilslutte direkte til eksisterende kulbrinteinfrastruktur."
I en brintbrændselscelle, brint og oxygen kommer sammen på overfladen af en katalysator. Den kemiske reaktion frigiver elektroner, som fanges af specialiserede materialer i brændselscellen og pumpes ind i et kredsløb.
Det modsatte af en brændselscelle er en elektrolysator, som bruger elektricitet til at drive en kemisk reaktion. Avisens forfattere er eksperter i at designe elektrolysatorer, der omdanner CO 2 ind i andre kulstofbaserede molekyler, såsom ethylen. Holdet omfatter ph.d. kandidat Adnan Ozden, som er superviseret af professor David Sinton, samt flere medlemmer af Sargents team, herunder ph.d. kandidat Joshua Wicks, postdoc F. Pelayo García de Arquer og tidligere postdoc Cao-Thang Dinh.
"Ethylen er et af de mest udbredte kemikalier i verden, " siger Wicks. "Det bruges til at lave alt fra frostvæske til græsplænemøbler. I dag er det afledt af fossile brændstoffer, men hvis vi i stedet kunne klare det ved at opgradere affalds-CO 2 , det ville give et nyt økonomisk incitament til at opfange kulstof."
Nutidens elektrolysatorer producerer endnu ikke ethylen i en skala, der er stor nok til at konkurrere med, hvad der er afledt af fossile brændstoffer. En del af udfordringen ligger i den unikke karakter af den kemiske reaktion, der omdanner CO 2 til ethylen og andre kulstofbaserede molekyler.
"Reaktionen kræver tre ting:CO 2 , som er en gas; hydrogen ioner, som kommer fra flydende vand; og elektroner, som overføres gennem en metalkatalysator, " siger Ozden. "Bringer de tre forskellige faser - især CO 2 - sammen er hurtigt udfordrende, og det er det, der har begrænset reaktionshastigheden."
I deres seneste elektrolyserdesign, holdet brugte et unikt arrangement af materialer til at overvinde udfordringerne med at bringe reaktanterne sammen. Elektroner leveres ved hjælp af en kobberbaseret katalysator, som teamet tidligere havde udviklet. Men i stedet for en flad metalplade, katalysatoren i den nye elektrolysator er i form af små partikler indlejret i et lag af et materiale kendt som Nafion.
Nafion er en ionomer - en polymer, der kan lede ladede partikler kendt som ioner. I dag, det er almindeligt anvendt i brændselsceller, hvor dens rolle er at transportere positivt ladede brint (H+) ioner rundt i reaktoren.

I den forbedrede elektrolysator, reaktionen sker i et tyndt lag, der kombinerer en kobberbaseret katalysator med Nafion, en ionledende polymer. Det unikke arrangement af disse materialer giver en reaktionshastighed, der er 10 gange højere end tidligere designs. Kredit:U of T Engineering/Daria Perevezentsev
"I vores eksperimenter, vi opdagede, at et bestemt arrangement af Nafion kan lette transporten af gasser såsom CO 2 , " siger García de Arquer. "Vores design gør det muligt for gasreaktanter at nå katalysatoroverfladen hurtigt nok og på en tilstrækkeligt fordelt måde til at øge reaktionshastigheden markant."
Da reaktionen ikke længere er begrænset af, hvor hurtigt de tre reaktanter kan samles, holdet var i stand til at omdanne CO 2 til ethylen og andre produkter 10 gange hurtigere end før. De opnåede dette uden at reducere reaktorens samlede effektivitet, hvilket betyder mere produkt til nogenlunde samme kapitalomkostning.
På trods af fremrykningen, enheden er stadig langt fra kommerciel levedygtighed. En af de store tilbageværende udfordringer har at gøre med stabiliteten af katalysatoren under de nye højere strømtætheder.
"Vi kan pumpe elektroner ind 10 gange hurtigere, hvilket er fantastisk, men vi kan kun betjene systemet i omkring ti timer, før katalysatorlaget bryder sammen, " siger Dinh. "Dette er stadig langt fra målet om tusindvis af timer, der ville være nødvendige for industriel anvendelse."
Dinh, som nu er professor i kemiteknik ved Queen's University, fortsætter arbejdet ved at undersøge nye strategier til stabilisering af katalysatorlaget, såsom yderligere ændring af den kemiske struktur af Nafion eller tilføjelse af yderligere lag for at beskytte den.
De andre teammedlemmer planlægger at arbejde med forskellige udfordringer, såsom at optimere katalysatoren til at producere andre kommercielt værdifulde produkter ud over ethylen.
"Vi valgte ethylen som et eksempel, men principperne her kan anvendes til syntese af andre værdifulde kemikalier, inklusive ethanol", siger Wicks. "Ud over dets mange industrielle anvendelser, ethanol er også meget brugt som brændstof."
Evnen til at producere brændstoffer, byggematerialer og andre produkter på en CO2-neutral måde er et vigtigt skridt i retning af at mindske vores afhængighed af fossile brændstoffer.
"Selv hvis vi holder op med at bruge olie til energi, vi får stadig brug for alle disse molekyler, " siger García de Arquer. "Hvis vi kan producere dem ved at bruge affalds-CO 2 og vedvarende energi, vi kan have en stor indflydelse i forhold til at dekarbonisere vores økonomi."
 Varme artikler
Varme artikler
-
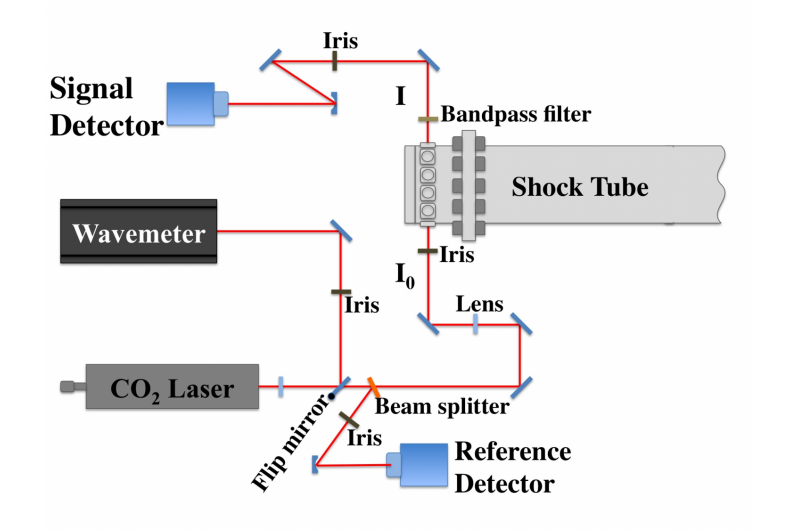 Giver en renere forbrændingNedbrydningen af DEC blev evalueret ved hjælp af en laserstråle, der passerede gennem et kompliceret system af spejle og linser (nederst), før den nåede stødrøret (øverst til venstre). Kredit:© 2017
Giver en renere forbrændingNedbrydningen af DEC blev evalueret ved hjælp af en laserstråle, der passerede gennem et kompliceret system af spejle og linser (nederst), før den nåede stødrøret (øverst til venstre). Kredit:© 2017 -
 Hvordan bakterier producerer manganoxid-nanopartiklerForskere studerede strukturen af et rekombinant enzym, der er ansvarlig for biomineralisering af Mn, give ledetråde til potentiel miljøsanering eller bioenergiproduktion. Kredit:Environmental Molecu
Hvordan bakterier producerer manganoxid-nanopartiklerForskere studerede strukturen af et rekombinant enzym, der er ansvarlig for biomineralisering af Mn, give ledetråde til potentiel miljøsanering eller bioenergiproduktion. Kredit:Environmental Molecu -
 Brug af kvanteprikker og en smartphone til at finde dræberbakterierForskerne Anwar Sunna (til højre) og Vinoth Kumar Rajendran med deres smartphone-aktiverede MRSA-detektor. Kredit:Sunna Lab En kombination af quantum dot nanoteknologi og et smartphonekamera kan s
Brug af kvanteprikker og en smartphone til at finde dræberbakterierForskerne Anwar Sunna (til højre) og Vinoth Kumar Rajendran med deres smartphone-aktiverede MRSA-detektor. Kredit:Sunna Lab En kombination af quantum dot nanoteknologi og et smartphonekamera kan s -
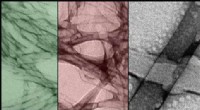 Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
- Gravitationsbølger kunne kaste lys over oprindelsen af sorte huller
- Politiuddannelse reducerede klager og magtanvendelse mod civile
- 4 enkle trin til at tage mere effektive noter
- Alvorlig tyfon Doksuri rammer det centrale Vietnam
- Amerikansk videnskab bliver lukket lige sammen med den føderale regering
- NASA -opfindelser, du kan bruge hver dag


