Hold det enkelt - Syntetisering af nyttige organiske forbindelser er nu blevet lettere og billigere

Kredit:CC0 Public Domain
Suzuki-Miyaura-reaktionen er en velkendt kemisk proces, hvor en reaktion mellem organiske borsyrer og arylhalogenider fører til syntese af "biaryl" -forbindelser, som er vigtige komponenter i forskellige lægemidler og kemiske produkter. Dette kaldes også krydskobling, som to arylmolekyler kombineres, eller krydskoblet, i denne proces. Fordi de organiske aromatiske molekyler - som dannes som følge af denne reaktion - har forskellige anvendelser, såsom i opløsningsmidler og lægemidler, at finde en måde at optimere de eksisterende krydskoblingsreaktioner på er afgørende. Det er derfor, i en ny undersøgelse offentliggjort i ACS katalysatorer , et hold forskere fra Japan, herunder Junior Assoc Prof Yuichiro Mutoh og Prof Shinichi Saito fra Tokyo University of Science, ønskede at kontrollere, om denne reaktion kan gøres mere effektiv.
"Beskyttet" organisk borsyre, som er en organisk borsyre med en 'maskeringsgruppe, 'bruges ofte som en forløber for borsyre i Suzuki-Miyaura-reaktionen. Fordi reaktiviteten af den beskyttede borsyre er lav, det tager ikke del i denne reaktion. Dermed, maskeringsgruppen skal fjernes for at reaktionen kan fortsætte, hvilket tilføjer endnu et trin til processen. Dette fik disse forskere til at spekulere på:hvad nu hvis de maskerede molekyler blev brugt direkte i reaktionen? Det ville føre os til en meget hurtigere, billigere teknik!
Prof Saito forklarer, "Fordi fjernelsen af maskeringsgruppen er nødvendig for at tilvejebringe de latente boronsyrer, der deltager i efterfølgende Suzuki-Miyaura-reaktioner, den direkte anvendelse af den beskyttede borsyre i en Suzuki-Miyaura-reaktion ville være yderst ønskelig med hensyn til antal trin og atomøkonomi. Dette ville hjælpe med at strømline syntesen af komplekse molekyler. "Den eneste udfordring var, at indtil nu, der var ingen kendt måde at bruge beskyttede boronsyrer direkte på uden at fjerne maskeringsgruppen først, og dermed, forskerne satte sig for at finde måder at gøre dette på.
Forskerne vidste, at processen krævede en palladiumkatalysator (et molekyle eller en forbindelse, der kan fremskynde en reaktion), en base, og to start -arylmolekyler. De fortsatte med at kontrollere, om reaktionen finder sted med et beskyttet molekyle. Til at starte med, de undersøgte forskellige basers indvirkning på reaktionen. De så, at når en bestemt kaliumbase, kaldet KOτ-Bu, var brugt, det resulterede i et højt udbytte af produkter, og denne effekt som ikke set med andre baser. Derefter, de testede forskellige palladium-baserede katalysatorer og så, at alle katalysatorer gav et lignende udbytte, angiver, at fælles palladium-baserede katalysatorsystemer kan bruges til krydskoblingen. Dette fik dem til at konkludere, at KOτ-Bu-basen spillede en afgørende rolle, hvis man skulle bruge beskyttet borsyre direkte.
Efter over et dusin vellykkede Suzuki-Miyaura-reaktioner med højt udbytte for forskellige biarylforbindelser, teamet gennemførte 'kontrol'-eksperimenter for at kontrollere andre variabler og for at få indsigt i de underliggende mekanismer i KOτ-Bu-basen. Specifikt, de kontrollerede, om den kemiske art var til stede i reaktionsblandingen, før reaktionen var fuldført, som afdækkede en mellemproduktforbindelse, der involverer KOτ-Bu-basen og borsyre-reagenset. Ved hjælp af teknikker som NMR-spektroskopi og enkelt-krystal røntgendiffraktionsanalyse, videnskabsmændene bekræftede, at nøglen til succes med disse krydskoblingsreaktioner er brugen af KOτ-Bu som basen, da det muliggør dannelsen af et aktivt borat, afgørende for reaktionen.
Metoden opdaget i denne undersøgelse giver indsigt i Suzuki-Miyaura-reaktionen og foreslår en ny måde, hvorpå de nødvendige trin for at bruge beskyttede borsyrer kan minimeres. Hele processen med at opnå biarylmolekyler blev båret i en enkelt gryde, hvilket er fordelagtigt i forhold til plads og omkostninger. Prof Saito slutter, "Vi udviklede en måde, hvorpå reaktionen kunne være trin- og potøkonomisk, funktioner, der har fået stor opmærksomhed i de seneste år. Dermed, denne undersøgelse åbner nye muligheder for brug af beskyttede borsyrer i forskellige koblingsreaktioner. "
På grund af sine nye fund, denne undersøgelse blev endda valgt til at være på forsiden af januar 2020 -udgaven af ACS -katalyse . Disse fund vil forhåbentlig hjælpe med at forenkle syntesen af vigtige komplekse molekyler, herunder farmaceutiske lægemidler, så flere mennesker kan drage fordel af fremskridt inden for de kemiske videnskaber.
 Varme artikler
Varme artikler
-
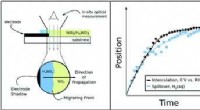 Brug af vedvarende elektricitet til industrielle hydrogeneringsreaktionerKredit:RCS Fra design af forbedrede batterier til brug af sol- og vindenergi til kemisk produktion af råvarer, University of Pittsburghs James McKone måder at kemiteknik kan gøre verden mere bæred
Brug af vedvarende elektricitet til industrielle hydrogeneringsreaktionerKredit:RCS Fra design af forbedrede batterier til brug af sol- og vindenergi til kemisk produktion af råvarer, University of Pittsburghs James McKone måder at kemiteknik kan gøre verden mere bæred -
 Kobberoxidfotokatoder:Lasereksperiment afslører placeringen af effektivitetstabEn grøn laserimpuls exciterer indledningsvis elektronerne i Cu2O; kun brøkdele af et sekund senere, en anden laserimpuls (UV-lys) sonderer energien af den exciterede elektron. Kredit:M. Kuensting/HZ
Kobberoxidfotokatoder:Lasereksperiment afslører placeringen af effektivitetstabEn grøn laserimpuls exciterer indledningsvis elektronerne i Cu2O; kun brøkdele af et sekund senere, en anden laserimpuls (UV-lys) sonderer energien af den exciterede elektron. Kredit:M. Kuensting/HZ -
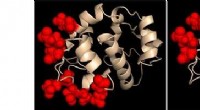 Forskere opdager, hvordan proteinpar styrer cellulære calciumsignalerProteinkemikers skildring af den calciumfølende region i to konstruerede STIM1-proteinvarianter. De steder, der blev ændret, er fremhævet i hvert tilfælde som røde kugler. Adfærden af disse to konst
Forskere opdager, hvordan proteinpar styrer cellulære calciumsignalerProteinkemikers skildring af den calciumfølende region i to konstruerede STIM1-proteinvarianter. De steder, der blev ændret, er fremhævet i hvert tilfælde som røde kugler. Adfærden af disse to konst -
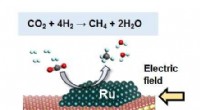 Ny metode omdanner kuldioxid til metan ved lave temperaturerHydrogenering af CO2 til CH4. Kredit:Sekine Laboratory, Waseda Universitet En ny metode udviklet af et team af Waseda-universitetets forskere under ledelse af professor Yasushi Sekine kan bidrage
Ny metode omdanner kuldioxid til metan ved lave temperaturerHydrogenering af CO2 til CH4. Kredit:Sekine Laboratory, Waseda Universitet En ny metode udviklet af et team af Waseda-universitetets forskere under ledelse af professor Yasushi Sekine kan bidrage
- BÆRERE fanger rekordindstilling røntgenudbrud
- Klimasmart landbrug for at sikre en fødevaresikker fremtid
- Forskning viser, hvordan man kan forbedre bindingen mellem implantater og knogler
- Hvad tiltrækker os mest til et turistmål? Seværdigheder, kultur og gastronomi
- Ultrahurtig, on-chip PCR kunne fremskynde diagnosen under pandemier
- Forskere producerer 50x mere stabilt adsorbent


