Metoden giver høj mængde af D-lactat ved hjælp af cyanobakterier, kunne revolutionere produktionen af bioplast
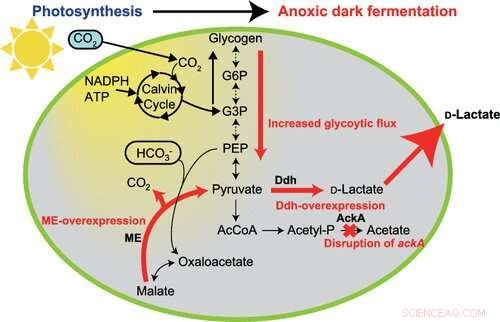
Figur 1:Vejen til omdannelse af kuldioxid til D-laktat. Synechocystis sp. PCC 6803 producerer glykogen inde i sine celler fra CO2 og lys. Det blev afsløret, at når Synechocystis sp. PCC 6803, der har akkumuleret glykogen, anbringes i anoxiske mørke forhold, dette aktiverer den metaboliske vej (angivet med de røde pile), som fremmer D-lactonproduktionen. Kredit:Kobe University
Et forskningshold ledet af Kobe University har belyst mekanismen, hvorved cyanobakterier (Synechocystis sp. PCC 6803) producerer D-lactat, viser, at æblesyreenzym letter denne produktion. Efterfølgende det lykkedes dem at producere verdens højeste mængde (26,6 g/L) af D-lactat direkte fra CO 2 og lys ved at modificere D-lactat-syntesevejen ved hjælp af genteknologi.
Det forventes, at denne succes vil bidrage til udviklingen af vigtige procesteknologier til fremstilling af polymælkesyre, som bruges til fremstilling af bionedbrydelig plast. Dette kunne være med til at gøre konceptet om et bæredygtigt, et lavt CO2-samfund en realitet.
Forskergruppen bestod af professor HASUNUMA Tomohisa (fra Kobe Universitys Engineering Biology Research Center), Projektlektor HIDESE Ryota (fra Kobe University's Graduate School of Science, Technology and Innovation) og lektor OSANAI Takashi (fra Meiji University's School of Agriculture).
Resultaterne af denne forskning blev offentliggjort online i det internationale videnskabelige tidsskrift ACS syntetisk biologi den 31. januar, 2020.
Udnyttelsen af bioproduktion til at syntetisere alsidige kemiske forbindelser og funktionelle råmaterialer, der normalt er afledt af olie, er afgørende for både miljøet og ressourcernes bæredygtighed. I de seneste år, bioproduktionsmetoder ved hjælp af mikrober har fået opmærksomhed. Blandt disse mikrober er mikroalger. Det er muligt at fremstille forskellige nyttige stoffer som olier og pigmenter fra mikroalger ved hjælp af sollys og CO 2 .
Cyanobakterier er en type hurtigtvoksende mikroalger, som er lette at genmodificere. Cyanobakterier er blevet brugt til at producere D-lactat før, det lave udbytte har imidlertid været en hindring, som forhindrer den praktiske anvendelse af disse metoder.
Cyanobakterier bliver CO 2 ind i sukkerglykogenet via fotosyntesen. Hvis cyanobakterier, som har akkumuleret glykogen inde i sine celler, placeres i et mørkt miljø uden ilt, glykogenet metaboliseres af cyanobakterierne, og det udskiller organiske syrer (såsom rav og mælkesyre) i vækstmediet.
For at syntetisere D-lactat fra cyanobakterier, der skal en stigning i pyruvatproduktionen til. Denne forskergruppe opdagede, at æblesyreenzymet, som omdanner æblesyre til pyruvat, er afgørende for produktionen af D-laktat. De brugte dynamisk metabolomik til at belyse mekanismen bag D-laktatproduktion. Gennem denne analyse, de opdagede, at når for meget æblesyre produceres inde i cellerne, æblesyre omdannes ikke kun til pyruvat, men også vejen til at producere pyruvat fra glykogen er aktiveret (figur 1). D-lactat biosyntetiseres fra pyruvat af D-lactat dehydrogenase. Forskergruppen lykkedes med at producere 26,6 g/L D-lactat med en omdannelsesrate på 94,3 % fra det akkumulerede glykogen ved at genmanipulere D-lactat-dehydrogenasen for at optimere dens funktion (Figur 2).
Denne forskning repræsenterer et vigtigt fremskridt hen imod udviklingen af en industriel proces til fremstilling af D-lactat fra CO 2 . Gruppen har til formål at fortsætte med at booste D-laktatproduktionen gennem optimering af metaboliske veje og analyse af dyrkningsbetingelser.
Der er et stort marked for D-laktat, som kan bruges som råmateriale i produktionen stereokompleks PLA, der er en biologisk nedbrydelig plast. På den anden side, høj renhed og produktivitet er påkrævet for at gøre biologisk syntetisering af D-lactat ved hjælp af mikrober levedygtig. Der findes bioproduktionsmetoder, der bruger heterotrofe mikrober som E. coli, disse bruger dog sukker (glukose) fra majs eller sukkerrør som energikilde til produktion. Det betyder, at dyrkning af disse planter til bioproduktion forårsager en lang række problemer, såsom konkurrence med fødevarekilder, brug af agerjord og ferskvandsressourcer, og bidrag til miljøødelæggelse (f.eks. skovrydning).
Cyanobakterier, på den anden side, er en ideel mikrobe til fremstilling af nyttige stoffer, da det kan omdanne CO 2 fikseres via fotosyntese til forskellige målforbindelser. Ud over, cyanobakterier har en meget højere fotosynteseevne end planter, hvilket betyder, at den endda kan dyrkes under stærkt lys. Det kræver ikke jord og mange sorter kan dyrkes i havvand. Derfor er det håbet, at cyanobakterier kan udgøre det ultimative grundlag for bioproduktion, da det kun kræver sollys, CO 2 og havvand.
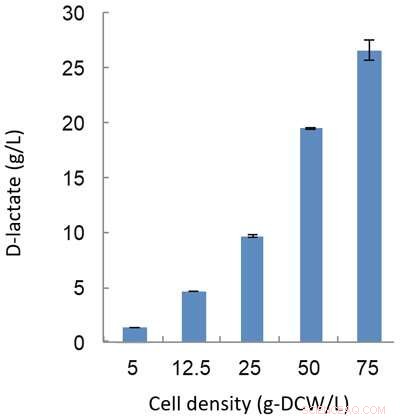
Figur 2:D-lactonproduktionshastighed for genetisk modificerede cyanobakterier. Under anoxiske mørke forhold, celletætheden af den fermenterede cyanobakterieopløsning steg. Dette førte til den succesrige produktion af 26,6 g/L D-lactat, verdens højeste rate ved brug af en autotrof mikroorganisme. Kredit:Kobe University
Det er almindeligt kendt, at cyanobakterier kan være en måde at syntetisere D-lactat på, og der er gjort forsøg på at øge D-lactatproduktionen ved hjælp af genetisk modifikation. Imidlertid, næsten alle systemer, der producerer D-lactat, er forbundet med formering via fotosyntese, så lave mængder af dette målstof syntetiseres. Årsagen til dette er, at mekanismen for D-laktatproduktion i cyanobakterier ikke er blevet godt forstået.
Metabolomanalyseteknikker giver forskere mulighed for både at identificere og beregne mængden af forbindelser, der findes inde i celler. Denne forskergruppe udviklede "Dynamic Metabolomics", som gjorde det muligt for dem at observere mængden af stoffer, der metaboliseres over tid.
Synechocystis sp. PCC 6803 cyanobakterier brugt i denne undersøgelse er en af de mest almindeligt undersøgte cyanobakterier på verdensplan. Det er en modelorganisme for fotosyntatproduktion, fordi den er nem at genmodificere og vokser hurtigt. Tidligere forskning udført af denne gruppe ved hjælp af dynamisk metabolomik viste, at ravsyre hovedsageligt produceres via æblesyre i Synechocystis sp. PCC 6803. Den aktuelle undersøgelse fokuserede på æblesyreenzym, som omdanner æblesyre til pyruvat. Først, de havde til formål at belyse virkningerne af æblesyreenzym på metabolismen af Synechocystis sp. PCC 6803 gennem dynamisk metabolomics. Deres efterfølgende mål var at øge D-lactatproduktionen ved hjælp af metabolisk manipulation.
Forskningsmetodologi
To typer celler blev skabt for at udførligt undersøge mekanismen bag D-lactatproduktion:1. Celler, der ikke havde nogen æblesyreenzymfunktion, og 2. Celler, hvor denne funktion var optimeret, fører til en overekspression af æblesyreenzym.
Dynamisk metabolomik blev brugt til at analysere forskellen i metabolismen mellem disse to celler. Det viste sig, at der blev produceret mere pyruvat fra glykogen, når niveauet af æblesyre i cellerne var lavt (figur 1).
Forskergruppen genmodificerede yderligere æbleenzym-optimerede celler til at overudtrykke D-lactat-dehydrogenase, og forbedrede D-lactat-dehydrogenasens funktion til at producere D-lactat fra pyruvat. Ud over, gruppen gensplejsede cellerne til at fjerne enzymet acetatkinase for at undertrykke produktionen af biproduktsyrer.
Den modificerede Synechocystis sp. PCC 6803 blev derefter dyrket i et mørkt anoxisk miljø (fermenteringsbetingelser). Under disse forhold, cellerne nåede den optimale tæthed. Denne forskergruppe oversteg langt verdens hidtil højeste udbytte af D-lactat (10,7 g/L), ved at producere 26,6 g/l med en hastighed på 0,185 g/l/h (figur 2). Det menes, at dette fund kan bidrage til en billig proces til fremstilling af høje niveauer af D-lactat.
Yderligere forskning
Cyanobakterier kan bruges til at producere mange alsidige kemiske forbindelser og funktionelle råmaterialer, denne teknologi er dog endnu ikke veludviklet nok til at blive implementeret i industriel skala. Det store problem er, at lavere niveauer af målforbindelsen produceres ved hjælp af cyanobakterier, sammenlignet med de mængder, der produceres ved brug af heterotrofe mikroorganismer. Den nuværende forskning har vist, at den dynamiske metabolomiske analyse er yderst effektiv til at evaluere funktionen af Synechocystis. Baseret på resultatet af den dynamiske metabolomik, denne gruppe gjorde det muligt for Synechocystis at yde deres fulde potentiale ved at genetisk modificere deres stofskifte.
Det er håbet, at en forøgelse af cyanobakteriers fotosyntetiske produktivitet gennem dynamisk metabolomik og metabolisk manipulation kan bidrage til realiseringen af en bæredygtig, lavemissionssamfund.
Sidste artikelKollagen kan modstå flere belastninger end hidtil kendt
Næste artikelMagnetiske tænder afsløret ved hjælp af kvantebilleder
 Varme artikler
Varme artikler
-
 Ny undersøgelse præsenterer højaktive ozygenerede grupper i kulstofmaterialer til oxygenreduktion…Figur 1. Ydeevnekarakteriseringerne af ORHP. Kredit:Professor Jong-Beom Baek, UNIST Hydrogenperoxid (H 2 O 2 ) har fundet mange anvendelser i den moderne industri, herunder at fungere som en g
Ny undersøgelse præsenterer højaktive ozygenerede grupper i kulstofmaterialer til oxygenreduktion…Figur 1. Ydeevnekarakteriseringerne af ORHP. Kredit:Professor Jong-Beom Baek, UNIST Hydrogenperoxid (H 2 O 2 ) har fundet mange anvendelser i den moderne industri, herunder at fungere som en g -
 Forskere opdager unikke multifibrillære fibreElektrospinning af en multifibrillær polyacrylonitrilfiber. Kredit:University of Bayreuth / Rennecke. Stærk og sej, men alligevel så lette som en fjer - materialer med denne enestående kombination
Forskere opdager unikke multifibrillære fibreElektrospinning af en multifibrillær polyacrylonitrilfiber. Kredit:University of Bayreuth / Rennecke. Stærk og sej, men alligevel så lette som en fjer - materialer med denne enestående kombination -
 Video:Hvordan fungerer aircondition?Kredit:The American Chemical Society Klimaanlæg udfører den tilsyneladende magiske bedrift at lave luften inde i et hjem, bil eller indkøbscenter lækkert køligt. Kilden til den søde lettelse er ke
Video:Hvordan fungerer aircondition?Kredit:The American Chemical Society Klimaanlæg udfører den tilsyneladende magiske bedrift at lave luften inde i et hjem, bil eller indkøbscenter lækkert køligt. Kilden til den søde lettelse er ke -
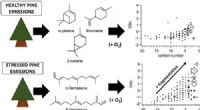 Bladlusstressede fyrretræer viser forskellig sekundær organisk aerosoldannelseKredit:American Chemical Society Planter udsender gasser, kaldet flygtige organiske forbindelser (VOCer), der kommer ind i atmosfæren, hvor de kan interagere med andre naturlige og menneskeskabte
Bladlusstressede fyrretræer viser forskellig sekundær organisk aerosoldannelseKredit:American Chemical Society Planter udsender gasser, kaldet flygtige organiske forbindelser (VOCer), der kommer ind i atmosfæren, hvor de kan interagere med andre naturlige og menneskeskabte
- Næste generation af fotodetektorkamera, der skal implementeres under demonstrationsmission for robo…
- Smeltende isbjerge er nøglen til sekvensen af en istid, finder forskerne
- Nuklear diagnostik hjælper med at bane vej for antændelse på NIF inertial indeslutningsfusion
- Fed idé:Magma opbevaret i kølerum før gigantisk vulkanudbrud
- Mandela -effekten:Hvorfor husker vi begivenheder, der ikke opstod
- Ulve viste sig at være mere samarbejdsvillige med deres egen slags end hunde med deres


